Gás nobre - Noble gas
| gases nobres | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|||||||||||
|
|||||||||||
| ↓ Período | |||||||||||
| 1 |
Hélio (He) 2 |
||||||||||
| 2 |
Neon (Ne) 10 |
||||||||||
| 3 |
Argônio (Ar) 18 |
||||||||||
| 4 |
Criptônio (Kr) 36 |
||||||||||
| 5 |
Xenon (Xe) 54 |
||||||||||
| 6 |
Radon (Rn) 86 |
||||||||||
| 7 |
Oganesson (Og) 118 |
||||||||||
|
Lenda
|
|||||||||||
Os gases nobres (historicamente também os gases inertes ; às vezes chamados de aerogênios ) constituem uma classe de elementos químicos com propriedades semelhantes; sob condições padrão , são todos gases monoatômicos inodoros, incolores com reatividade química muito baixa . Os seis gases nobres que ocorrem naturalmente são hélio (He), néon (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe) e o radônio radioativo (Rn).
Oganesson (Og) é um elemento altamente radioativo produzido sinteticamente, com várias previsões para ser outro gás nobre, ou para quebrar a tendência e ser reativo, devido a efeitos relativísticos . Em parte devido à meia-vida extremamente curta de 0,7 ms de seu único isótopo conhecido , sua química ainda não foi investigada.
Para os primeiros seis períodos da tabela periódica , os gases nobres são exatamente os membros do grupo 0 . Os gases nobres são tipicamente altamente não reativos, exceto quando sob condições extremas particulares. A inércia dos gases nobres os torna muito adequados em aplicações onde reações não são desejadas. Por exemplo, o argônio é usado em lâmpadas incandescentes para evitar a oxidação do filamento quente de tungstênio; além disso, o hélio é usado na respiração do gás por mergulhadores de águas profundas para prevenir a toxicidade do oxigênio, nitrogênio e dióxido de carbono (hipercapnia) .
As propriedades dos gases nobres podem ser bem explicadas por teorias modernas da estrutura atômica : sua camada externa de elétrons de valência é considerada "cheia", dando-lhes pouca tendência para participar de reações químicas, e foi possível preparar apenas um algumas centenas de compostos de gases nobres . Os pontos de fusão e ebulição de um determinado gás nobre são próximos, diferindo em menos de 10 ° C (18 ° F); ou seja, eles são líquidos em apenas uma pequena faixa de temperatura.
Néon, argônio, criptônio e xenônio são obtidos do ar em uma unidade de separação de ar usando os métodos de liquefação de gases e destilação fracionada . O hélio é proveniente de campos de gás natural que têm altas concentrações de hélio no gás natural , usando técnicas de separação criogênica de gás , e o radônio é geralmente isolado da decomposição radioativa de compostos de rádio , tório ou urânio dissolvidos . Os gases nobres têm várias aplicações importantes em setores como iluminação, soldagem e exploração espacial. Um gás respiratório de hélio-oxigênio é frequentemente usado por mergulhadores em águas profundas em águas salgadas de mais de 55 m (180 pés). Depois que os riscos causados pela inflamabilidade do hidrogênio se tornaram aparentes no desastre de Hindenburg , ele foi substituído por hélio em dirigíveis e balões .
História
Gás nobre é traduzido do substantivo alemão Edelgas , usado pela primeira vez em 1898 por Hugo Erdmann para indicar seu nível extremamente baixo de reatividade. O nome faz uma analogia com o termo " metais nobres ", que também apresentam baixa reatividade. Os gases nobres também foram chamados de gases inertes , mas este rótulo foi reprovado, pois muitos compostos de gases nobres são agora conhecidos. Gases raros é outro termo que foi usado, mas também é impreciso porque o argônio forma uma parte considerável (0,94% em volume, 1,3% em massa) da atmosfera da Terra devido à decomposição do potássio-40 radioativo .
Pierre Janssen e Joseph Norman Lockyer descobriram um novo elemento em 18 de agosto de 1868 enquanto observavam a cromosfera do Sol , e o chamaram de hélio em homenagem à palavra grega para o Sol, ἥλιος ( hḗlios ). Nenhuma análise química foi possível na época, mas o hélio foi posteriormente descoberto como um gás nobre. Antes deles, em 1784, o químico e físico inglês Henry Cavendish havia descoberto que o ar contém uma pequena proporção de uma substância menos reativa que o nitrogênio . Um século depois, em 1895, Lord Rayleigh descobriu que as amostras de nitrogênio do ar tinham uma densidade diferente do nitrogênio resultante de reações químicas . Junto com o cientista escocês William Ramsay da University College de Londres , Lord Rayleigh teorizou que o nitrogênio extraído do ar foi misturado com outro gás, levando a um experimento que isolou com sucesso um novo elemento, o argônio, da palavra grega ἀργός ( argós , "ocioso "ou" preguiçoso "). Com essa descoberta, eles perceberam que uma classe inteira de gases estava faltando na tabela periódica. Durante sua busca por argônio, Ramsay também conseguiu isolar o hélio pela primeira vez enquanto aquecia cleveita , um mineral. Em 1902, tendo aceitado as evidências para os elementos hélio e argônio, Dmitri Mendeleev incluiu esses gases nobres como o grupo 0 em seu arranjo dos elementos, que mais tarde se tornaria a tabela periódica.
Ramsay continuou sua busca por esses gases usando o método de destilação fracionada para separar o ar líquido em vários componentes. Em 1898, ele descobriu os elementos Krypton , neon e xenônio , e nomeou-los após as palavras gregas κρυπτός ( kryptós , "escondido"), νέος ( Néos , "novo"), e ξένος ( ksénos , "estranho"), respectivamente . O radônio foi identificado pela primeira vez em 1898 por Friedrich Ernst Dorn e foi denominado emanação do rádio , mas não foi considerado um gás nobre até 1904, quando suas características foram consideradas semelhantes às de outros gases nobres. Rayleigh e Ramsay receberam os Prêmios Nobel de Física e Química de 1904 , respectivamente, por sua descoberta dos gases nobres; nas palavras de JE Cederblom, então presidente da Royal Swedish Academy of Sciences , "a descoberta de um grupo inteiramente novo de elementos, do qual nenhum representante único era conhecido com certeza, é algo totalmente único na história da química, sendo intrinsecamente um avanço na ciência de significado peculiar ".
A descoberta dos gases nobres ajudou no desenvolvimento de uma compreensão geral da estrutura atômica . Em 1895, o químico francês Henri Moissan tentou formar uma reação entre o flúor , o elemento mais eletronegativo , e o argônio, um dos gases nobres, mas falhou. Os cientistas não conseguiram preparar compostos de argônio até o final do século 20, mas essas tentativas ajudaram a desenvolver novas teorias da estrutura atômica. Aprendendo com esses experimentos, o físico dinamarquês Niels Bohr propôs em 1913 que os elétrons nos átomos são organizados em camadas ao redor do núcleo e que, para todos os gases nobres, exceto o hélio, a camada mais externa sempre contém oito elétrons. Em 1916, Gilbert N. Lewis formulou a regra do octeto , que concluiu que um octeto de elétrons na camada externa era o arranjo mais estável para qualquer átomo; este arranjo fez com que eles não reagissem com outros elementos, uma vez que não precisavam de mais elétrons para completar sua camada externa.
Em 1962, Neil Bartlett descobriu o primeiro composto químico de um gás nobre, o hexafluoroplatinato de xenônio . Compostos de outros gases nobres foram descobertos logo depois: em 1962 para o radônio, difluoreto de radônio ( RnF
2), que foi identificado por técnicas de radiotraçador e em 1963 para criptônio, difluoreto de criptônio ( KrF
2) O primeiro composto estável de argônio foi relatado em 2000, quando o fluorohidreto de argônio (HArF) foi formado a uma temperatura de 40 K (-233,2 ° C; -387,7 ° F).
Em outubro de 2006, cientistas do Joint Institute for Nuclear Research e do Lawrence Livermore National Laboratory criaram com sucesso oganesson sintético , o sétimo elemento do grupo 18, bombardeando califórnio com cálcio.
Propriedades físicas e atômicas
| Propriedade | Hélio | Néon | Argônio | Krypton | Xenon | Radon | Oganesson |
|---|---|---|---|---|---|---|---|
| Densidade (g / dm 3 ) | 0,1786 | 0,9002 | 1,7818 | 3,708 | 5,851 | 9,97 | 7200 (previsto) |
| Ponto de ebulição (K) | 4,4 | 27,3 | 87,4 | 121,5 | 166,6 | 211,5 | 450 ± 10 (previsto) |
| Ponto de fusão (K) | - | 24,7 | 83,6 | 115,8 | 161,7 | 202,2 | 325 ± 15 (previsto) |
| Entalpia de vaporização (kJ / mol) | 0,08 | 1,74 | 6,52 | 9,05 | 12,65 | 18,1 | - |
| Solubilidade em água a 20 ° C (cm 3 / kg) | 8,61 | 10,5 | 33,6 | 59,4 | 108,1 | 230 | - |
| Número atômico | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| Raio atômico (calculado) ( pm ) | 31 | 38 | 71 | 88 | 108 | 120 | - |
| Energia de ionização (kJ / mol) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 | 839 (previsto) |
| Eletro-negatividade | 4,16 | 4,79 | 3,24 | 2,97 | 2,58 | 2,60 | - |
Os gases nobres têm força interatômica fraca e, conseqüentemente, têm pontos de fusão e ebulição muito baixos . Eles são todos gases monoatômicos sob condições padrão , incluindo os elementos com massas atômicas maiores do que muitos elementos normalmente sólidos. O hélio tem várias qualidades únicas quando comparado com outros elementos: seu ponto de ebulição a 1 atm é inferior ao de qualquer outra substância conhecida; é o único elemento conhecido que exibe superfluidez ; e, é o único elemento que não pode ser solidificado por resfriamento à pressão atmosférica (um efeito explicado pela mecânica quântica como sua energia de ponto zero é muito alta para permitir o congelamento) - uma pressão de 25 atmosferas padrão (2.500 kPa ; 370 psi ) deve ser aplicado a uma temperatura de 0,95 K (-272.200 ° C; -457,960 ° F) para convertê-lo em um sólido, enquanto uma pressão de cerca de 115 kbar é necessária à temperatura ambiente. Os gases nobres até o xenônio têm vários isótopos estáveis . O radônio não tem isótopos estáveis ; seu isótopo de vida mais longa, 222 Rn , tem meia-vida de 3,8 dias e decai para formar hélio e polônio , que finalmente decai para chumbo . Os pontos de fusão e ebulição aumentam ao descer o grupo.

Os átomos de gases nobres, como átomos na maioria dos grupos, aumentam constantemente no raio atômico de um período para o outro devido ao aumento do número de elétrons. O tamanho do átomo está relacionado a várias propriedades. Por exemplo, o potencial de ionização diminui com um raio crescente porque os elétrons de valência nos gases nobres maiores estão mais distantes do núcleo e, portanto, não são mantidos tão fortemente unidos pelo átomo. Os gases nobres possuem o maior potencial de ionização entre os elementos de cada período, o que reflete a estabilidade de sua configuração eletrônica e está relacionado à sua relativa falta de reatividade química. Alguns dos gases nobres mais pesados, entretanto, têm potenciais de ionização pequenos o suficiente para serem comparáveis aos de outros elementos e moléculas . Foi a percepção de que o xenônio tem um potencial de ionização semelhante ao da molécula de oxigênio que levou Bartlett a tentar oxidar o xenônio usando hexafluoreto de platina , um agente oxidante conhecido por ser forte o suficiente para reagir com o oxigênio. Gases nobres não podem aceitar um elétron para formar ânions estáveis ; ou seja, eles têm uma afinidade de elétron negativa .
As propriedades físicas macroscópicas dos gases nobres são dominadas pelas forças fracas de van der Waals entre os átomos. A força atrativa aumenta com o tamanho do átomo como resultado do aumento da polarizabilidade e da diminuição do potencial de ionização. Isso resulta em tendências de grupo sistemáticas: conforme se desce do grupo 18, o raio atômico e com ele as forças interatômicas aumentam, resultando em um ponto de fusão, ponto de ebulição, entalpia de vaporização e solubilidade crescentes . O aumento da densidade se deve ao aumento da massa atômica .
Os gases nobres são gases quase ideais sob condições padrão, mas seus desvios da lei dos gases ideais forneceram pistas importantes para o estudo das interações intermoleculares . O potencial de Lennard-Jones , frequentemente usado para modelar interações intermoleculares, foi deduzido em 1924 por John Lennard-Jones a partir de dados experimentais sobre argônio antes do desenvolvimento da mecânica quântica fornecer as ferramentas para a compreensão das forças intermoleculares a partir dos primeiros princípios . A análise teórica dessas interações tornou-se tratável porque os gases nobres são monoatômicos e os átomos esféricos, o que significa que a interação entre os átomos é independente de direção, ou seja, isotrópica .
Propriedades quimicas

Os gases nobres são incolores, inodoros, insípidos e não inflamáveis sob condições padrão. Eles já foram rotulados como grupo 0 na tabela periódica porque se acreditava que tinham valência zero, o que significa que seus átomos não podem se combinar com os de outros elementos para formar compostos . No entanto, foi descoberto mais tarde que alguns de fato formam compostos, fazendo com que esse rótulo caia em desuso.
Configuração de elétron
Como outros grupos, os membros desta família mostram padrões em sua configuração eletrônica , especialmente as camadas mais externas, resultando em tendências no comportamento químico:
| Z | Elemento | Nº de elétrons / camada |
|---|---|---|
| 2 | hélio | 2 |
| 10 | néon | 2, 8 |
| 18 | argônio | 2, 8, 8 |
| 36 | criptônio | 2, 8, 18, 8 |
| 54 | xenônio | 2, 8, 18, 18, 8 |
| 86 | radônio | 2, 8, 18, 32, 18, 8 |
| 118 | oganesson | 2, 8, 18, 32, 32, 18, 8 (previsto) |
Os gases nobres têm camadas de elétrons de valência completa . Os elétrons de valência são os elétrons mais externos de um átomo e normalmente são os únicos elétrons que participam das ligações químicas . Os átomos com camadas de elétrons de valência total são extremamente estáveis e, portanto, não tendem a formar ligações químicas e têm pouca tendência a ganhar ou perder elétrons. No entanto, gases nobres mais pesados, como o radônio, são mantidos com menos firmeza pela força eletromagnética do que gases nobres mais leves, como o hélio, tornando mais fácil remover elétrons externos de gases nobres pesados.
Como resultado de uma camada completa, os gases nobres podem ser usados em conjunto com a notação de configuração eletrônica para formar a notação de gás nobre . Para fazer isso, o gás nobre mais próximo que precede o elemento em questão é escrito primeiro e, em seguida, a configuração do elétron é continuada desse ponto em diante. Por exemplo, a notação eletrônica do fósforo é 1s 2 2s 2 2p 6 3s 2 3p 3 , enquanto a notação do gás nobre é [Ne] 3s 2 3p 3 . Essa notação mais compacta torna mais fácil identificar os elementos e é mais curta do que escrever a notação completa dos orbitais atômicos .
Os gases nobres cruzam a fronteira entre os blocos - o hélio é um elemento s enquanto o resto dos membros são elementos p - o que é incomum entre os grupos IUPAC. A maioria, senão todos os outros grupos IUPAC, contém elementos de um bloco cada.
Compostos
Os gases nobres apresentam reatividade química extremamente baixa ; conseqüentemente, apenas algumas centenas de compostos de gases nobres foram formados. Os compostos neutros nos quais o hélio e o néon estão envolvidos nas ligações químicas não foram formados (embora existam alguns íons contendo hélio e haja alguma evidência teórica para alguns íons neutros contendo hélio), enquanto o xenônio, o criptônio e o argônio mostraram apenas reatividade menor. A reatividade segue a ordem Ne <He <Ar <Kr <Xe <Rn ≪ Og.
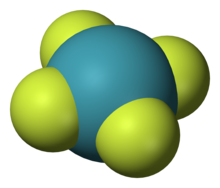
Em 1933, Linus Pauling previu que os gases nobres mais pesados poderiam formar compostos com flúor e oxigênio. Ele previu a existência de hexafluoreto de criptônio ( KrF
6) e hexafluoreto de xenônio ( XeF
6), especulou que XeF
8pode existir como um composto instável e sugeriu que o ácido xênico poderia formar sais de perxenato . Essas previsões mostraram-se geralmente precisas, exceto que XeF
8agora é considerado termodinamicamente e cineticamente instável.
Os compostos de xenônio são os mais numerosos dos compostos de gases nobres que se formaram. A maioria deles tem o átomo de xenônio no estado de oxidação de +2, +4, +6 ou +8 ligado a átomos altamente eletronegativos , como flúor ou oxigênio, como no difluoreto de xenônio ( XeF
2), tetrafluoreto de xenônio ( XeF
4), hexafluoreto de xenônio ( XeF
6), tetróxido de xenônio ( XeO
4), e perxenato de sódio ( Na
4XeO
6) O xenônio reage com o flúor para formar vários fluoretos de xenônio de acordo com as seguintes equações:
- Xe + F 2 → XeF 2
- Xe + 2F 2 → XeF 4
- Xe + 3F 2 → XeF 6
Alguns desses compostos foram usados em síntese química como agentes oxidantes ; XeF
2, em particular, está disponível comercialmente e pode ser usado como um agente de fluoração . Em 2007, cerca de quinhentos compostos de xenônio ligados a outros elementos foram identificados, incluindo compostos de organoxenônio (contendo xenônio ligado ao carbono) e xenônio ligado ao nitrogênio, cloro, ouro, mercúrio e o próprio xenônio. Compostos de xenônio ligados ao boro, hidrogênio, bromo, iodo, berílio, enxofre, titânio, cobre e prata também foram observados, mas apenas em baixas temperaturas em matrizes de gases nobres ou em jatos supersônicos de gases nobres.
O radônio é mais reativo do que o xenônio e forma ligações químicas mais facilmente do que o xenônio. No entanto, devido à alta radioatividade e meia-vida curta dos isótopos de radônio , apenas alguns fluoretos e óxidos de radônio foram formados na prática. O radônio vai mais longe em direção ao comportamento metálico do que o xenônio; o difluoreto RnF 2 é altamente iônico, e o catiônico Rn 2+ é formado em soluções de fluoreto de halogênio. Por esta razão, o impedimento cinético torna difícil oxidar o radônio além do estado +2. Apenas experimentos com traçadores parecem ter tido sucesso em fazê-lo, provavelmente formando RnF 4 , RnF 6 e RnO 3 .
O criptônio é menos reativo do que o xenônio, mas vários compostos foram relatados com o criptônio no estado de oxidação de +2. O difluoreto de criptônio é o mais notável e facilmente caracterizado. Em condições extremas, o criptônio reage com o flúor para formar KrF 2 de acordo com a seguinte equação:
- Kr + F 2 → KrF 2
Os compostos nos quais o criptônio forma uma ligação simples com o nitrogênio e o oxigênio também foram caracterizados, mas só são estáveis abaixo de −60 ° C (−76 ° F) e −90 ° C (−130 ° F), respectivamente.
Átomos de criptônio quimicamente ligados a outros não-metais (hidrogênio, cloro, carbono), bem como alguns metais de transição tardia (cobre, prata, ouro) também foram observados, mas apenas em baixas temperaturas em matrizes de gases nobres ou em jatos supersônicos de gases nobres . Condições semelhantes foram usadas para obter os primeiros compostos de argônio em 2000, como o fluorohidreto de argônio (HArF), e alguns ligados aos metais de transição tardia cobre, prata e ouro. Em 2007, nenhuma molécula neutra estável envolvendo hélio ou néon ligado covalentemente era conhecida.
A extrapolação de tendências periódicas prediz que o oganesson deve ser o mais reativo dos gases nobres; tratamentos teóricos mais sofisticados indicam maior reatividade do que sugerem tais extrapolações, a ponto de questionar a aplicabilidade do descritor "gás nobre". Espera-se que o Oganesson seja parecido com o silício ou o estanho no grupo 14: um elemento reativo com um +4 comum e um estado menos comum +2, que em temperatura e pressão ambiente não é um gás, mas sim um semicondutor sólido. Testes empíricos / experimentais serão necessários para validar essas previsões.
Os gases nobres - incluindo o hélio - podem formar íons moleculares estáveis na fase gasosa. O mais simples é o íon molecular hidreto de hélio , HeH + , descoberto em 1925. Por ser composto dos dois elementos mais abundantes no universo, hidrogênio e hélio, acredita-se que ocorra naturalmente no meio interestelar , embora não tenha sido detectado ainda. Além desses íons, existem muitos excímeros neutros conhecidos dos gases nobres. Estes são compostos como ArF e KrF que são estáveis apenas quando em um estado eletrônico excitado ; alguns deles encontram aplicação em lasers de excimer .
Além dos compostos em que um átomo de gás nobre está envolvido em uma ligação covalente , os gases nobres também formam compostos não covalentes . Os clatratos , descritos pela primeira vez em 1949, consistem em um átomo de gás nobre aprisionado em cavidades de estruturas cristalinas de certas substâncias orgânicas e inorgânicas. A condição essencial para sua formação é que os átomos convidados (gás nobre) devem ser de tamanho apropriado para caber nas cavidades da estrutura do cristal hospedeiro. Por exemplo, o argônio, o criptônio e o xenônio formam clatratos com a hidroquinona , mas o hélio e o néon não porque são muito pequenos ou insuficientemente polarizáveis para serem retidos. Néon, argônio, criptônio e xenônio também formam clatratos hidratados, onde o gás nobre fica preso no gelo.
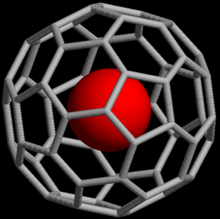
Os gases nobres podem formar compostos de fulereno endoédrico , nos quais o átomo do gás nobre fica preso dentro de uma molécula de fulereno . Em 1993, foi descoberto que quando C
60, uma molécula esférica que consiste em 60 átomos de carbono, é exposta a gases nobres em alta pressão, complexos como He @ C
60pode ser formado (a notação @ indica que ele está contido dentro de C
60mas não covalentemente ligado a ele). A partir de 2008, complexos endoédricos com hélio, néon, argônio, criptônio e xenônio foram criados. Esses compostos têm encontrado uso no estudo da estrutura e reatividade dos fulerenos por meio da ressonância magnética nuclear do átomo de gás nobre.
Compostos de gases nobres, como difluoreto de xenônio ( XeF
2) são considerados hipervalentes porque violam a regra do octeto . A ligação em tais compostos pode ser explicada usando um modelo de ligação de três centros e quatro elétrons . Este modelo, proposto pela primeira vez em 1951, considera a ligação de três átomos colineares. Por exemplo, ligação em XeF
2é descrito por um conjunto de três orbitais moleculares (MOs) derivados dos orbitais p em cada átomo. A ligação resulta da combinação de um orbital p preenchido de Xe com um orbital p preenchido pela metade de cada átomo F , resultando em um orbital de ligação preenchido, um orbital de ligação não preenchido e um orbital anti -ligação vazio . O orbital molecular mais ocupado está localizado nos dois átomos terminais. Isso representa uma localização de carga que é facilitada pela alta eletronegatividade do flúor.
A química dos gases nobres mais pesados, criptônio e xenônio, está bem estabelecida. A química dos mais leves, argônio e hélio, ainda está em um estágio inicial, enquanto um composto de néon ainda não foi identificado.
Ocorrência e produção
A abundância de gases nobres no universo diminui à medida que seu número atômico aumenta. O hélio é o elemento mais comum no universo depois do hidrogênio, com uma fração de massa de cerca de 24%. A maior parte do hélio no universo foi formado durante a nucleossíntese do Big Bang , mas a quantidade de hélio está aumentando continuamente devido à fusão do hidrogênio na nucleossíntese estelar (e, em um grau muito leve, a decadência alfa de elementos pesados). As abundâncias na Terra seguem tendências diferentes; por exemplo, o hélio é apenas o terceiro gás nobre mais abundante na atmosfera. A razão é que não há hélio primordial na atmosfera; devido à pequena massa do átomo, o hélio não pode ser retido pelo campo gravitacional da Terra . O hélio na Terra vem da decomposição alfa de elementos pesados, como urânio e tório, encontrados na crosta terrestre e tende a se acumular em depósitos de gás natural . A abundância de argônio, por outro lado, é aumentada como resultado do decaimento beta do potássio-40 , também encontrado na crosta terrestre, para formar argônio-40 , que é o isótopo de argônio mais abundante na Terra apesar de ser relativamente raro no Sistema Solar . Este processo é a base para o método de datação de potássio-argônio . O xenônio tem uma abundância inesperadamente baixa na atmosfera, no que foi chamado de problema do xenônio ausente ; uma teoria é que o xenônio ausente pode estar preso em minerais dentro da crosta terrestre. Após a descoberta do dióxido de xenônio , a pesquisa mostrou que o Xe pode substituir o Si no quartzo . O radônio é formado na litosfera pela decadência alfa do rádio. Ele pode penetrar em edifícios por meio de rachaduras em suas fundações e se acumular em áreas que não são bem ventiladas. Devido à sua alta radioatividade, o radônio apresenta um risco significativo para a saúde; está implicado em cerca de 21.000 mortes por câncer de pulmão por ano apenas nos Estados Unidos. Oganesson não ocorre na natureza e, em vez disso, é criado manualmente por cientistas.
| Abundância | Hélio | Néon | Argônio | Krypton | Xenon | Radon |
|---|---|---|---|---|---|---|
| Sistema Solar (para cada átomo de silício) | 2343 | 2,148 | 0,1025 | 5,515 × 10 −5 | 5,391 × 10 −6 | - |
| Atmosfera da Terra (fração de volume em ppm ) | 5,20 | 18,20 | 9.340,00 | 1,10 | 0,09 | (0,06–18) × 10 −19 |
| Rocha ígnea (fração de massa em ppm) | 3 × 10 −3 | 7 × 10 −5 | 4 × 10 −2 | - | - | 1,7 × 10 −10 |
| Gás | Preço de 2004 ( USD / m 3 ) |
|---|---|
| Hélio (grau industrial) | 4,20-4,90 |
| Hélio (grau de laboratório) | 22,30-44,90 |
| Argônio | 2,70-8,50 |
| Néon | 60-120 |
| Krypton | 400-500 |
| Xenon | 4000-5000 |
Para uso em larga escala, o hélio é extraído por destilação fracionada do gás natural, que pode conter até 7% de hélio.
Néon, argônio, criptônio e xenônio são obtidos do ar usando métodos de liquefação de gases , para converter elementos em um estado líquido, e destilação fracionada , para separar misturas em partes componentes. O hélio é normalmente produzido pela separação do gás natural e o radônio é isolado da decomposição radioativa dos compostos de rádio. Os preços dos gases nobres são influenciados por sua abundância natural, sendo o argônio o mais barato e o xenônio o mais caro. Como exemplo, a tabela ao lado lista os preços de 2004 nos Estados Unidos para quantidades de laboratório de cada gás.
Formulários
Os gases nobres têm pontos de ebulição e fusão muito baixos, o que os torna úteis como refrigerantes criogênicos . Em particular, o hélio líquido , que ferve a 4,2 K (−268,95 ° C; −452,11 ° F), é usado para ímãs supercondutores , como os necessários em imagens de ressonância magnética nuclear e ressonância magnética nuclear . O néon líquido, embora não atinja temperaturas tão baixas quanto o hélio líquido, também é usado na criogenia porque tem mais de 40 vezes mais capacidade de refrigeração do que o hélio líquido e três vezes mais do que o hidrogênio líquido.
O hélio é utilizado como componente dos gases respiratórios em substituição ao nitrogênio, devido à sua baixa solubilidade em fluidos, principalmente em lipídios . Os gases são absorvidos pelo sangue e pelos tecidos do corpo quando sob pressão, como no mergulho autônomo , o que causa um efeito anestésico conhecido como narcose por nitrogênio . Devido à sua reduzida solubilidade, pouco hélio é levado para as membranas celulares , e quando o hélio é usado para substituir parte das misturas respiratórias, como no trimix ou heliox , ocorre uma diminuição no efeito narcótico do gás em profundidade. A solubilidade reduzida do hélio oferece outras vantagens para a condição conhecida como doença descompressiva ou as curvas . A quantidade reduzida de gás dissolvido no corpo significa que menos bolhas de gás se formam durante a diminuição da pressão da subida. Outro gás nobre, o argônio, é considerado a melhor opção para uso como gás de insuflação de roupa seca para mergulho. O hélio também é usado como gás de enchimento em barras de combustível nuclear para reatores nucleares.
Desde o desastre de Hindenburg em 1937, o hélio substituiu o hidrogênio como gás de elevação em dirigíveis e balões devido à sua leveza e incombustibilidade, apesar de uma redução de 8,6% na flutuabilidade.
Em muitas aplicações, os gases nobres são usados para fornecer uma atmosfera inerte. O argônio é usado na síntese de compostos sensíveis ao ar que são sensíveis ao nitrogênio. O argônio sólido também é usado para o estudo de compostos muito instáveis, como intermediários reativos , aprisionando-os em uma matriz inerte em temperaturas muito baixas. O hélio é usado como meio de transporte na cromatografia gasosa , como gás de enchimento para termômetros e em dispositivos de medição de radiação, como o contador Geiger e a câmara de bolhas . O hélio e o argônio são comumente usados para proteger os arcos de soldagem e o metal de base circundante da atmosfera durante a soldagem e o corte, bem como em outros processos metalúrgicos e na produção de silício para a indústria de semicondutores.
Gases nobres são comumente usados em iluminação por causa de sua falta de reatividade química. Argônio, misturado com nitrogênio, é usado como gás de enchimento para lâmpadas incandescentes . O criptônio é usado em lâmpadas de alto desempenho, que possuem temperaturas de cor mais altas e maior eficiência, pois reduz a taxa de evaporação do filamento mais do que o argônio; lâmpadas halógenas , em particular, usam criptônio misturado com pequenas quantidades de compostos de iodo ou bromo . Os gases nobres brilham em cores distintas quando usados dentro de lâmpadas de descarga de gás , como as " luzes de néon ". Essas luzes recebem o nome de néon, mas geralmente contêm outros gases e fósforos , que adicionam vários matizes à cor laranja-avermelhada do néon. O xenônio é comumente usado em lâmpadas de arco de xenônio , que, devido ao seu espectro quase contínuo que se assemelha à luz do dia, encontram aplicação em projetores de filme e como faróis de automóveis.
Os gases nobres são usados em lasers de excímeros , que são baseados em moléculas eletronicamente excitadas de vida curta, conhecidas como excímeros . Os excímeros usados para lasers podem ser dímeros de gases nobres, como Ar 2 , Kr 2 ou Xe 2 , ou mais comumente, o gás nobre é combinado com um halogênio em excímeros, como ArF, KrF, XeF ou XeCl. Esses lasers produzem luz ultravioleta que, devido ao seu comprimento de onda curto (193 nm para ArF e 248 nm para KrF), permite imagens de alta precisão. Os lasers Excimer têm muitas aplicações industriais, médicas e científicas. Eles são usados para microlitografia e microfabricação , que são essenciais para a fabricação de circuitos integrados , e para cirurgia a laser , incluindo angioplastia a laser e cirurgia ocular .
Alguns gases nobres têm aplicação direta na medicina. O hélio às vezes é usado para melhorar a respiração de quem sofre de asma . O xenônio é usado como anestésico devido à sua alta solubilidade em lipídios, o que o torna mais potente do que o óxido nitroso normal , e porque é facilmente eliminado do corpo, resultando em uma recuperação mais rápida. O Xenon encontra aplicação em imagens médicas dos pulmões por meio da ressonância magnética hiperpolarizada. O radônio, que é altamente radioativo e só está disponível em quantidades mínimas, é usado na radioterapia .
Gases nobres, particularmente xenônio, são usados predominantemente em motores de íons devido à sua inércia. Como os motores iônicos não são movidos por reações químicas, os combustíveis quimicamente inertes são desejados para evitar reações indesejadas entre o combustível e qualquer outra coisa no motor.
O Oganesson é muito instável para trabalhar e não tem nenhuma aplicação conhecida além da pesquisa.
Cor de descarga

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
|
|
|
|
|
|
| Hélio | Néon | Argônio | Krypton | Xenon |
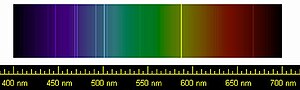
A cor da emissão de descarga de gás depende de vários fatores, incluindo o seguinte:
- parâmetros de descarga (valor local de densidade de corrente e campo elétrico , temperatura, etc. - observe a variação de cor ao longo da descarga na linha superior);
- pureza do gás (mesmo uma pequena fração de certos gases pode afetar a cor);
- material do envelope do tubo de descarga - observe a supressão dos componentes UV e azul nos tubos da linha inferior feitos de vidro doméstico grosso.
Veja também
- Gás nobre (página de dados) , para tabelas estendidas de propriedades físicas.
- Metal nobre , para metais resistentes à corrosão ou oxidação.
- Gás inerte , para qualquer gás que não seja reativo em circunstâncias normais.
- Gás industrial
- Neutrônio
- Regra do octeto
Notas
Referências
|
Recursos de biblioteca sobre gás nobre |
- Bennett, Peter B .; Elliott, David H. (1998). A Fisiologia e a Medicina do Mergulho . Publicação SPCK . ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services (5 de dezembro de 2007). CliffsAP Chemistry . CliffsNotes . ISBN 978-0-470-13500-6.
- Greenwood, NN; Earnshaw, A. (1997). Química dos Elementos (2ª ed.). Oxford: Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Harding, Charlie J .; Janes, Rob (2002). Elementos da P bloco . Royal Society of Chemistry . ISBN 0-85404-690-9.
- Holloway, John H. (1968). Noble-Gas Chemistry . Londres : Methuen Publishing . ISBN 0-412-21100-9.
- Mendeleev, D. (1902–1903). Osnovy Khimii (The Principles of Chemistry) (em russo) (7ª ed.).
- Ozima, Minoru; Podosek, Frank A. (2002). Noble Gas Geochemistry . Cambridge University Press . ISBN 0-521-80366-7.
- Weinhold, F .; Landis, C. (2005). Valência e união . Cambridge University Press . ISBN 0-521-83128-8.