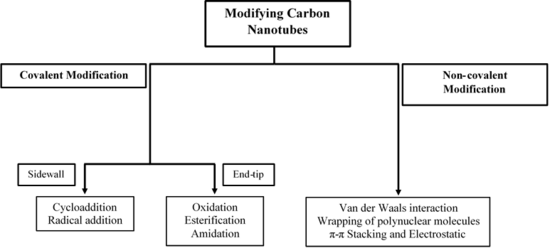
Química do nanotubo de carbono - Carbon nanotube chemistry
A química dos nanotubos de carbono envolve reações químicas , que são usadas para modificar as propriedades dos nanotubos de carbono (CNTs). Os CNTs podem ser funcionalizados para obter as propriedades desejadas que podem ser usadas em uma ampla variedade de aplicações. Os dois métodos principais de funcionalização do CNT são modificações covalentes e não covalentes.
Devido à sua natureza hidrofóbica, os CNTs tendem a se aglomerar dificultando sua dispersão em solventes ou poliméricos viscosos. Os feixes de nanotubos ou agregados resultantes reduzem o desempenho mecânico do composto final. A superfície dos CNTs pode ser modificada para reduzir a hidrofobicidade e melhorar a adesão interfacial a um polímero em massa por meio de fixação química.
| Parte de uma série de artigos sobre |
| Nanomateriais |
|---|
 |
| Nanotubos de carbono |
| Fulerenos |
| Outras nanopartículas |
| Materiais nanoestruturados |
Modificação covalente
A modificação covalente anexa um grupo funcional ao nanotubo de carbono. Os grupos funcionais podem ser fixados na parede lateral ou nas extremidades do nanotubo de carbono. As extremidades dos nanotubos de carbono têm a maior reatividade devido ao seu maior ângulo de pirimidização e as paredes dos nanotubos de carbono têm ângulos de pirimidização mais baixos, que apresentam menor reatividade. Embora as modificações covalentes sejam muito estáveis, o processo de ligação interrompe a hibridização sp 2 dos átomos de carbono porque uma ligação σ é formada. A interrupção da hibridização sp 2 estendida normalmente diminui a condutância dos nanotubos de carbono.
Oxidação
A purificação e oxidação de nanotubos de carbono (CNTs) tem sido bem representada na literatura. Esses processos foram essenciais para a produção de nanotubos de carbono de baixo rendimento, onde as partículas de carbono, as partículas de carbono amorfo e os revestimentos representavam uma porcentagem significativa do material total e ainda são importantes para a introdução de grupos funcionais de superfície. Durante a oxidação ácida, a rede ligada carbono-carbono das camadas grafíticas é quebrada, permitindo a introdução de unidades de oxigênio na forma de grupos carboxila , fenólicos e lactona , que foram amplamente explorados para posterior funcionalização química.
Os primeiros estudos sobre oxidação de nanotubos de carbono envolveram reações em fase gasosa com vapor de ácido nítrico no ar, que funcionalizou indiscriminadamente os nanotubos de carbono com grupos carboxílicos, carbonila ou hidroxila . Nas reações de fase líquida, os nanotubos de carbono foram tratados com soluções oxidantes de ácido nítrico ou uma combinação de ácido nítrico e sulfúrico para o mesmo efeito. No entanto, a superoxidação pode ocorrer fazendo com que o nanotubo de carbono se quebre em fragmentos, que são conhecidos como fragmentos carbonáceos. Xing et al. revelou oxidação assistida por sonicação, com ácido nítrico e sulfúrico, de nanotubos de carbono e grupos carbonila e carboxila produzidos. Após a reação de oxidação em solução ácida, o tratamento com peróxido de hidrogênio limitou os danos na rede de nanotubos de carbono. Nanotubos de carbono de parede única podem ser encurtados de maneira escalonável usando oleum (100% H 2 SO 4 com 3% SO 3 ) e ácido nítrico. O ácido nítrico corta os nanotubos de carbono enquanto o oleum cria um canal.
Em um tipo de modificação química, a anilina é oxidada a um intermediário de diazônio . Após a expulsão do nitrogênio, ele forma uma ligação covalente como um radical aril :
Esterificação / Amidação
Grupos carboxílicos são usados como precursores para a maioria das reações de esterificação e amidação . O grupo carboxílico é convertido em um cloreto de acila com o uso de cloreto de tionila ou oxalila que é então feito reagir com a amida, amina ou álcool desejado. Nanotubos de carbono foram depositados com nanopartículas de prata com o auxílio de reações de aminação. Foi demonstrado que os nanotubos de carbono funcionalizados com amida quelam as nanopartículas de prata. Nanotubos de carbono modificados com cloreto de acila reagem prontamente com moléculas altamente ramificadas, como a poli (amidoamina) , que atua como um molde para o íon prata e, posteriormente, sendo reduzido pelo formaldeído . Nanotubos de carbono modificados com amino podem ser preparados pela reação de etilenodiamina com nanotubos de carbono funcionalizados com cloreto de acila.
Reações de halogenação
Os nanotubos de carbono podem ser tratados com ácido peroxitrifluroacético para dar principalmente ácido carboxílico e grupos funcionais trifluoroacéticos. Os nanotubos de carbono fluorados, por substituição, podem ser posteriormente funcionalizados com uréia , guanidina , tioureia e aminossilano . Usando a reação de Hunsdiecker, os nanotubos de carbono tratados com ácido nítrico podem reagir com o iodosobenzenediacetato para iodar os nanotubos de carbono.
Cycloaddition
Também são conhecidos protocolos para cicloadições , como reações de Diels-Alder , cicloadições 1,3-dipolares de iletos de azometina e reações de cicloadição azida-alquino. Um exemplo é uma reação DA assistida por hexacarbonil de cromo e alta pressão. A razão I D / I G para a reação com dieno de Danishefsky é 2,6.
A reação de cicloadição 1,3 mais conhecida envolve iletos de azometina reagindo com nanotubos de carbono, que são de grande interesse. A adição de um anel de pirrolidina pode levar a uma variedade de grupos funcionais, tais como dendrímeros de poli (amidoamina) de segunda geração , adendos de ftalocianina, grupos perfluoroalquilsilano e grupos amino etilenoglicol. A reação de cicloadição de Diels pode ocorrer, especialmente em nanotubos de carbono fluorados. Eles são conhecidos por sofrer reações de Diels-Alder com dienos, como 2,3-dimetil-1,3- butadieno , antraceno e 2-trimetilsiloxil-1,3-butadieno.
Adição radical

A modificação de nanotubos de carbono com sais de aril diazônio foi estudada primeiro por Tour et al. Devido às condições adversas necessárias para o composto de diazônio gerado in situ , outros métodos foram explorados. Stephenson et al. relataram o uso de derivados de anilina com nitrito de sódio em ácido sulfúrico 96% e persulfato de amônio . Price et al. demonstraram que agitar nanotubos de carbono em água e tratar com anilinas e agentes oxidantes provou ser uma reação mais branda. A química do diazônio funcionalizou os nanotubos de carbono que foram usados como um precursor para modificações posteriores. As reações de acoplamento de Suzuki e Heck foram realizadas em nanotubos de carbono funcionalizados com iodofenil . Wong et al. demonstraram reações fotoquímicas leves para sililar os nanotubos de carbono com trimetoxissilano e hexafenildisilano .
Adição nucleofílica
Hirsch et al. conduziu adições nucleofílicas com compostos de organolítio e organomagnésio em nanotubos de carbono. Com mais oxidação no ar, eles foram capazes de criar nanotubos de carbono modificados com alquil. Hirsch também foi capaz de mostrar a adição nucleofílica de aminas gerando amidas de lítio, levando a nanotubos de carbono modificados com amino.
Adição eletrofílica
Os nanotubos também podem ser alquilados com halogenetos de alquila usando lítio ou sódio metálico e amônia líquida ( condições de redução de Birch ). O sal de nanotubo inicial pode funcionar como um iniciador de polimerização e pode reagir com peróxidos para formar nanotubos funcionalizados com alcoxi
A modificação alquil e hidroxil de nanotubos de carbono foi demonstrada com a adição eletrofílica de alquilhalogenetos por irradiação de microondas. Tessonnier et al. nanotubos de carbono modificados com grupos amino por desprotonação com butil lítio e reagindo com substituição de amino. Balaban et al. aplicou a acilação de Friedel-Crafts a nanotubos de carbono com nitrobenzeno a 180 ° C junto com cloreto de alumínio.
Modificações não covalentes
As modificações não covalentes utilizam forças de van der Waals e interações π-π por adsorção de compostos aromáticos polinucleares, surfactantes , polímeros ou biomoléculas . As modificações não covalentes não perturbam a configuração natural dos nanotubos de carbono com o custo da estabilidade química, e estão sujeitas à separação de fases, dissociação entre duas fases, no estado sólido.
Compostos aromáticos polinucleares
Alguns compostos aromáticos polinucleares comuns que são funcionalizados com porções hidrofílicas ou hidrofóbicas são usados para solubilizar nanotubos de carbono em solventes orgânicos ou aquosos. Alguns desses anfifílicos são sistemas de fenil , naftaleno , fenantreno , pireno e porfirina . O maior empilhamento π-π de anfifílicos aromáticos, como anfifílicos pireno, teve a melhor solubilidade em comparação aos anfifílicos fenil com o pior empilhamento π-π, levando a mais solubilidade em água. Esses sistemas aromáticos podem ser modificados com grupos amino e ácido carboxílico antes de funcionalizar os nanotubos de carbono.
Biomoléculas
A interação entre nanotubos de carbono e biomoléculas tem sido amplamente estudada devido ao seu potencial para serem utilizados em aplicações biológicas. A modificação dos nanotubos de carbono com proteínas, carboidratos e ácidos nucléicos é construída com a técnica bottom-up. As proteínas possuem alta afinidade com os nanotubos de carbono devido à sua diversidade de aminoácidos serem hidrofóbicos ou hidrofílicos. Polissacarídeos têm sido usados com sucesso para modificar nanotubos de carbono formando híbridos estáveis. Para tornar os nanotubos de carbono solúveis em água, fosfolipídios como lisoglicerofosfolipídios têm sido usados. A cauda de fosfolipídio única envolve o nanotubo de carbono, mas os fosfolipídios de cauda dupla não tinham a mesma capacidade.
empilhamento π-π e interações eletrostáticas
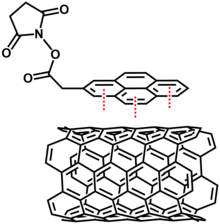
Moléculas que possuem bifuncionalidade são usadas para modificar o nanotubo de carbono. Uma das extremidades da molécula são compostos poliaromáticos que interagem com o nanotubo de carbono através do empilhamento π-π. A outra extremidade da mesma molécula possui um grupo funcional, como amino, carboxil ou tiol. Por exemplo, derivados de pireno e ariltióis foram usados como ligantes para várias nanopérolas de metal, como ouro, prata e platina.
Intertravamento mecânico
Um caso particular de modificação não covalente é a formação de derivados mecanicamente interligados do tipo rotaxano de nanotubos de parede única (SWNTs) . Nessa estratégia, os SWNTs são encapsulados por macrociclo (s) molecular (s), que são formados ao redor deles por macrociclização ou pré-formados e rosqueados em um estágio posterior. Em MINTs ( M echanically I nterlocked N ano T ubes), o SWNT e macrociclo orgânico são ligados por meio de sua topologia, através de uma ligação mecânica , combinando a estabilidade das estratégias covalentes - pelo menos uma ligação covalente deve ser quebrada para separar SWNT e macrociclo (s) - com a integridade estrutural das estratégias não covalentes clássicas - a rede C-sp 2 do SWNT permanece intacta.
Caracterização
Uma ferramenta útil para a análise de nanotubos derivatizados é a espectroscopia Raman, que mostra uma banda G (G para grafite ) para os nanotubos nativos em 1580 cm -1 e uma banda D (D para defeito) em 1350 cm -1 quando o grafite a rede é interrompida com a conversão de carbono hibridizado sp² em sp³ . A razão de ambos os picos I D / I G é tomada como uma medida de funcionalização. Outras ferramentas são a espectroscopia de UV, onde nanotubos primitivos mostram singularidades de Van Hove distintas, onde os tubos funcionalizados não, e a análise simples de TGA .
Veja também
Notas