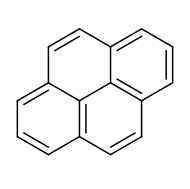
Pyrene - Pyrene
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Pyrene |
|
| Outros nomes
Benzo [ def ] fenantreno
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 1307225 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100,004,481 |
| 84203 | |
| KEGG | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 16 H 10 | |
| Massa molar | 202,256 g · mol −1 |
| Aparência | sólido incolor
(as impurezas amarelas são freqüentemente encontradas em níveis residuais em muitas amostras). |
| Densidade | 1.271 g / mL |
| Ponto de fusão | 145 a 148 ° C (293 a 298 ° F; 418 a 421 K) |
| Ponto de ebulição | 404 ° C (759 ° F; 677 K) |
| 0,146 mg / L | |
| -147,9 · 10 −6 cm 3 / mol | |
| Perigos | |
| Riscos principais | irritante |
| Frases R (desatualizado) | 36/37 / 38-45-53 |
| Frases S (desatualizado) | 24 / 25-26-36 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | não inflamável |
| Compostos relacionados | |
|
PAHs relacionados
|
benzopireno |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O pireno é um hidrocarboneto aromático policíclico (PAH) que consiste em quatro anéis de benzeno fundidos , resultando em um sistema aromático plano . A fórmula química é C
16H
10. Este sólido amarelo é o menor PAH perifundido (aquele em que os anéis são fundidos em mais de uma face). O pireno se forma durante a combustão incompleta de compostos orgânicos.
Ocorrência e propriedades
O pireno foi isolado pela primeira vez do alcatrão de carvão , onde ocorre até 2% em peso. Como um PAH perifundido, o pireno é muito mais estabilizado por ressonância do que seu anel de cinco membros contendo o isômero fluoranteno . Portanto, é produzido em uma ampla gama de condições de combustão. Por exemplo, automóveis produzem cerca de 1 μg / km.
Reações
A oxidação com cromato dá perinaftenona e depois ácido naftaleno-1,4,5,8-tetracarboxílico. O pireno sofre uma série de reações de hidrogenação e é suscetível à halogenação, adições de Diels-Alder e nitração, todas com vários graus de seletividade. A bromação ocorre em uma das 3 posições.
A redução com sódio fornece o ânion radical. A partir desse ânion, uma variedade de complexos pi-arenos pode ser preparada.
Fotofísica
O pireno e seus derivados são usados comercialmente para fazer corantes e precursores de corantes, por exemplo, piranina e ácido naftaleno-1,4,5,8-tetracarboxílico. Possui forte absorvância em UV-Vis em três bandas nítidas a 330 nm em DCM. A emissão está próxima da absorção, mas movendo-se a 375 nm. A morfologia dos sinais muda com o solvente. Seus derivados também são sondas moleculares valiosas via espectroscopia de fluorescência , com alto rendimento quântico e tempo de vida (0,65 e 410 nanossegundos, respectivamente, em etanol a 293 K). O pireno foi a primeira molécula para a qual o comportamento do excímero foi descoberto. Esse excímero aparece em torno de 450 nm. Theodor Förster relatou isso em 1954.
Formulários
O espectro de emissão de fluorescência do pireno é muito sensível à polaridade do solvente, então o pireno tem sido usado como uma sonda para determinar ambientes de solvente. Isso se deve ao fato de seu estado excitado ter uma estrutura não plana diferente do estado fundamental. Certas bandas de emissão não são afetadas, mas outras variam em intensidade devido à força de interação com um solvente.

Embora não seja tão problemático quanto o benzopireno , estudos em animais mostraram que o pireno é tóxico para os rins e o fígado . Sabe-se agora que o pireno afeta várias funções vivas em peixes e algas.
Experimentos em porcos mostram que o 1-hidroxipireno urinário é um metabólito do pireno, quando administrado por via oral.
Os pirenos são fortes materiais doadores de elétrons e podem ser combinados com diversos materiais para fazer sistemas doadores-aceitadores de elétrons que podem ser usados em aplicações de conversão de energia e coleta de luz.
Veja também
Referências
- ^ União internacional da química pura e aplicada (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 . The Royal Society of Chemistry . p. 206. doi : 10.1039 / 9781849733069 . ISBN 978-0-85404-182-4.
- ^ a b Senkan, Selim e Castaldi, Marco (2003) "Combustion" na Enciclopédia de Química Industrial de Ullmann , Wiley-VCH, Weinheim.
- ^ Gumprecht, WH (1968). "3-bromopireno". Org. Synth . 48 : 30. doi : 10.15227 / orgsyn.048.0030 .
- ^ Kucera, Benjamin E .; Jilek, Robert E .; Brennessel, William W .; Ellis, John E. (2014). "Complexos de bis (pireno) de metal de vanádio, nióbio e titânio: complexos de pireno homolépticos isoláveis de metais de transição". Acta Crystallographica Seção C Química Estrutural . 70 (8): 749–753. doi : 10.1107 / S2053229614015290 . PMID 25093352 .
- ^ a b Tagmatarchis, Nikos; Ewels, Christopher P .; Bittencourt, Carla; Arenal, Raul; Pelaez-Fernandez, Mario; Sayed-Ahmad-Baraza, Yuman; Cantão-Vitória, Ruben (05-06-2017). "Funcionalização de MoS 2 com 1,2-ditiolanos: para nanohíbridos doador-aceitadores para conversão de energia" . Materiais e aplicações NPJ 2D . 1 (1): 13. doi : 10.1038 / s41699-017-0012-8 . ISSN 2397-7132 .
- ^ Van Dyke, David A .; Pryor, Brian A .; Smith, Philip G .; Topp, Michael R. (maio de 1998). "Espectroscopia de fluorescência resolvida no tempo de nanossegundos no laboratório de físico-química: Formação do excímero de pireno em solução". Journal of Chemical Education . 75 (5): 615. doi : 10.1021 / ed075p615 .
- ^ Förster, Th .; Kasper, K. (junho de 1954). "Ein Konzentrationsumschlag der Fluoreszenz". Zeitschrift für Physikalische Chemie . 1 (5_6): 275–277. doi : 10.1524 / zpch.1954.1.5_6.275 .
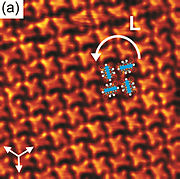
- ^ Pham, Tuan Anh; Song, Fei; Nguyen, Manh-Thuong; Stöhr, Meike (2014). "Auto-montagem de derivados de pireno em Au (111): efeitos substituintes em interações intermoleculares" . Chem. Comun . 50 (91): 14089–92. doi : 10.1039 / C4CC02753A . PMID 24905327 .
- ^ Oliveira, M .; Ribeiro, A .; Hylland, K .; Guilhermino, L. (2013). "Efeitos únicos e combinados de microplásticos e pireno em juvenis (grupo 0+) do góbio comum Pomatoschistus microps (Teleostei, Gobiidae)". Indicadores Ecológicos . 34 : 641–647. doi : 10.1016 / j.ecolind.2013.06.019 .
- ^ Oliveira, M .; Gravato, C .; Guilhermino, L. (2012). "Efeitos tóxicos agudos do pireno em Pomatoschistus microps (Teleostei, Gobiidae): Mortalidade, biomarcadores e desempenho de natação". Indicadores Ecológicos . 19 : 206–214. doi : 10.1016 / j.ecolind.2011.08.006 .
- ^ Oliveira, M .; Ribeiro, A .; Guilhermino, L. (2012). "Efeitos da exposição a microplásticos e PAHs em microalgas Rhodomonas baltica e Tetraselmis chuii". Bioquímica e Fisiologia Comparada Parte A: Fisiologia Molecular e Integrativa . 163 : S19 – S20. doi : 10.1016 / j.cbpa.2012.05.062 .
- ^ Oliveira, M .; Ribeiro, A .; Guilhermino, L. (2012). "Efeitos da exposição de curto prazo a microplásticos e pireno em Pomatoschistus microps (Teleostei, Gobiidae)". Bioquímica e Fisiologia Comparada Parte A: Fisiologia Molecular e Integrativa . 163 : S20. doi : 10.1016 / j.cbpa.2012.05.063 .
- ^ Keimig, SD; Kirby, KW; Morgan, DP; Keizer, JE; Hubert, TD (1983). "Identificação de 1-hidroxipireno como um dos principais metabólitos do pireno na urina de porco". Xenobiotica . 13 (7): 415–20. doi : 10.3109 / 00498258309052279 . PMID 6659544 .
Leitura adicional
- Birks, JB (1969). Photophysics of Aromatic Molecules . Londres: Wiley.
- Valeur, B. (2002). Fluorescência molecular: princípios e aplicações . Nova York: Wiley-VCH.
- Birks, JB (1975). "Excimers". Relatórios de progresso em física . 38 (8): 903–974. doi : 10.1088 / 0034-4885 / 38/8/001 . ISSN 0034-4885 .
- Fetzer, JC (2000). A química e a análise dos grandes hidrocarbonetos aromáticos policíclicos . Nova York: Wiley.