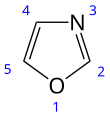
Oxazol - Oxazole
|
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
1,3-oxazol |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100,005,474 |
||
| Número EC | |||
| Malha | D010080 | ||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 3 H 3 N O | |||
| Massa molar | 69,06 g / mol | ||
| Densidade | 1.050 g / cm 3 | ||
| Ponto de ebulição | 69 a 70 ° C (156 a 158 ° F; 342 a 343 K) | ||
| Acidez (p K a ) | 0,8 (de ácido conjugado) | ||
| Página de dados suplementares | |||
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|||
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
||
| UV , IR , NMR , MS | |||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O oxazol é o composto original de uma vasta classe de compostos orgânicos aromáticos heterocíclicos . Estes são azóis com um oxigênio e um nitrogênio separados por um carbono. Os oxazóis são compostos aromáticos, mas menos do que os tiazóis. O oxazol é uma base fraca; seu ácido conjugado tem um p K a de 0,8, em comparação com 7 para o imidazol .
Preparação
Os métodos clássicos de síntese de oxazol em química orgânica são
- a síntese Robinson-Gabriel por desidratação de 2-acilaminocetonas
- a síntese de oxazol de Fischer a partir de cianoidrinas e aldeídos
- a reação de Bredereck com α- halocetonas e formamida
- a reação de Van Leusen com aldeídos e TosMIC
Outros métodos:
- Oxazolinas podem também ser obtidos a partir de certas cycloisomerization propargilo amidas . Em um estudo, os oxazóis foram preparados por meio de uma síntese em um único recipiente que consiste na condensação de propargilamina e cloreto de benzoíla na amida , seguido por um acoplamento Sonogashira da extremidade alcina terminal com outro equivalente de cloreto de benzoíla, e concluindo com ácido p- toluenossulfônico catalisado cicloisomerização :
- Em uma síntese de oxazol relatada, os reagentes são um cloreto de benzoil nitro- substituído e um isonitrila :
Biossíntese
Em biomoléculas , os oxazóis resultam da ciclização e oxidação de peptídeos não ribossômicos de serina ou treonina :
Oxazoles não são tão abundantes em biomoléculas como os relacionados tiazoles com oxigénio substituído por um átomo de enxofre.
Reações
Com um pK a de 0,8 para o ácido conjugado, os oxazoles são muito menos básicos do que os imidazoles (pK a = 7).
- A desprotonação de oxazóis em C2 é freqüentemente acompanhada pela abertura do anel para o isonitrila.
- A substituição eletrofílica aromática ocorre em C5, exigindo grupos de ativação .
- A substituição nucleofílica aromática ocorre com grupos de saída em C2.
- As reações de Diels-Alder com dienos de oxazol podem ser seguidas por perda de oxigênio para formar piridinas .
- O rearranjo Cornforth de 4-aciloxazoles é uma reação de rearranjo térmico com o resíduo acil orgânico e o substituinte C5 mudando de posição.
- Várias reações de oxidação . Um estudo relata a oxidação de 4,5-difeniloxazol com 3 equivalentes de CAN na imida correspondente e ácido benzóico :
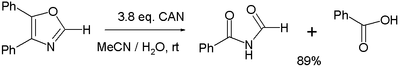
- Na meia-reação balanceada são consumidos três equivalentes de água para cada equivalente de oxazolina, gerando 4 prótons e 4 elétrons (este último derivado do Ce IV ).
Veja também
- Isoxazol , um análogo do átomo de nitrogênio na posição 2.
- Imidazol , um análogo do oxigênio substituído por um nitrogênio.
- Tiazol , um análogo do oxigênio substituído por um enxofre.
- Benzoxazol , onde o oxazol se funde a outro anel aromático.
- Pirrol , um análogo sem o átomo de oxigênio.
- Furano , um análogo sem o átomo de nitrogênio.
- Oxazolina , que tem uma ligação dupla reduzida.
- Oxazolidina , que tem ambas as ligações duplas reduzidas.
- Oxadiazóis com dois nitrogênios em vez de um (por exemplo, furazan ).
- Oxazolona , um análogo com um grupo carbonil