Lista de estados de oxidação dos elementos - List of oxidation states of the elements
Esta é uma lista de estados de oxidação conhecidos dos elementos químicos dentro de compostos químicos , excluindo valores não integrais . Os estados mais comuns aparecem em negrito. A tabela é baseada na de Greenwood e Earnshaw, com acréscimos observados. Todo elemento existe no estado de oxidação 0 quando é o elemento não ionizado puro em qualquer fase, seja alótropo monatômico ou poliatômico . A coluna para o estado de oxidação 0 mostra apenas elementos conhecidos por existir no estado de oxidação 0 em compostos . O formato da tabela, desenvolvido por Dmitri Mendeleev em 1889, mostra a periodicidade dos estados de oxidação dos elementos.
Lista
|
Estados de oxidação dos elementos
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Elemento | Estados de
oxidação negativos |
Estados de
oxidação positivos |
Grupo | Notas | |||||||||||||||
| -5 | -4 | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | +9 | |||||
| Z | |||||||||||||||||||
| 1 1 | hidrogênio | H | −1 | +1 | 1 1 | ||||||||||||||
| 2 | hélio | Ele | 18 | ||||||||||||||||
| 3 | lítio | Li | +1 | 1 1 | |||||||||||||||
| 4 | berílio | Estar | 0 0 | +1 | +2 | 2 | |||||||||||||
| 5 | boro | B | -5 | −1 | 0 0 | +1 | +2 | +3 | 13 | ||||||||||
| 6 | carbono | C | -4 | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 14 | |||||||
| 7 | azoto | N | -3 | -2 | −1 | +1 | +2 | +3 | +4 | +5 | 15 | ||||||||
| 8 | oxigênio | O | -2 | −1 | 0 0 | +1 | +2 | 16 | |||||||||||
| 9 | flúor | F | −1 | 17 | |||||||||||||||
| 10 | néon | Ne | 18 | ||||||||||||||||
| 11 | sódio | N / D | −1 | +1 | 1 1 | ||||||||||||||
| 12 | magnésio | Mg | +1 | +2 | 2 | ||||||||||||||
| 13 | alumínio | Al | -2 | −1 | +1 | +2 | +3 | 13 | |||||||||||
| 14 | silício | Si | -4 | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 14 | |||||||
| 15 | fósforo | P | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | 15 | |||||||
| 16 | enxofre | S | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 16 | |||||||
| 17 | cloro | Cl | −1 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | 17 | ||||||||
| 18 | argônio | Ar | 18 | ||||||||||||||||
| 19 | potássio | K | −1 | +1 | 1 1 | ||||||||||||||
| 20 | cálcio | Ca | +1 | +2 | 2 | ||||||||||||||
| 21 | escândio | Sc | 0 0 | +1 | +2 | +3 | 3 | ||||||||||||
| 22 | titânio | Ti | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 4 | |||||||||
| 23 | vanádio | V | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | 5 | ||||||||
| 24 | crómio | Cr | -4 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 6 | ||||||
| 25 | manganês | Mn | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | 7 | |||||
| 26 | ferro | Fe | -4 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | 8 | |||||
| 27 | cobalto | Co | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | 9 | ||||||||
| 28. | níquel | Ni | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 10 | |||||||||
| 29 | cobre | Cu | -2 | 0 0 | +1 | +2 | +3 | +4 | 11 | ||||||||||
| 30 | zinco | Zn | -2 | +1 | +2 | 12 | |||||||||||||
| 31 | gálio | Ga | -5 | -4 | -3 | -2 | −1 | +1 | +2 | +3 | 13 | ||||||||
| 32. | germânio | Ge | -4 | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 14 | |||||||
| 33 | arsênico | Como | -3 | -2 | −1 | +1 | +2 | +3 | +4 | +5 | 15 | ||||||||
| 34 | selênio | Se | -2 | −1 | +1 | +2 | +3 | +4 | +5 | +6 | 16 | ||||||||
| 35 | bromo | Br | −1 | +1 | +3 | +4 | +5 | +7 | 17 | ||||||||||
| 36. | krypton | Kr | +2 | 18 | |||||||||||||||
| 37. | rubídio | Rb | −1 | +1 | 1 1 | ||||||||||||||
| 38. | estrôncio | Sr | +1 | +2 | 2 | ||||||||||||||
| 39. | ítrio | Y | 0 0 | +1 | +2 | +3 | 3 | ||||||||||||
| 40. | zircônio | Zr | -2 | +1 | +2 | +3 | +4 | 4 | |||||||||||
| 41. | nióbio | Nb | -3 | −1 | +1 | +2 | +3 | +4 | +5 | 5 | |||||||||
| 42. | molibdênio | Mo | -4 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 6 | ||||||
| 43 | tecnécio | Tc | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | 7 | ||||||
| 44 | rutênio | Ru | -4 | -2 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | 8 | |||||
| 45 | ródio | Rh | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 9 | |||||||
| 46. | paládio | Pd | 0 0 | +1 | +2 | +3 | +4 | 10 | |||||||||||
| 47 | prata | Ag | -2 | −1 | +1 | +2 | +3 | 11 | |||||||||||
| 48. | cádmio | CD | -2 | +1 | +2 | 12 | |||||||||||||
| 49. | índio | No | -5 | -2 | −1 | +1 | +2 | +3 | 13 | ||||||||||
| 50. | lata | Sn | -4 | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | 14 | |||||||
| 51 | antimônio | Sb | -3 | -2 | −1 | +1 | +2 | +3 | +4 | +5 | 15 | ||||||||
| 52 | telúrio | Te | -2 | −1 | +1 | +2 | +3 | +4 | +5 | +6 | 16 | ||||||||
| 53 | iodo | Eu | −1 | +1 | +3 | +4 | +5 | +6 | +7 | 17 | |||||||||
| 54 | xenon | Xe | +2 | +4 | +6 | +8 | 18 | ||||||||||||
| 55 | césio | Cs | −1 | +1 | 1 1 | ||||||||||||||
| 56. | bário | BA | +1 | +2 | 2 | ||||||||||||||
| 57 | lantânio | La | 0 0 | +1 | +2 | +3 | 3 | ||||||||||||
| 58 | cério | Ce | +2 | +3 | +4 | n / D | |||||||||||||
| 59. | praseodímio | Pr | 0 0 | +1 | +2 | +3 | +4 | +5 | n / D | ||||||||||
| 60 | neodímio | Nd | 0 0 | +2 | +3 | +4 | n / D | ||||||||||||
| 61 | promécio | PM | +2 | +3 | n / D | ||||||||||||||
| 62 | samário | Sm | 0 0 | +2 | +3 | n / D | |||||||||||||
| 63. | európio | Eu | +2 | +3 | n / D | ||||||||||||||
| 64 | gadolínio | Gd | 0 0 | +1 | +2 | +3 | n / D | ||||||||||||
| 65 | térbio | Tb | 0 0 | +1 | +2 | +3 | +4 | n / D | |||||||||||
| 66. | disprósio | Dy | 0 0 | +2 | +3 | +4 | n / D | ||||||||||||
| 67 | hólmio | Ho | 0 0 | +2 | +3 | n / D | |||||||||||||
| 68 | érbio | Er | 0 0 | +2 | +3 | n / D | |||||||||||||
| 69 | túlio | Tm | +2 | +3 | n / D | ||||||||||||||
| 70 | itérbio | Yb | +2 | +3 | n / D | ||||||||||||||
| 71 | lutécio | Lu | 0 0 | +2 | +3 | n / D | |||||||||||||
| 72 | háfnio | Hf | -2 | +1 | +2 | +3 | +4 | 4 | |||||||||||
| 73 | tântalo | Ta | -3 | −1 | +1 | +2 | +3 | +4 | +5 | 5 | |||||||||
| 74 | tungstênio | W | -4 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 6 | ||||||
| 75 | rênio | Ré | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | 7 | ||||||
| 76 | ósmio | Os | -4 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | 8 | ||||
| 77 | irídio | Ir | -3 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | +9 | 9 | ||||
| 78 | platina | Pt | -3 | -2 | −1 | 0 0 | +1 | +2 | +3 | +4 | +5 | +6 | 10 | ||||||
| 79 | ouro | Au | -3 | -2 | −1 | +1 | +2 | +3 | +5 | 11 | |||||||||
| 80 | mercúrio | Hg | -2 | +1 | +2 | 12 | |||||||||||||
| 81 | tálio | Tl | -5 | -2 | −1 | +1 | +2 | +3 | 13 | ||||||||||
| 82 | conduzir | Pb | -4 | -2 | −1 | +1 | +2 | +3 | +4 | 14 | |||||||||
| 83 | bismuto | Bi | -3 | -2 | −1 | +1 | +2 | +3 | +4 | +5 | 15 | ||||||||
| 84 | polônio | Po | -2 | +2 | +4 | +5 | +6 | 16 | |||||||||||
| 85 | astático | At | −1 | +1 | +3 | +5 | +7 | 17 | |||||||||||
| 86 | radão | Rn | +2 | +6 | 18 | ||||||||||||||
| 87 | francium | Fr | +1 | 1 1 | |||||||||||||||
| 88 | rádio | Ra | +2 | 2 | |||||||||||||||
| 89 | actínio | Ac | +3 | 3 | |||||||||||||||
| 90 | tório | º | +1 | +2 | +3 | +4 | n / D | ||||||||||||
| 91 | protactínio | Pa | +3 | +4 | +5 | n / D | |||||||||||||
| 92 | urânio | você | +1 | +2 | +3 | +4 | +5 | +6 | n / D | ||||||||||
| 93 | neptúnio | Np | +2 | +3 | +4 | +5 | +6 | +7 | n / D | ||||||||||
| 94 | plutônio | Pu | +2 | +3 | +4 | +5 | +6 | +7 | n / D | ||||||||||
| 95 | amerício | Sou | +2 | +3 | +4 | +5 | +6 | +7 | n / D | ||||||||||
| 96 | cúrio | Cm | +3 | +4 | +5 | +6 | n / D | ||||||||||||
| 97 | berquélio | Bk | +3 | +4 | +5 | n / D | |||||||||||||
| 98 | californium | Cf | +2 | +3 | +4 | +5 | n / D | ||||||||||||
| 99 | einsteinio | Es | +2 | +3 | +4 | n / D | |||||||||||||
| 100 | férmio | Fm | +2 | +3 | n / D | ||||||||||||||
| 101 | Mendelevium | Md | +2 | +3 | n / D | ||||||||||||||
| 102 | nobelium | Não | +2 | +3 | n / D | ||||||||||||||
| 103 | Laurêncio | Lr | +3 | n / D | |||||||||||||||
| 104 | rutherfordium | Rf | +4 | 4 | |||||||||||||||
| 105 | dubnium | Db | +5 | 5 | |||||||||||||||
| 106 | seaborgium | Sg | 0 0 | +6 | 6 | ||||||||||||||
| 107 | bohrium | Bh | +7 | 7 | |||||||||||||||
| 108 | hassium | Hs | +8 | 8 | |||||||||||||||
| 109 | meitnerium | Mt | 9 | ||||||||||||||||
| 110 | darmstadtium | Ds | 10 | ||||||||||||||||
| 111 | roentgenium | Rg | 11 | ||||||||||||||||
| 112 | copernicium | Cn | +2 | 12 | |||||||||||||||
| 113 | nihonium | Nh | 13 | ||||||||||||||||
| 114 | flerovium | Fl | 14 | ||||||||||||||||
| 115 | moscovium | Mc | 15 | ||||||||||||||||
| 116 | fígado | Lv | 16 | ||||||||||||||||
| 117 | tennessine | Ts | 17 | ||||||||||||||||
| 118 | oganesson | Og | 18 | ||||||||||||||||
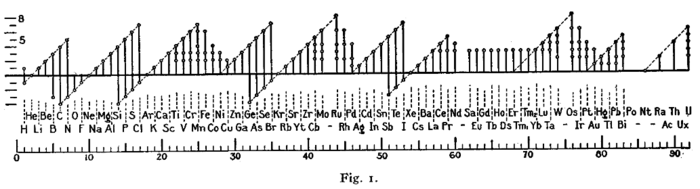
Formulários iniciais (regra do octeto)
Uma figura com formato semelhante (mostrado abaixo) foi usada por Irving Langmuir em 1919 em um dos primeiros artigos sobre a regra do octeto . A periodicidade dos estados de oxidação foi uma das evidências que levaram Langmuir a adotar a regra.