Trimerização de alcino - Alkyne trimerisation
Uma reação de trimerização de alcino é uma reação de cicloadição [2 + 2 + 2] em que três unidades de alcino reagem para formar um anel de benzeno . A reação requer um catalisador de metal. O processo é de interesse histórico, além de ser aplicável à síntese orgânica . Por ser uma reação de cicloadição, possui alta economia de átomos . Muitas variações foram desenvolvidas, incluindo a ciclização de misturas de alcinos e alcenos, bem como alcinos e nitrilos .
Mecanismo e estereoquímica
A trimerização do acetileno em benzeno é altamente exergônica, ocorrendo com uma variação de energia livre de 142 kcal / mol à temperatura ambiente. Barreiras cinéticas, no entanto, impedem que a reação prossiga suavemente. A descoberta veio em 1948, quando Reppe e Schweckendiek relataram seus resultados do tempo de guerra, mostrando que os compostos de níquel são catalisadores eficazes:
- 3 RC 2 H → C 6 R 3 H 3
Desde esta descoberta, muitas outras ciclotrimerizações foram relatadas.
Mecanismo
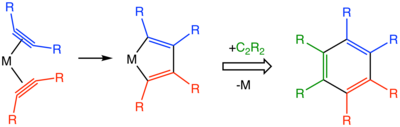
Em termos de mecanismo, as reações começam com a formação de complexos metal-alcino . A combinação de dois alcinos dentro da esfera de coordenação fornece um metalaciclopentadieno. Partindo do intermediário de metalaciclopentadieno, muitas vias podem ser consideradas, incluindo metalocicloheptatrienos, metalanorbornadienos e uma estrutura mais complicada com um ligante carbenóide.
Os catalisadores usados incluem ciclopentadienilcobalto dicarbonil e catalisador de Wilkinson .
Estereoquímica e regioquímica
A trimerização de alcinos assimétricos dá dois benzenos isoméricos. Por exemplo, fenilacetileno fornece 1,3,5- e 1,2,4-C 6 R 3 H 3 . O padrão de substituição sobre o produto areno é determinado em duas etapas: formação do intermediário metalociclopentadieno e incorporação do terceiro equivalente de alcino . O volume estérico nos parceiros de acoplamento alcino e catalisador foram invocados como os elementos de controle da regiosseletividade.
Catalisadores quirais têm sido empregados em combinação com arinas para produzir produtos atropisoméricos não racêmicos .
Escopo e limitações
Os catalisadores para ciclotrimerização são seletivos para ligações triplas, o que dá à reação um escopo de substrato bastante amplo. Muitos grupos funcionais são tolerados. A trimerização intermolecular regiosseletiva de alcinos assimétricos permanece um problema não resolvido.
Talvez o desenvolvimento mais útil nesta área, pelo menos do ponto de vista comercial, seja a cotrimerização de nitrilos e alcinos. Esta reação é uma via prática para algumas piridinas substituídas .
Alguns catalisadores são desativados pela formação de complexos η 4 de 18 elétrons estáveis . Ciclobutadieno , ciclohexadieno e complexos de areno foram todos observados como catalisadores inativados fora do ciclo. Além de polímeros de alta ordem, dímeros e trímeros, que se originam de baixas regio- e quimiosseletividades, foram observados produtos colaterais de enino derivados da dimerização de alcino. Os catalisadores de ródio são particularmente adeptos da formação de enino (veja abaixo). Para catálise de níquel , a formação de anéis maiores (particularmente ciclooctatetraeno ) pode ser um problema.
Aplicações sintéticas
A ciclização envolvendo substratos nos quais algumas ou todas as unidades alcino estão amarradas juntas pode fornecer sistemas de anéis fundidos. O comprimento da (s) corrente (s) controla os tamanhos dos anéis adicionais. A adição de um 1,5- diino com um alcino produz um benzociclobuteno , uma estrutura tensionada que pode então ser induzida a sofrer outras reações.
Todas as três unidades alcino podem ser amarradas, levando à criação de três anéis em uma única etapa, com cada um dos dois tamanhos de anel adicionais controlados pelos respectivos comprimentos de amarração.
Os triinos lotados podem se transformar em produtos que exibem quiralidade helicoidal . Em um exemplo notável para a formação de três novos anéis aromáticos em uma etapa, o triino mostrado é transformado no produto helicoidal por meio de tratamento com ciclopentadienilcobalto dicarbonil . Em 2004, esse processo ainda não tinha se tornado assimétrico, mas os produtos podiam ser separados por HPLC quiral . A ciclização realizada com um diino e um alcino separado proporciona maior controle. Usando ciclopentadienilcobalto dicarbonil , CpCo (CO) 2 comercialmente disponível , como catalisador, bis (trimetilsilil) acetileno (BTMSA) irá reagir com um benzeno diino-1,2-dissubstituído para formar um sistema aromático de antroquinona :
A benzina , gerada in situ a partir de um anel de benzeno contendo substituintes triflato e trimetilsilila orto- distribuídos , pode ser usada para gerar um arino no lugar de um acetileno e combinado com um diino adequado. Esse derivado de benzeno reage com 1,7-octadino na presença de um catalisador adequado para gerar um sistema de naftaleno. Este é um exemplo de uma reação hexadeidro Diels-Alder .
Comparação com outros métodos
A ciclotrimerização apresenta uma alternativa para a funcionalização de compostos aromáticos pré-formados por meio da substituição eletrofílica ou nucleofílica , cuja regiosseletividade às vezes pode ser difícil de controlar.
Outros métodos para a formação direta de anéis aromáticos a partir de precursores substituídos e insaturados incluem a reação de Dötz , catalisada por paládio [4 + 2] benzanulação de eninos com alcinos e cicloadição mediada por ácido de Lewis [4 + 2] de eninos com alcinos. A ciclização de espécies transitórias de benzina com alcinos, catalisada por paládio, também pode produzir compostos aromáticos substituídos.
Leitura adicional
- Musso, F .; Solari, E .; Floriani, C. (1997). "Ativação de hidrocarbonetos com haletos metálicos: tetracloreto de zircônio que catalisa a reação de Jacobsen e auxilia na trimerização de alcinos por meio da formação de complexos η 6 -Arene-Zircônio (IV)". Organometálicos . 16 (22): 4889. doi : 10,1021 / om970438g .
- Rodríguez, J. Gonzalo; Martín-Villamil, Rosa; Fonseca, Isabel (1997). "Ciclotrimerização catalisada por Tris (2,4-pentanedionato) vanádio e polimerização de 4- (N, N-dimetilamino) feniletino: estrutura de raios-X de 1,2,4-tris [4- (N, N-dimetilamino) fenil ]benzeno". Journal of the Chemical Society, Perkin Transactions 1 (6): 945–948. doi : 10.1039 / a605474i . ISSN 0300-922X .
- Sakurai, H .; Nakadaira, Y .; Hosomi, A .; Eriyama, Y .; Hirama, K .; Kabuto, C. (1984). "Química de compostos de silício orgânico. 193. Ciclotrimerização intramolecular de triinos macrocíclicos e acíclicos com carbonilas metálicas do Grupo 6. A formação de fulveno e benzeno". Geléia. Chem. Soc . 106 (26): 8315. doi : 10.1021 / ja00338a063 .
- Amer, I .; Bernstein, T .; Eisen, M .; Blum, J .; Vollhardt, KPC (1990). "Oligomerização de alcinos pelo sistema catalisador RhCl 3 -aliquat 336 Parte 1. Formação de derivados de benzeno". J. Mol. Catal . 60 (3): 313. doi : 10.1016 / 0304-5102 (90) 85254-F .
- Lee, CL; Hunt, CT; Balch, AL (1981). "Novas reações de ligações metal-metal. Reações de Pd 2 {(C 6 H 5 ) 2 PCH 2 P (C 6 H 5 ) 2 } 2 Cl 2 com acetilenos, olefinas e isotiocianatos". Inorg. Chem . 20 (8): 2498. doi : 10.1021 / ic50222a026 .
- Aalten, HL; van Koten, G .; Riethorst, E .; Stam, CH (1989). "A reação de Hurtley. 2. Novos complexos de acetilenos dissubstituídos com cobre (I) benzoatos tendo uma ligação orto carbono-cloro ou carbono-bromo reativa. Caracterização estrutural de raios-X de tetraquis (2-clorobenzoato) bis (dietil acetilenodicarboxilato) tetracopper ( EU)". Inorg. Chem . 28 (22): 4140. doi : 10.1021 / ic00321a020 .
- Hardesty, JH; Koerner, JB; Albright, TA; Lee, GB (1999). "Estudo Teórico da Trimerização do Acetileno com CpCo". Geléia. Chem. Soc . 121 (25): 6055. doi : 10.1021 / ja983098e .
- Ozerov, OV; Patrick, BO; Ladipo, FT (2000). "Altamente Regiosseletivo [2 + 2 + 2] Cycloaddition of Terminal Alkynes Catalyzed by η6-Arene Complexes of Titanium Supported by Dimethylsilyl-Bridgedp-tert-Butyl Calix [4] arene Ligand". Geléia. Chem. Soc . 122 (27): 6423. doi : 10.1021 / ja994543o .