Ciclooctatetraeno - Cyclooctatetraene
|
|
|||

|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Cicloocta-1,3,5,7-tetraeno |
|||
| Outros nomes
[8] Anuleno
(1 Z , 3 Z , 5 Z , 7 Z ) -Cicloocta-1,3,5,7-tetraeno 1,3,5,7-Ciclooctatetraeno COT |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.010.074 |
||
| Número EC | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 8 H 8 | |||
| Massa molar | 104,15 g / mol | ||
| Aparência | Amarelo claro | ||
| Densidade | 0,9250 g / cm 3 , líquido | ||
| Ponto de fusão | −5 a −3 ° C (23 a 27 ° F; 268 a 270 K) | ||
| Ponto de ebulição | 142 a 143 ° C (288 a 289 ° F; 415 a 416 K) | ||
| imiscível | |||
| -53,9 · 10 −6 cm 3 / mol | |||
| Perigos | |||
| Pictogramas GHS |
  
|
||
| Palavra-sinal GHS | Perigo | ||
| H225 , H304 , H315 , H319 , H335 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P280 , P301 + 310 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P331 , P332 + 313 , P337 + 313 , P362 , P370 + 378 , P403 + 233 , P403 + 235 , P405 | |||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | -11 ° C (12 ° F; 262 K) | ||
| 561 ° C (1.042 ° F; 834 K) | |||
| Compostos relacionados | |||
|
Hidrocarbonetos Relacionados
|
octano Tetraphenylene |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
1,3,5,7-Ciclooctatetraeno ( COT ) é um derivado insaturado do ciclooctano , com a fórmula C 8 H 8 . Também é conhecido como [8] anuleno . Este hidrocarboneto poliinsaturado é um líquido inflamável incolor a amarelo claro em temperatura ambiente. Por causa de sua relação estequiométrica com o benzeno , o COT tem sido objeto de muitas pesquisas e algumas controvérsias.
Ao contrário do benzeno, C 6 H 6 , ciclo-octatetraeno, C 8 H 8 , não é aromático , embora seu dianião , C
8H2−
8( ciclooctatetraenida ), é. Sua reatividade é característica de um polieno comum , ou seja, ele sofre reações de adição . O benzeno, ao contrário, sofre reações de substituição caracteristicamente , não acréscimos.
História
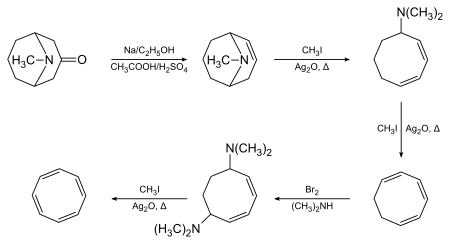
1,3,5,7-Cyclooctatetraene foi inicialmente sintetizado por Richard Willstätter em Munique em 1905 usando pseudopeletierina como o material de partida e a eliminação de Hofmann como a transformação chave:
Willstätter observou que o composto não apresentou a aromaticidade esperada. Entre 1939 e 1943, químicos em todos os Estados Unidos tentaram, sem sucesso, sintetizar COT. Eles racionalizaram sua falta de sucesso com a conclusão de que Willstätter não havia realmente sintetizado o composto, mas seu isômero, o estireno . Willstätter respondeu a essas críticas em sua autobiografia, onde observou que os químicos americanos "não se incomodaram" com a redução de seu ciclooctatetraeno a ciclooctano (uma reação impossível para o estireno). Durante a 2ª Guerra Mundial, Walter Reppe da BASF Ludwigshafen desenvolveu uma síntese simples de ciclo-octatetraeno a partir do acetileno, fornecendo material idêntico ao preparado por Willstätter. Quaisquer dúvidas remanescentes sobre a precisão da síntese original de Willstätter foram resolvidas quando Arthur C. Cope e colegas de trabalho no MIT relataram, em 1947, uma repetição completa da síntese de Willstätter, passo a passo, usando as técnicas originalmente relatadas. Eles obtiveram o mesmo ciclooctatetraeno e, subsequentemente, relataram a caracterização espectral moderna de muitos dos produtos intermediários, mais uma vez confirmando a precisão do trabalho original de Willstätter.
Estrutura e ligação
Os primeiros estudos demonstraram que o COT não exibia a química de um composto aromático. Então, os primeiros experimentos de difração de elétrons concluíram que as distâncias da ligação CC eram idênticas. No entanto, os dados de difração de raios-X de H. S. Kaufman demonstraram que o ciclooctatetraeno adota várias conformações e contém duas distâncias de ligação C – C distintas. Este resultado indicou que COT é um anuleno com ligações fixas alternadas de CC simples e duplas.
Em seu estado normal, o ciclooctatetraeno é não-plano e adota uma conformação de tubo com ângulos C = C − C = 126,1 ° e C = C − H = 117,6 °. O grupo de pontos do ciclooctatetraeno é D 2d .
Em seu estado de transição planar, o estado de transição D 4h é mais estável do que o estado de transição D 8h devido ao efeito Jahn-Teller .
Síntese
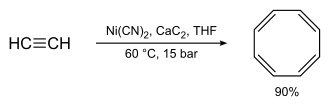
A síntese original de Richard Willstätter (4 reações de eliminação consecutivas em uma estrutura de ciclooctano) fornece rendimentos relativamente baixos. A síntese de Reppe de ciclooctatetraeno, que envolve o tratamento de acetileno em alta pressão com uma mistura quente de cianeto de níquel e carboneto de cálcio , foi muito melhor, com rendimentos químicos próximos a 90%:
O COT também pode ser preparado por fotólise do barreleno , um de seus isômeros estruturais , a reação ocorrendo por meio de outro isômero isolável , o semibulvaleno . Os derivados COT também podem ser sintetizados por meio de intermediários semibulvaleno. Na sequência ilustrada abaixo, o octaetilciclooctatetraeno (C 8 Et 8 ) é formado por isomerização térmica de octaetilsemibulvaleno, ele próprio formado por ciclodimerização mediada por brometo de cobre (I) de 1,2,3,4-tetraetil-1,4-dilitio-1, 3-butadieno.
Como o COT é instável e forma facilmente peróxidos orgânicos explosivos , uma pequena quantidade de hidroquinona é geralmente adicionada ao material disponível comercialmente. O teste de peróxidos é recomendado ao usar um frasco previamente aberto; os cristais brancos em volta do gargalo da garrafa podem ser compostos do peróxido, que pode explodir quando perturbado mecanicamente.
Ocorrência natural
O ciclooctatetraeno foi isolado de certos fungos.
Reações
As ligações π em COT reagem normalmente para olefinas, ao invés de sistemas de anéis aromáticos. Mono- e poli epóxidos podem ser gerados pela reação de COT com peroxiácidos ou com dimetildioxirano . Várias outras reações de adição também são conhecidas. Além disso, o poliacetileno pode ser sintetizado por meio da polimerização de abertura de anel de ciclooctatetraeno. O próprio COT - e também análogos com cadeias laterais - tem sido usado como ligantes de metal e em compostos sanduíche .
O ciclooctatetraeno também sofre reações de rearranjo para formar sistemas de anéis aromáticos . Por exemplo, a oxidação com sulfato de mercúrio (II) aquoso forma fenilacetaldeído e o rearranjo fotoquímico de seu monopóxido forma benzofurano .
Ciclooctatetraenida como um ligante e precursor do ligante
COT reage prontamente com o potássio metálico para formar o sal K 2 COT, que contém o dianião C
8H2−
8. O dianião é plano, octogonal e aromático com uma contagem de elétrons de Hückel de 10.
O ciclooctatetraeno forma complexos organometálicos com alguns metais, incluindo ítrio , lantanídeos e actinídeos. O composto sanduíche uranocene (u (COT) 2 ) apresenta dois ῃ 8 -COT ligandos. No bis (ciclooctatetraeno) ferro (Fe (COT) 2 ), um COT é ῃ 6 e o outro é ῃ 4 . (Ciclooctatetraeno) tricarbonil de ferro apresenta ῃ 4 -COT. Os espectros de RMN de 1 H à temperatura ambiente desses complexos de ferro são singletes, indicativos de fluxionalidade .
O ciclooctatetraeno é clorado para dar um composto [4.2.0] - bicíclico , que reage posteriormente com acetilenodicarboxilato de dimetila em uma reação de Diels-Alder (DA). Retro-DA a 200 ° C libera cis-diclorociclobuteno. Este composto reage com diiron nonacarbonyl para dar ciclobutadieno ferro tricarbonil .
Veja também
- Ciclobutadieno
- Pentalene
- Barrelene , isômero estrutural de ciclooctatetraeno
- Heptafulvene , isômero estrutural do ciclooctatetraeno
- Semibullvalene
- Benzeno