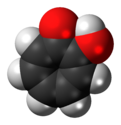
Tropolone - Tropolone
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
2-hidroxiciclohepta-2,4,6-trien-1-ona |
|||
| Outros nomes
2-hidroxitropona; Purpurocatecol
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,007,799 |
||
| Número EC | |||
| KEGG | |||
| Malha | D014334 | ||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 7 H 6 O 2 | |||
| Massa molar | 122,12 g / mol | ||
| Ponto de fusão | 50 a 52 ° C (122 a 126 ° F; 323 a 325 K) | ||
| Ponto de ebulição | 80 a 84 ° C (176 a 183 ° F; 353 a 357 K) (0,1 mmHg) | ||
| Acidez (p K a ) | 6,89 (e -0,5 para ácido conjugado) | ||
| -61 · 10 −6 cm 3 / mol | |||
| Perigos | |||
| Frases S (desatualizado) | S22 S24 / 25 | ||
| Ponto de inflamação | 112 ° C (234 ° F; 385 K) | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
Hinokitiol (4-isopropil-tropolona) | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Tropolone é um composto orgânico com a fórmula C 7 H 5 (OH) O. É um sólido amarelo claro que é solúvel em solventes orgânicos. O composto tem sido de interesse de pesquisadores químicos por causa de sua estrutura eletrônica incomum e seu papel como um precursor de ligante. Embora não seja geralmente preparado a partir do tropone , pode ser visto como seu derivado com um grupo hidroxila na posição 2.
Síntese e reações
Muitos métodos foram descritos para a síntese da tropolona. Um envolve a bromação de 1,2-cicloheptanodiona com N- bromossuccinimida seguida de desidrohalogenação a temperaturas elevadas, enquanto outro usa a condensação de aciloína do éster etílico do ácido pimélico, a aciloína novamente seguida de oxidação por bromo .
O composto sofre prontamente O-alquilação para dar derivados cicloheptatrienil, que por sua vez são intermediários sintéticos versáteis. Com cátions metálicos, ele sofre desprotonação para dar complexos de quelato, por exemplo, Cu (O 2 C 7 H 5 ) 2 . A tropolona é ácida (base conjugada mostrada, E) com um pKa de 7, que está entre o do fenol (10) e o do ácido benzóico (4). O aumento da acidez em comparação com o fenol é devido à estabilização de ressonância regular .
Ocorrência natural
Cerca de 200 derivados de tropolona de ocorrência natural foram isolados, principalmente de plantas e fungos . Compostos tropolona e seus derivados incluem dolabrins, dolabrinols, thujaplicins , thujaplicinols, ácido stipitatic , ácido stipitatonic, nootkatin, nootkatinol, ácido puberúlico, ácido puberulónico, sepedonin, 4-acetyltropolone, pygmaein, isopygmaein, procein, chanootin, benzotropolones (tais como purpurogallin , crocipodina, goupiolona A e B), teaflavina e derivados, bromotropolonas, tropoisoquinolinas e tropoloisoquinolinas (tais como grandirubrina, imerubrina, isoimerubrina, pareitropona, pareirubrina A e B), colchicina , colchicona e outros. O tropolone surge por meio de uma via de policetídeo , que fornece um intermediário fenólico que sofre expansão do anel.
Eles são encontrados especialmente em espécies de plantas específicas, como as famílias Cupressaceae e Liliaceae . Os tropolones são mais abundantes no cerne, folhas e cascas das plantas, portanto, os óleos essenciais são ricos em vários tipos de tropolones. Os primeiros derivados naturais da tropolona foram estudados e purificados em meados da década de 1930 e início da década de 1940. Thuja plicata , Thujopsis dolabrata , Chamaecyparis obtusa , Chamaecyparis taiwanensis e Juniperus thurifera estavam na lista de árvores das quais os primeiros tropolones foram identificados. Os primeiros tropolones sintéticos foram thujaplicins derivados de Ralph Raphael .
Efeitos biológicos
É um inibidor da polifenol oxidase da uva e da tirosinase do cogumelo .
Derivados de tropolona
| Nome | Estrutura química | Fontes naturais |
|---|---|---|
| Tropolone | Pseudomonas lindbergii , Pseudomonas plantarii | |
| Hinokitiol | Árvores Cupressaceae | |
| Ácido estipitático | Talaromyces stipitatus | |
| Colchicina | Colchicum autumnale , Gloriosa superba |
| Classe | Exemplos | Principais fontes naturais | Instruções de pesquisa | Patenteado em produtos |
|---|---|---|---|---|
| Tropolones simples | Tropolone | Pseudomonas lindbergii , Pseudomonas plantarii | Antibacteriano, antifúngico, inseticida, pesticida, inibição do crescimento vegetal, antiinflamatório, antioxidante, neuroproteção, anti-protease, anti-escurecimento (anti-tirosinase e anti-polifenol oxidase), antineoplásico, quelante | - |
| Dolabrins | β-dolabrin, α-dolabrinol | Caragana pygmaea , Cupressus goveniana , Cupressus abramsiana , Thujopsis dolabrata | Antibacteriano, antifúngico, inseticida, pesticida, inibição do crescimento vegetal, inibição da protease | Repelente de insetos, desodorante |
| Thujaplicins | α-thujaplicin, β-thujaplicin ( hinokitiol ), γ-thujaplicin, thujaplicinol | Chamaecyparis obtusa , Thuja plicata , thujopsis dolabrata , Juniperus Cedrus , cedro-do-atlas , Cupressus lusitanica , Chamaecyparis lawsoniana , Chamaecyparis taiwanensis , thyoides Chamaecyparis , Cupressus arizonica , Cupressus macnabiana , Cupressus macrocarpa , Cupressus guadalupensis , Juniperus chinensis , Juniperus communis , Juniperus californica , occidentalis Juniperus , Juniperus oxycedrus , Juniperus sabina , Calocedrus decurrens , Calocedrus formosana , Platycladus orientalis , Thuja occidentalis , Thuja standishii , Tetraclinis articulata , Cattleya forbesii , Carya glabra | Antifúngico, antibacteriano, anti-escurecimento (anti-tirosinase), quelante, inseticida, pesticida, antimalárico, antiviral, antiinflamatório, inibição do crescimento vegetal, anti-protease, antidiabético, antineoplásico, quimiossensibilizador, antioxidante, neuroproteção, medicina veterinária | Repelente de insetos, desodorante, pasta de dente, spray oral, cuidados com a pele e cabelo, conservante de madeira, aditivo alimentar, embalagem de alimentos |
| Tropolonas sesquiterpênicas | Nootkatin, nootkatinol, nootkatol, nootkatene, nootkatone , valencene-13-ol, nootkastatin | Chamaecyparis nootkatensis , toranja | Antifúngico, anti-escurecimento (anti-tirosinase), inseticida, fungicida, antineoplásico | Repelentes de insetos, sabor, perfumaria |
| Pigmeus | Pygmaein, Isopygmaein | Caragana pygmaea , Cupressus goveniana , Cupressus abramsiana | - | - |
| Benzotropolonas | Purpurogallin , crocipodin, goupiolone A e B | Espécies Quercus , Leccinum crocipodium , Goupia glabra | Antibacteriano, inibição do crescimento vegetal, inibição da protease, antineoplásico, antimalárico, antioxidante, antiviral | Aditivo alimentar |
| Theaflavins | Theaflavin , ácido theaflavic, theaflavate A e B | Camellia sinensis ,espécie Quercus | Antibacteriano, antiinflamatório, antioxidante, antiviral, antidiabético, quimiossensibilizador | - |
| Tropoisoquinolinas e tropoloisoquinolinas | Grandirubrina, imerubrina, isoimerubrina, pareitropona, pareirubrina A e B | Cissampelos pareira , Abuta grandifolia | Antileucêmico | - |
| Alcalóides tropone | Colchicina , demecolcina | Colchicum autumnale , Gloriosa superba | Antimitótico, antiinflamatório, anti-gota, melhoramento de plantas | Medicamento farmacêutico |