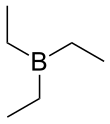
Trietilborano - Triethylborane
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Trietilborano |
|||
| Outros nomes
Trietilborina, trietilborão
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard |
100,002,383 |
||
| Número EC | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 6 H 15 B | |||
| Massa molar | 98,00 g / mol | ||
| Aparência | Líquido incolor a amarelo pálido | ||
| Densidade | 0,677 g / cm 3 | ||
| Ponto de fusão | −93 ° C (−135 ° F; 180 K) | ||
| Ponto de ebulição | 95 ° C (203 ° F; 368 K) | ||
| Não aplicável; altamente reativo | |||
| Perigos | |||
| Riscos principais | Espontaneamente inflamável ao ar; causa queimaduras | ||
| Ficha de dados de segurança | SDS externo | ||
| Frases R (desatualizado) | R11 R14 / 15 R17 R19 R34 R35 R36 / 37 | ||
| Frases S (desatualizado) | S6 S7 / 8 S16 S33 S36 / 37/39 S43 A S45 S29 | ||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | <−20 ° C (−4 ° F; 253 K) | ||
| −20 ° C (−4 ° F; 253 K) | |||
| Compostos relacionados | |||
|
Compostos relacionados
|
|||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O trietilborano ( TEB ), também denominado trietilborão , é um organoborano (um composto com uma ligação BC). É um líquido pirofórico incolor . A sua fórmula química é (C 2 H 5 ) 3 B, abreviado Et 3 B . É solúvel em solventes orgânicos tetrahidrofurano e hexano .
Preparação e estrutura
O trietilborano é preparado pela reação de trimetilborato com trietilalumínio :
- Et 3 Al + (MeO) 3 B → Et 3 B + (MeO) 3 Al
A molécula é monomérica, ao contrário do H 3 B e do Et 3 Al, que tendem a se dimerizar. Possui um núcleo plano BC 3 .
Formulários
Motor turbojato
O trietilborano foi usado para inflamar o combustível JP-7 nos motores turbojato / ramjet Pratt & Whitney J58 que acionam o Lockheed SR-71 Blackbird e seu predecessor, o A-12 OXCART . O trietilborano é adequado para isso por causa de suas propriedades pirofóricas , especialmente pelo fato de que queima a uma temperatura muito alta. Foi escolhido como método de ignição por razões de confiabilidade, e no caso do Blackbird, porque o combustível JP-7 tem volatilidade muito baixa e é difícil de acender. As velas de ignição convencionais representam um alto risco de mau funcionamento. O trietilborano foi usado para dar partida em cada motor e para acender os pós - combustores .
Foguete
Misturado com 10-15% de trietilalumínio , foi usado antes da decolagem para acender os motores F-1 do foguete Saturno V.
O foguete SpaceX Falcon 9 também usa uma mistura de trietilalumínio-trietilborano (TEA-TEB) como ignitor de primeiro e segundo estágios.
Química orgânica
Industrialmente, o trietilborano é utilizado como iniciador em reações radicais , onde é eficaz mesmo em baixas temperaturas. Como iniciador, pode substituir alguns compostos organoestânicos .
Ele reage com enolatos metálicos , produzindo enoxitrietilboratos que podem ser alquilados no átomo de carbono α da cetona mais seletivamente do que em sua ausência. Por exemplo, o enolato do tratamento da ciclohexanona com hidreto de potássio produz 2-alilciclohexanona com 90% de rendimento quando o trietilborano está presente. Sem ele, a mistura de produto contém 43% do produto mono-alilado, 31% de ciclohexanonas dialiladas e 28% de material de partida não reagido. A escolha da base e da temperatura influencia se o enolato mais ou menos estável é produzido, permitindo o controle sobre a posição dos substituintes. Partindo de 2-metilciclohexanona, reagindo com hidreto de potássio e trietilborano em THF à temperatura ambiente leva ao enolato mais substituído (e mais estável), enquanto a reação a −78 ° C com hexametildisilazida de potássio , KN [Si (CH
3)
3]
2e o trietilborano gera o enolato menos substituído (e menos estável). Após a reação com iodeto de metila, a primeira mistura dá 2,2-dimetilciclohexanona com 90% de rendimento, enquanto a última produz 2,6-dimetilciclohexanona com 93% de rendimento.
É usado na reação de desoxigenação Barton-McCombie para desoxigenação de álcoois. Em combinação com hidreto de tri- terc- butoxialumínio de lítio, ele cliva os éteres. Por exemplo, o THF é convertido, após hidrólise, em 1-butanol . Também promove certas variantes da reação Reformatskii .
O trietilborano é o precursor dos agentes redutores trietilboro-hidreto de lítio (" Superidrido ") e trietilboro-hidreto de sódio .
- MH + Et 3 B → MBHEt 3 (M = Li, Na)
O trietilborano reage com o metanol para formar dietil (metoxi) borano, que é usado como agente quelante na redução de Narasaka-Prasad para a geração estereosseletiva de sin -1,3- dióis de β-hidroxicetonas.
Segurança
O trietilborano é fortemente pirofórico , com uma temperatura de autoignição de −20 ° C (−4 ° F), queimando com uma chama verde-maçã característica de compostos de boro. Portanto, é normalmente manuseado e armazenado usando técnicas sem ar . O trietilborano também é agudamente tóxico se ingerido, com um DL50 de 235 mg / kg em cobaias.