Família da lipase pancreática - Pancreatic lipase family
 Complexo de lipase pancreática humana com colipase
| |||||||||
| Identificadores | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Símbolo | Lipase | ||||||||
| Pfam | PF00151 | ||||||||
| InterPro | IPR013818 | ||||||||
| PRÓSITO | PDOC00110 | ||||||||
| SCOP2 | 1lpa / SCOPe / SUPFAM | ||||||||
| Superfamília OPM | 127 | ||||||||
| Proteína OPM | 1lpa | ||||||||
| |||||||||
As lipases de triglicerídeos ( EC 3.1.1.3 ) são uma família de enzimas lipolíticas que hidrolisam as ligações éster dos triglicerídeos. As lipases são amplamente distribuídas em animais, plantas e procariotos.
Existem pelo menos três isozimas específicas de tecido em vertebrados superiores, pancreática, hepática e gástrica / lingual. Essas lipases estão intimamente relacionadas entre si e com a lipase de lipoproteína ( EC 3.1.1.34 ), que hidrolisa triglicerídeos de quilomícrons e lipoproteínas de densidade muito baixa (VLDL).
A região mais conservada em todas essas proteínas está centrada em um resíduo de serina que demonstrou participar, com uma histidina e um resíduo de ácido aspártico, em um sistema de retransmissão de carga. Essa região também está presente nas lipases de origem procariótica e na lecitina-colesterol aciltransferase ( EC 2.3.1.43 ) (LCAT), que catalisa a transferência de ácidos graxos entre a fosfatidilcolina e o colesterol.
Lipase pancreática humana
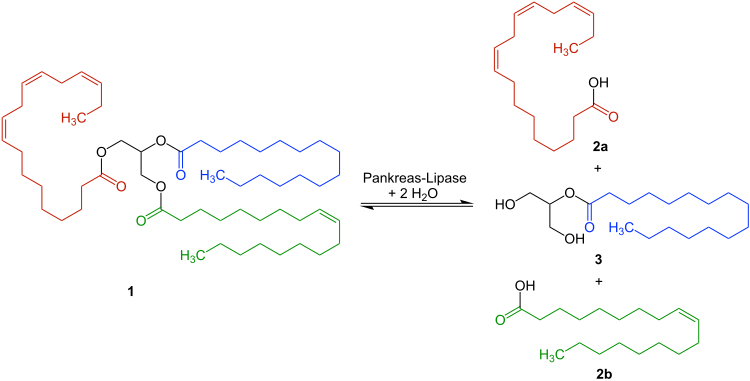
A lipase pancreática , também conhecida como triacilglicerol lipase pancreática ou esteapsina , é uma enzima secretada pelo pâncreas . Como a enzima lipase primária que hidrolisa (quebra) as moléculas de gordura da dieta no sistema digestivo humano, é uma das principais enzimas digestivas , convertendo substratos de triglicerídeos como 1 encontrados em óleos ingeridos em monoglicerídeos 3 e ácidos graxos livres 2a e 2b .
Os sais biliares secretados do fígado e armazenados na vesícula biliar são liberados no duodeno , onde revestem e emulsificam grandes gotas de gordura em gotas menores, aumentando assim a área de superfície total da gordura, o que permite que a lipase separe a gordura de forma mais eficaz. Os monômeros resultantes (2 ácidos graxos livres e um 2-monoacilglicerol) são então movidos por meio de peristaltismo ao longo do intestino delgado para serem absorvidos no sistema linfático por um vaso especializado chamado lácteo .
Ao contrário de algumas enzimas pancreáticas que são ativadas por clivagem proteolítica (por exemplo, tripsinogênio ), a lipase pancreática é secretada em sua forma final. No entanto, torna-se eficiente apenas na presença de colipase no duodeno .
Em humanos, a lipase pancreática é codificada pelo gene PNLIP .
Proteínas humanas contendo este domínio
Importância do diagnóstico
A lipase pancreática é secretada no duodeno através do sistema de dutos do pâncreas. Sua concentração no soro é normalmente muito baixa. Sob extrema perturbação da função pancreática, como pancreatite ou adenocarcinoma pancreático , o pâncreas pode começar a se autolisar e liberar enzimas pancreáticas, incluindo lipase pancreática no soro. Assim, por meio da medição da concentração sérica de lipase pancreática, a pancreatite aguda pode ser diagnosticada.
Inibidores
Os inibidores da lipase, como o orlistat, podem ser usados como tratamento para a obesidade.
Verificou-se que um peptídeo selecionado por exibição de fago inibia a lipase pancreática.
Veja também
Referências
Leitura adicional
- Roussel A, Yang Y, Ferrato F, Verger R, Cambillau C, Lowe M (novembro de 1998). "Estrutura e atividade da proteína 2 relacionada à lipase pancreática de rato" . J. Biol. Chem . 273 (48): 32121–8. doi : 10.1074 / jbc.273.48.32121 . PMID 9822688 .
- Crandall WV, Lowe ME (2001). "Os resíduos de colipase Glu64 e Arg65 são essenciais para a digestão normal de gordura mediada por lipase na presença de micelas de sais biliares" . J. Biol. Chem . 276 (16): 12505–12. doi : 10.1074 / jbc.M009986200 . PMID 11278590 .
- Freie AB, Ferrato F, Carrière F, Lowe ME (2006). "Val-407 e Ile-408 no beta5'-loop da lipase pancreática medeiam as interações lipase-colipase na presença de micelas de sais biliares" . J. Biol. Chem . 281 (12): 7793–800. doi : 10.1074 / jbc.M512984200 . PMC 3695395 . PMID 16431912 .
- Hegele RA, Ramdath DD, Ban MR, Carruthers MN, Carrington CV, Cao H (2001). "Polimorfismos em PNLIP, codificação da lipase pancreática e associações com características metabólicas" . J. Hum. Genet . 46 (6): 320–4. doi : 10.1007 / s100380170066 . PMID 11393534 .
- Chahinian H, Sias B, Carrière F (2000). "O domínio C-terminal da lipase pancreática: analogias funcionais e estruturais com domínios c2". Curr. Protein Pept. Sci . 1 (1): 91–103. doi : 10.2174 / 1389203003381487 . PMID 12369922 .
- Ranaldi S, Belle V, Woudstra M, Rodriguez J, Guigliarelli B, Sturgis J, Carriere F, Fournel A (2009). "Abertura e desdobramento da tampa em lipase pancreática humana em baixo pH revelado por rotulagem de rotação direcionada ao local EPR e espectroscopia FTIR". Bioquímica . 48 (3): 630–8. doi : 10.1021 / bi801250s . PMID 19113953 .
- Grupe A, Li Y, Rowland C, Nowotny P, Hinrichs AL, Smemo S, Kauwe JS, Maxwell TJ, Cherny S, Doil L, Tacey K, van Luchene R, Myers A, Wavrant-De Vrièze F, Kaleem M, Hollingworth P, Jehu L, Foy C, Archer N, Hamilton G, Holmans P, Morris CM, Catanese J, Sninsky J, White TJ, Powell J, Hardy J, O'Donovan M, Lovestone S, Jones L, Morris JC, Thal L, Owen M, Williams J, Goate A (2006). "Uma varredura do cromossomo 10 identifica um novo locus mostrando forte associação com a doença de Alzheimer de início tardio" . Sou. J. Hum. Genet . 78 (1): 78–88. doi : 10.1086 / 498851 . PMC 1380225 . PMID 16385451 .
- Thomas A, Allouche M, Basyn F, Brasseur R, Kerfelec B (2005). "Papel do padrão de hidrofobicidade da tampa na atividade da lipase pancreática" . J. Biol. Chem . 280 (48): 40074–83. doi : 10.1074 / jbc.M502123200 . PMID 16179352 .
- van Tilbeurgh H, Egloff MP, Martinez C, Rugani N, Verger R, Cambillau C (1993). "Ativação interfacial do complexo lipase-procolipase por micelas mistas revelada por cristalografia de raios-X". Nature . 362 (6423): 814–20. Bibcode : 1993Natur.362..814V . doi : 10.1038 / 362814a0 . PMID 8479519 . S2CID 4305832 .
- Lessinger JM, Arzoglou P, Ramos P, Visvikis A, Parashou S, Calam D, Profilis C, Férard G (2003). "Preparação e caracterização de materiais de referência para lipase pancreática humana: BCR 693 (de suco pancreático humano) e BCR 694 (recombinante)". Clin. Chem. Lab. Med . 41 (2): 169–76. doi : 10.1515 / CCLM.2003.028 . PMID 12667003 . S2CID 28593258 .
- Colin DY, Deprez-Beauclair P, Allouche M, Brasseur R, Kerfelec B (2008). "Explorando a cavidade do sítio ativo da lipase pancreática humana". Biochem. Biophys. Res. Comun . 370 (3): 394–8. doi : 10.1016 / j.bbrc.2008.03.043 . PMID 18353248 .
- Ramos P, Coste T, Piémont E, Lessinger JM, Bousquet JA, Chapus C, Kerfelec B, Férard G, Mély Y (2003). "A fluorescência resolvida no tempo permite o monitoramento seletivo de alterações ambientais de Trp30 na lipase pancreática humana contendo sete Trp". Bioquímica . 42 (43): 12488–96. doi : 10.1021 / bi034900e . PMID 14580194 .
- Yang Y, Lowe ME (1998). "Lipase triglicerídeo pancreático humano expressa em células de levedura: purificação e caracterização". Protein Expr. Purif . 13 (1): 36–40. doi : 10.1006 / prep.1998.0874 . PMID 9631512 .
- Sims HF, Jennens ML, Lowe ME (1993). "O gene que codifica a lipase pancreática humana: estrutura e conservação de uma sequência Alu na família do gene da lipase". Gene . 131 (2): 281–5. doi : 10.1016 / 0378-1119 (93) 90307-O . PMID 8406023 .
- Grandval P, De Caro A, De Caro J, Sias B, Carrière F, Verger R, Laugier R (2004). "Avaliação crítica de um ELISA específico e dois ensaios enzimáticos de lipases pancreáticas em soros humanos". Pancreatologia . 4 (6): 495–503, discussão 503–4. doi : 10.1159 / 000080246 . PMID 15316225 . S2CID 39583651 .
- Belle V, Fournel A, Woudstra M, Ranaldi S, Prieri F, Thomé V, Currault J, Verger R, Guigliarelli B, Carrière F (2007). "Sondando a abertura da tampa de lipase pancreática usando rotulagem de rotação dirigida ao local e espectroscopia EPR". Bioquímica . 46 (8): 2205–14. doi : 10.1021 / bi0616089 . PMID 17269661 .
- Lowe ME (1997). "Estrutura e função da lipase pancreática e colipase". Annu. Rev. Nutr . 17 : 141–58. doi : 10.1146 / annurev.nutr.17.1.141 . PMID 9240923 .
- Bourbon-Freie A, Dub RE, Xiao X, Lowe ME (2009). "Trp-107 e trp-253 são responsáveis pelo aumento da fluorescência em estado estacionário que acompanha a mudança conformacional na lipase triglicerídica pancreática humana induzida por tetrahidrolipstatina e sal biliar" . J. Biol. Chem . 284 (21): 14157–64. doi : 10.1074 / jbc.M901154200 . PMC 2682864 . PMID 19346257 .
- Ranaldi S, Belle V, Woudstra M, Bourgeas R, Guigliarelli B, Roche P, Vezin H, Carrière F, Fournel A (2010). "Amplitude da abertura da tampa de lipase pancreática em solução e identificação de subconjuntos conformacionais de rótulo de spin combinando onda contínua e espectroscopia EPR pulsada e dinâmica molecular". Bioquímica . 49 (10): 2140–9. doi : 10.1021 / bi901918f . PMID 20136147 .