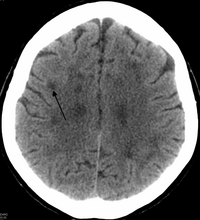
leucoencefalopatia difuso hereditário com esferóides - Hereditary diffuse leukoencephalopathy with spheroids
Hereditária leucoencefalopatia difusa com esferóides ( HDL ) é um início adulto rara desordem dominante autossómica caracterizada por cerebral matéria branca degeneração com desmielinização e axonais esferóides conduzindo a disfunção cognitiva e motora progressiva. Esferóides são inchaços axonais com descontínua ou ausência de mielina bainhas. Acredita-se que a doença resulta de disfunção da microglia primária que conduz à ruptura da integridade secundário axonal, danos neuroaxonal, e esferóides axonais focais que conduzem à desmielinização . Esferóides nas HDL se assemelham em certa medida, os produzidos por tensão de cisalhamento em um traumatismo craniano fechado , com danos para os axónios, causando-lhes a inchar, devido ao bloqueio do transporte axoplasmático . Em adição ao trauma, esferóides axonais podem ser encontradas no cérebro de idade, acidente vascular cerebral, e em outras doenças degenerativas. Em HDL, é incerto se desmielinização ocorre antes dos esferóides axonais ou o que desencadeia a neurodegeneração após o desenvolvimento aparentemente normal do cérebro e da matéria branca, embora déficits genéticos sugerem que a desmielinização e patologia axonal pode ser secundária a disfunção microglial. A síndrome clínica em pacientes com HDL não é específico e pode ser confundida com a doença de Alzheimer , demência frontotemporal , atípica Parkinsonismo , esclerose múltipla , ou a degeneração córtico-basal .
Conteúdo
Os sintomas clínicos
Com sintomas de alterações de personalidade, alterações comportamentais, demência , depressão e epilepsia, HDL tem sido comumente diagnosticada por uma série de outras doenças. Demência ou alterações comportamentais frontotemporal, por exemplo, têm comumente dirigiu alguns médicos a considerar erroneamente diagnósticos tais como a doença de Alzheimer, demência frontotemporal ou atípico parkinsonismo. A presença de alterações de substância branca levou a erros de diagnóstico de esclerose múltipla. As HDL geralmente manifesta-se com neuropsiquiátricos sintomas, progredindo para a demência, e depois de alguns anos mostra disfunção motora. Eventualmente, os pacientes tornam-se uma cadeira de rodas ou acamado.
Degeneração da matéria branca está associado e faz o diagnóstico diferencial de outras leucodistrofias início do adulto, tais como leucodistrofia metacromática (MLD), a doença de Krabbe (leucodistrofia celular globóide), e ligada ao X adrenoleucodistrofia (X-ADL).
| Doença | Trait exclusivo |
|---|---|
| MLD | Acúmulo de material metacromática na substância branca |
| doença de Krabbe | Presença de células derivadas de globóides microglia que têm múltiplos núcleos |
| X-ALD | Predominante parieto-occipital anormalidade substância branca |
| Fuga Branco Matter (VWM) Doença |
|
| Nasu-Hakola |
|
sintomas neuropsiquiátricos
Muitos sintomas neuropsiquiátricos foram identificados em estudos clínicos de pacientes HDL. Estes incluem depressão grave e ansiedade que foram identificados em cerca de 70% das famílias HDL, beirando a tendências suicidas e abuso de substâncias , tais como o alcoolismo . Além disso, os doentes podem apresentar desorientação, confusão, agitação, irritabilidade, agressividade, um estado mental alterado, a perda da capacidade de executar movimentos aprendidos ( apraxia ), ou a incapacidade de falar ( mutismo ).
comprometimento motor
Pessoas com HDL podem sofrer de tremores, diminuição dos movimentos do corpo, instabilidade ( Parkinsonismo , os músculos de um dos lados do corpo em contracção constante ( hemiparesia espástica ), deficiência na função motora e sensorial nas extremidades inferiores ( paraparesia ), paralisia resultante em parcial ou perda total de todas as extremidades e do tronco ( tetraparésia ), e a falta de coordenação dos movimentos musculares voluntários ( ataxia ).
doenças relacionadas
Desordens relacionadas com o mesmo espectro de doença como HDLs incluem doença Nasu-Hakola ( Osteodistrofias lipomembranosa policístico com leucoencefalopatia esclerosante ), e um tipo de leucodistrofia com macrófagos cheios de pigmento chamado pigmentada leucodistrofia ortocromático (Pold). Em adição a doença da matéria branca, Nasu-Hakola provoca quistos ósseos. É causada por mutações nos genes envolvidos na mesma factor estimulador de colónias (CSF) cascata de sinalização da via tal como identificado nas HDL.
Doença Nasu-Hakola parece ser causado por mutações na proteína TYRO proteína tirosina-quinase de ligação ( TYROBP - também conhecida como a DAP12) ou o receptor de disparo expressos em células 2 (mielóide trem2 proteína). Embora diferentes mutações do gene ocorrem dentro da via para Nasu-Hakola e HDLs, ambos são caracterizadas por degeneração substância branca com esferóides axonais. Pesquisadores atuais no campo acreditam que a análise mais aprofundada e comparação das duas anomalias genéticas nestes distúrbios podem levar a uma melhor compreensão dos mecanismos da doença nestas doenças raras. Pold exibe desmielinização dos axónios não inflamatória com sintomas iniciais de euforia, apatia, dor de cabeça, e disfunção executivo . Enquanto HDL é autossômica dominante, algumas famílias com Põld têm características que sugerem herança autossômica recessiva. No entanto, Pold foi recentemente demonstrado que têm a mesma base genética como HDLs.
Causas
A causa da HDL na maioria das famílias é a mutação no factor estimulador de colónias 1 receptor (CSF1R), um factor de crescimento para a microglia e monócitos / macrófagos, sugerindo que a disfunção da microglia pode ser primário nas HDL.
As mutações são concentrados em tirosina cinase do domínio (TKD) da proteína. As mutações foram encontradas principalmente nos exs 12-22 do intracelular TKD, incluindo 10 Mutações que têm um único nucleótido supressão e um único codão de eliminação que consiste de um tripleto de nucleótidos que foram removidos causando um todo aminoácido de não ser codificado. Além disso, três splicing mutações no local foram identificados que causou uma deleção em enquadramento de um exão , uma sequência de nucleótidos expressa, conduzindo à remoção de mais de 40 aminoácidos no TKD.
Esta determinação baseou-se em estudos genéticos de 14 HDLs famílias confirmando mutações neste gene. A proteína do receptor CSF1 funciona principalmente na regulação, a sobrevivência, a proliferação e diferenciação de células microgliais. O mecanismo de disfunção da microglia devido a mutações no CSF1R para a perda de mielina e formação esferóide axonal permanece desconhecido. Mais pesquisas são necessárias para entender melhor a doença patogênese .
Patologia
Em HDL, não é o alargamento dos ventrículos laterais e marcado afinamento ou enfraquecimento da substância branca cerebral. A perda de substância branca é causada por mielina perda. Estas alterações estão associadas com difusa gliose , perda moderada de axónios e muitas esferóides axonais.
Activado ou microglia ameboid e macrófagos que contêm restos de mielina, gotículas lipídicas e grânulos autofluorescente pigmentos castanhos são encontradas nas áreas com desmielinização e esferóides axonais. Em áreas severamente degenerados há muitos, astrócitos reactivos grandes preenchidos com gliais fibrilas .
Em casos de autópsia, foi demonstrado que alterações na substância branca estão relativamente limita ao cérebro , evitando o cerebelo e muitos dos grandes feixes de fibras do sistema nervoso. A excepção é os tractos corticospinais (intervalos piramidais) no tronco cerebral e, por vezes, na medula espinhal .
A patologia cerebral de HDL que se assemelha de doença Nasu-Hakola (Osteodistrofias lipomembranosa policístico com leucoencefalopatia esclerosante).
Diagnóstico
Pesquisa a partir de 2012 inclui investigações de função microglial. Este trabalho seria ainda esclarecer se a doença é principalmente um defeito na função microglia. Para tal estudo, as células microgliais de HDLs afins podem ser cultivadas a partir de cérebro de autópsia e analisado, em comparação com células normais da microglia, com base em diferenças nas ocorrências de mutação e expressão do factor de crescimento.
Os estudos clínicos e genealógicos
Para obter uma melhor compreensão da doença, os pesquisadores analisaram retrospectivamente prontuários de probandos e outros que foram avaliados através de exames clínicos ou questionários. As amostras de sangue são recolhidas a partir das famílias dos probandos para testes genéticos. Estes membros da família são avaliados utilizando a sua história médica padrão , em sua progressão dos sintomas como a de Parkinson ( Unified Disease Rating Scale de Parkinson ), e sobre a sua progressão de comprometimento cognitivo como demência ( Folstein Teste ).
neuroimagem
Padrão MRI scans foram realizadas em 1,5 scanners Tesla com espessura de 5 mm e espaçamento de 5 mm a tela para lesões da substância branca em famílias identificadas. Se intensidades de sinal das imagens de ressonância magnética são mais elevados em regiões de matéria branca do que em regiões de matéria cinzenta, o paciente é considerado em risco para as HDL, embora um número de outras desordens também pode produzir alterações da matéria branca e os resultados não são de diagnóstico sem genética teste ou patológica confirmação.
Patologia
As secções de tecido a partir de biópsias de cérebro ou de autópsia cérebros são geralmente incorporado em parafina a partir da qual são cortadas secções uma montada em lâminas de vidro para estudos histológicos. Manchas especiais de mielina e patologia axonal mostram as alterações anormais que são característicos de HDL são identificados na matéria branca do neocórtex , gânglios basais , tálamo , mesencéfalo , ponte e medula espinhal. Além de rotina histológicos métodos ( coloração H & E ), as amostras são avaliadas com imuno-histoquímica para a ubiquitina , proteína precursora de amilóide, e para caracterizar as alterações neurofilamento axonais e proteína básica mielina para a patologia de mielina. Manchas de imuno-histoquímica para a microglia (CD68 ou HLA-DR) e astritos (GFAP) são também técnicas úteis para caracterizar a patologia substância branca. Com uma patologia semelhante à pold, as HDL é geralmente agrupados como leucoencefalopatia início na idade adulta com esferóides axonais e glia pigmentado (alsp) de modo a dar a estas individualmente sob condições reconhecido maior atenção.
Classificação
HDLs cai sob a categoria de cérebro doenças da substância branca chamados leucoencefalopatias que são caracterizadas por um certo grau de disfunção substância branca. HDLs tem lesões da substância branca com anormalidades na bainha de mielina em torno de axónios, onde as influências causadores estão a ser continuamente explorado com base em descobertas recentes genéticos. Estudos realizados por Sundal e colegas da Suécia mostrou que um alelo de risco em caucasianos pode ser causador porque casos identificados têm sido, até agora, entre as grandes famílias caucasianas.
Gestão
Epidemiologia
Um perfil clínico médio a partir de estudos publicados mostra que a idade de início mediana para pacientes HDLs é de 44,3 anos, com uma duração média da doença de 5,8 anos e a idade média de morte a 53,2 anos. A partir de 2012, houve cerca de 15 casos identificados com pelo menos 11 casos esporádicos de HDL. casos HDL foram localizados na Alemanha, Noruega, Suécia e Estados Unidos, mostrando uma distribuição internacional, centrada entre o Norte da Europa e dos Estados Unidos.
Através do estudo de numerosos parentes, verificou-se que a doença não ocorreu entre apenas homens ou mulheres, mas sim foi distribuída uniformemente indicativo de uma autossômica em vez de uma doença genética ligada ao sexo . Observou-se também que os casos HDL não pular gerações como ocorreria com uma herança recessiva, e como tal tem sido rotulado autossômica dominante.
História
Esta doença foi descrita pela primeira vez em 1984 por Axelsson et al. em um grande sueco pedigree. É um distúrbio mais conhecido para neuropatologistas que os clínicos. A neuropatologista com um interesse em HDL, Dr. Dennis W. Dickson, identificou um número de casos de neuropatologia estudo de cérebros submetidos à investigação de demências e movimento do adulto-início familiares em Nova York e depois na Flórida. O reconhecimento da importância desta doença como causa de desordens de demência e de movimento adulto início foi ainda mais acentuada em 1997 na Mayo Clinic, quando o Dr. Zbigniew K. Wszolek identificou uma família com HDL que foi inicialmente pensado para ser devido a outro processo da doença ( FTDP-17), mas apenas uma autópsia de um e depois outros membros da família revelou que ele seja HDL. Wszolek estabelecida uma organização internacional consórcio em 2005 para identificar outras famílias e recolher amostras de DNA ou do cérebro de membros da família para confirmação neuropatológico e pesquisa genética na Clínica Mayo na Flórida.
Veja também
Referências
links externos
| Classificação | |
|---|---|
| Fontes externas |