Dióxido de selênio - Selenium dioxide

|
|
|
|

|
|
| Nomes | |
|---|---|
| Outros nomes
Óxido de selênio (IV)
Anidrido selenoso |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.028.358 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 3283 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| SeO 2 | |
| Massa molar | 110,96 g / mol |
| Aparência | Cristais brancos, tornam-se ligeiramente rosados com decomposição |
| Odor | rabanetes podres |
| Densidade | 3,954 g / cm 3 , sólido |
| Ponto de fusão | 340 ° C (644 ° F; 613 K) (tubo selado) |
| Ponto de ebulição | 350 ° C (662 ° F; 623 K) subl. |
| 38,4 g / 100 mL (20 ° C) 39,5 g / 100 mL (25 ° C) 82,5 g / 100 mL (65 ° C) |
|
| Solubilidade | solúvel em benzeno |
| Solubilidade em etanol | 6,7 g / 100 mL (15 ° C) |
| Solubilidade em acetona | 4,4 g / 100 mL (15 ° C) |
| Solubilidade em ácido acético | 1,11 g / 100 mL (14 ° C) |
| Solubilidade em metanol | 10,16 g / 100 mL (12 ° C) |
| Pressão de vapor | 1,65 kPa (70 ° C) |
| Acidez (p K a ) | 2,62; 8,32 |
| −27,2 · 10 −6 cm 3 / mol | |
|
Índice de refração ( n D )
|
> 1,76 |
| Estrutura | |
| veja o texto | |
| trigonal (Se) | |
| Perigos | |
| Ficha de dados de segurança | ICSC 0946 |
| Tóxico ( T ) Perigoso para o meio ambiente ( N ) |
|
| Frases R (desatualizado) | R23 / 25 , R33 , R50 / 53 |
| Frases S (desatualizado) | (S1 / 2) , S20 / 21 , S28 , S45 , S60 , S61 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LC Lo (o mais baixo publicado )
|
5890 mg / m 3 (coelho, 20 min) 6590 mg / m 3 (cabra, 10 min) 6590 mg / m 3 (ovelha, 10 min) |
| Compostos relacionados | |
|
Outros ânions
|
Dissulfeto de selênio |
|
Outros cátions
|
Dióxido de enxofre Dióxido de telúrio |
| Trióxido de selênio | |
|
Compostos relacionados
|
Ácido selenoso |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais no estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Dióxido de selênio é o composto químico com a fórmula SeO 2 . Este sólido incolor é um dos compostos de selênio mais freqüentemente encontrados .
Propriedades
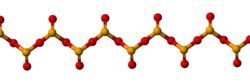
O SeO 2 sólido é um polímero unidimensional , cuja cadeia consiste em átomos alternados de selênio e oxigênio . Cada átomo de Se é piramidal e carrega um grupo terminal de óxido. Os comprimentos da ligação Se-O em ponte são 179 pm e a distância Se-O do terminal é 162 pm. A estereoquímica relativa em Se alterna ao longo da cadeia do polímero ( sindiotática ). Na fase gasosa, o dióxido de selênio está presente como dímeros e outras espécies oligoméricas, em temperaturas mais altas é monomérico. A forma monomérica adota uma estrutura curvada muito semelhante à do dióxido de enxofre com um comprimento de ligação de 161 pm. A forma dimérica foi isolada em uma matriz de argônio de baixa temperatura e os espectros vibracionais indicam que ela tem uma forma de cadeira centrosimétrica. A dissolução de SeO 2 em oxidicloreto de selênio dá o trímero [Se (O) O] 3 . O SeO 2 monomérico é uma molécula polar, com o momento de dipolo de 2,62 D apontado do ponto médio dos dois átomos de oxigênio até o átomo de selênio.
O sólido sublima prontamente. Em concentrações muito baixas, o vapor tem um odor repulsivo, parecido com raiz-forte em decomposição. Em concentrações mais altas, o vapor tem um odor semelhante ao de molho de raiz-forte e pode queimar o nariz e a garganta ao ser inalado. Enquanto o SO 2 tende a ser molecular e o SeO 2 é uma cadeia unidimensional, o TeO 2 é um polímero reticulado.
O SeO 2 é considerado um óxido ácido : ele se dissolve em água para formar o ácido selenoso . Freqüentemente, os termos ácido selenoso e dióxido de selênio são usados alternadamente. Ele reage com a base para formar sais de selenito contendo o SeO 2−
3 ânion. Por exemplo, a reação com hidróxido de sódio produz selenito de sódio :
- SeO 2 + 2 NaOH → Na 2 SeO 3 + H 2 O
Preparação
O dióxido de selênio é preparado pela oxidação do selênio pela queima no ar ou pela reação com ácido nítrico ou peróxido de hidrogênio , mas talvez a preparação mais conveniente seja a desidratação do ácido selenoso .
- 2 H 2 O 2 + Se → SeO 2 + 2 H 2 O
- 3 Se + 4 HNO 3 + H 2 O → 3 H 2 SeO 3 + 4 NO
- H 2 SeO 3 ⇌ SeO 2 + H 2 O
Ocorrência
A forma natural do dióxido de selênio, downeyite, é um mineral muito raro. Ele é encontrado em apenas alguns depósitos de carvão em chamas.
Usos
Síntese orgânica
SeO 2 é um reagente importante na síntese orgânica . A oxidação do paraldeído (trímero do acetaldeído) com SeO 2 dá glioxal e a oxidação da ciclohexanona dá ciclohexano-1,2-diona. O material de partida de selênio é reduzido a selênio e precipita como um sólido vermelho amorfo que pode ser facilmente filtrado. Esse tipo de reação é chamado de oxidação de Riley . Também é conhecido como um reagente para a oxidação "alílica", uma reação que acarreta a seguinte conversão
Isso pode ser descrito de forma mais geral como;
- R 2 C = CR'-CHR " 2 + [O] → R 2 C = CR'-C (OH) R" 2
onde R, R ', R "podem ser substituintes alquil ou aril .
Como corante
O dióxido de selênio confere uma cor vermelha ao vidro . É usado em pequenas quantidades para neutralizar a cor devido às impurezas do ferro e, assim, criar vidro (aparentemente) incolor. Em grandes quantidades, dá uma cor vermelha rubi profunda.
Dióxido de selênio é o ingrediente ativo em algumas soluções de azulamento frio .
Também foi usado como toner na revelação fotográfica .
Segurança
O selênio é um elemento essencial , mas a ingestão de mais de 5 mg / dia leva a sintomas inespecíficos .


