Seleneto de hidrogênio - Hydrogen selenide
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Seleneto de hidrogênio
|
|||
| Outros nomes
Ácido
hidroselênico selano hidreto de selênio |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.029.071 |
||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 2202 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| H 2 Se | |||
| Massa molar | 80,98 g / mol | ||
| Aparência | Gás incolor | ||
| Odor | rábano apodrecido | ||
| Densidade | 3,553 g / dm 3 | ||
| Ponto de fusão | −65,73 ° C (−86,31 ° F; 207,42 K) | ||
| Ponto de ebulição | −41,25 ° C (−42,25 ° F; 231,90 K) | ||
| 0,70 g / 100 mL | |||
| Solubilidade | solúvel em CS 2 , fosgênio | ||
| Pressão de vapor | 9,5 atm (21 ° C) | ||
| Acidez (p K a ) | 3,89 | ||
| Ácido conjugado | Selenônio | ||
| Base conjugada | Selenide | ||
| Estrutura | |||
| Dobrado | |||
| Perigos | |||
| Riscos principais | Extremamente tóxico e inflamável | ||
| Ficha de dados de segurança | ICSC 0284 | ||
|
|
|||
| Frases R (desatualizado) | R23 / 25 , R33 , R50 / 53 | ||
| Frases S (desatualizado) | (S1 / 2) , S20 / 21 , S28 , S45 , S60 , S61 | ||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | gás inflamável | ||
| Dose ou concentração letal (LD, LC): | |||
|
LC Lo (o mais baixo publicado )
|
0,3 ppm (cobaia, 8 h) 5,9 ppm (rato, 1 h) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 0,05 ppm (0,2 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 0,05 ppm (0,2 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
1 ppm | ||
| Compostos relacionados | |||
|
Outros ânions
|
H 2 O H 2 S H 2 Te H 2 Po |
||
|
Outros cátions
|
Na 2 Se Ag 2 Se |
||
|
Compostos relacionados
|
Arsine | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O seleneto de hidrogênio é um composto inorgânico com a fórmula H 2 Se. Este calcogeneto de hidrogênio é o hidreto de selênio mais simples e mais comumente encontrado . H 2 O Se é um líquido incolor, inflamável de gás em condições padrão. É o composto de selênio mais tóxico, com limite de exposição de 0,05 ppm em um período de 8 horas. Mesmo em concentrações extremamente baixas, este composto tem um cheiro muito irritante, parecido com o de raiz-forte em decomposição ou 'vazamento de gás', mas cheira a ovos podres em concentrações mais altas.
Estrutura e propriedades
H 2 Se adota uma estrutura curvada com um ângulo de ligação H − Se − H de 91 °. Consistente com esta estrutura, três bandas vibracionais ativas de IR são observadas: 2358, 2345 e 1034 cm −1 .
As propriedades de H 2 S e H 2 Se são semelhantes, embora o seleneto seja mais ácido com p K a = 3,89, e o segundo p K a = 11, ou 15,05 ± 0,02 a 25 ° C.
Preparação
Industrialmente, é produzido tratando o selênio elementar a T> 300 ° C com gás hidrogênio. Várias rotas para H 2 Se foram relatadas, as quais são adequadas para preparações em grande e pequena escala. Em laboratório, o H 2 Se é geralmente preparado pela ação da água sobre o Al 2 Se 3 , concomitante à formação de alumina hidratada . Uma reação relacionada envolve a hidrólise ácida de FeSe.
- Al 2 Se 3 + 6 H 2 O ⇌ 2 Al (OH) 3 + 3 H 2 Se
H 2 Se, também podem ser preparados por meio de métodos diferentes de acordo com o in situ geração em solução aquosa, utilizando hidreto de boro , teste Marsh e liga de Devarda . De acordo com o método Sonoda, H 2 Sé é gerado a partir da reacção de H 2 O e CO em si na presença de Et 3 N . H 2 Se pode ser adquirido em cilindros.
Reações
O selênio elementar pode ser recuperado do H 2 Se por meio de uma reação com dióxido de enxofre aquoso (SO 2 ).
- 2 H 2 Se + SO 2 ⇌ 2 H 2 O + 2 Se + S
Sua decomposição é usada para preparar o elemento de alta pureza.
Formulários
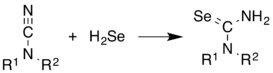
H 2 Se é comumente usado na síntese de compostos contendo Se. Ele adiciona alcenos. Ilustrativa é a síntese de selenoureias a partir de cianamidas .
H 2 gás Se é usado para narcótico semicondutores com selénio.
Segurança
O seleneto de hidrogênio é perigoso, sendo o composto de selênio mais tóxico e muito mais tóxico do que seu congênere sulfeto de hidrogênio . O valor do limite é 0,05 ppm. O gás atua como irritante em concentrações superiores a 0,3 ppm, que é o principal sinal de alerta de exposição; abaixo de 1 ppm, isso é "insuficiente para evitar a exposição", enquanto a 1,5 ppm a irritação é "intolerável". A exposição em altas concentrações, mesmo por menos de um minuto, faz com que o gás ataque os olhos e as membranas mucosas; isso causa sintomas semelhantes aos do resfriado por pelo menos alguns dias depois. Na Alemanha, o limite para água potável é 0,008 mg / L, e a US EPA recomenda uma contaminação máxima de 0,01 mg / L.
Apesar de ser altamente tóxico, nenhuma morte humana foi relatada. Suspeita-se que isso se deva à tendência do gás de oxidar-se para formar selênio vermelho nas membranas mucosas; o selênio elementar é menos tóxico do que os selenetos.