Diazometano - Diazomethane
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Diazometano
|
|
| Outros nomes
Azimetileno,
Azometileno, Diazirina |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100,005,803 |
| Número EC | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CH 2 N 2 | |
| Massa molar | 42,04 g / mol |
| Aparência | Gás amarelo |
| Odor | mofado |
| Densidade | 1,4 (ar = 1) |
| Ponto de fusão | −145 ° C (−229 ° F; 128 K) |
| Ponto de ebulição | −23 ° C (−9 ° F; 250 K) |
| hidrólise | |
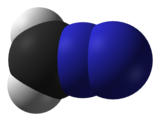
| Estrutura | |
| linear C = N = N | |
| polar | |
| Perigos | |
| Riscos principais | tóxico e explosivo |
| Pictogramas GHS |
 
|
| Palavra-sinal GHS | Perigo |
| H350 | |
| P201 , P202 , P281 , P308 + 313 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Dose ou concentração letal (LD, LC): | |
|
LC 50 ( concentração média )
|
175 ppm (cat, 10 min) |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 0,2 ppm (0,4 mg / m 3 ) |
|
REL (recomendado)
|
TWA 0,2 ppm (0,4 mg / m 3 ) |
|
IDLH (perigo imediato)
|
2 ppm |
| Compostos relacionados | |
|
Grupos funcionais relacionados ;
compostos |
RN = N = N ( azida ), RN = NR (azo); R 2 CN 2 R = Ph, tms, CF 3 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
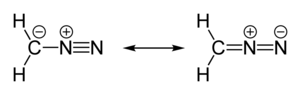
O diazometano é o composto químico CH 2 N 2 , descoberto pelo químico alemão Hans von Pechmann em 1894. É o composto diazo mais simples . Na forma pura, à temperatura ambiente, é um gás amarelo explosivo extremamente sensível ; assim, é quase universalmente usado como uma solução em éter dietílico . O composto é um agente de metilação popular em laboratório, mas é muito perigoso para ser empregado em escala industrial sem precauções especiais. O uso de diazometano foi significativamente reduzido pela introdução do reagente trimetilsilildiazometano mais seguro e equivalente .
Usar
Por segurança e conveniência, o diazometano é sempre preparado conforme necessário como uma solução em éter e usado como tal. Ele converte ácidos carboxílicos em ésteres metílicos e fenóis em seus éteres metílicos . Pensa-se que a reação prossegue via transferência de prótons do ácido carboxílico para o diazometano para dar o cátion metildiazônio, que reage com o íon carboxilato para dar o éster metílico e o gás nitrogênio. Estudos de rotulagem indicam que a transferência inicial de prótons é mais rápida do que a etapa de transferência de metila. Uma vez que a transferência de prótons é necessária para que a reação prossiga, esta reação é seletiva para os ácidos carboxílicos mais ácidos (p K a ~ 5) e fenóis (p K a ~ 10) em relação aos álcoois alifáticos (p K a ~ 15).
Em aplicações mais especializadas, diazometano e homólogos são usados na síntese de Arndt-Eistert e na reação de Büchner – Curtius – Schlotterbeck para homologação.
O diazometano reage com álcoois ou fenóis na presença de trifluoreto de boro (BF 3 ) para dar éteres metílicos .
O diazometano também é freqüentemente usado como fonte de carbeno . Ele prontamente participa de cicloadições 1,3-dipolares .
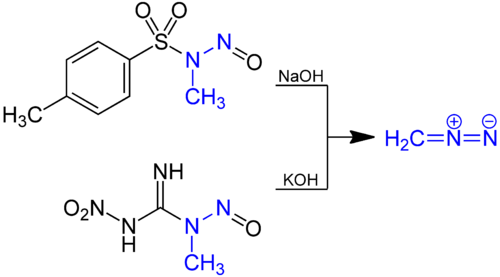
Preparação
O diazometano é preparado por hidrólise de uma solução etérea de uma N- metil nitrosamida com base aquosa. O precursor tradicional é N- nitroso- N- metilureia , mas este composto é um pouco instável, e hoje em dia compostos como N- metil- N ' -nitro- N - nitrosoguanidina (MNNG) e N- metil- N- nitroso- p -toluenossulfonamida (Diazald) são preferidos.
CH 2 N 2 reage com soluções básicas de D 2 O para dar o derivado deuterado CD 2 N 2 .
A concentração de CH 2 N 2 pode ser determinada de duas maneiras convenientes. Ele pode ser tratado com um excesso de ácido benzóico em Et 2 O frio . O ácido benzóico que não reagiu é então titulado de volta com NaOH padrão. Alternativamente, a concentração de CH 2 N 2 em Et 2 O pode ser determinada espectrofotometricamente a 410 nm, onde seu coeficiente de extinção , ε, é 7,2. A concentração de fase gasosa de diazometano pode ser determinada usando espectroscopia fotoacústica .
Compostos relacionados
O diazometano é isomérico e isoeletrônico com a cianamida mais estável , mas eles não podem se interconverter. Muitos derivados substituídos de diazometano foram preparados:
- O muito estável (CF 3 ) 2 CN 2 (2-diazo-1,1,1,3,3,3-hexafluoropropano; bp 12–13 ° C),
- Ph 2 CN 2 ( diazodifenilmetano ; pf 29-30 ° C).
- (CH 3 ) 3 SiCHN 2 ( trimetilsilildiazometano ), que está disponível comercialmente como uma solução e é tão eficaz quanto CH 2 N 2 para metilação.
- PhC (H) N 2 , um líquido vermelho pb <25 ° C a 0,1 mm Hg.
Segurança
O diazometano é tóxico por inalação ou por contato com a pele ou olhos (TLV 0,2 ppm). Os sintomas incluem desconforto no peito, dor de cabeça, fraqueza e, em casos graves, colapso. Os sintomas podem demorar. Mortes por envenenamento por diazometano foram relatadas. Em um caso, um trabalhador de laboratório consumiu um hambúrguer perto de uma estufa onde estava gerando uma grande quantidade de diazometano e morreu quatro dias depois de pneumonia fulminante. Como qualquer outro agente alquilante , espera-se que seja cancerígeno, mas tais preocupações são ofuscadas por sua grave toxicidade aguda.
O CH 2 N 2 pode explodir em contato com bordas afiadas, como juntas de vidro esmerilado, até mesmo arranhões em objetos de vidro. A vidraria deve ser inspecionada antes do uso e a preparação deve ocorrer atrás de um escudo anti-explosão. Kits especializados para preparar diazometano com juntas polidas à chama estão disponíveis comercialmente.
O composto explode quando aquecido além de 100 ° C, exposto a luz intensa, metais alcalinos ou sulfato de cálcio. O uso de um escudo anti-explosão é altamente recomendado ao usar este composto.
Um trabalho de prova de conceito foi feito com microfluídicos , em que a síntese contínua de ponto de uso de N- metil- N- nitrosoureia e hidróxido de potássio 0,93 M em água foi seguida por conversão de ponto de uso com ácido benzóico , resultando em um rendimento de 65% do éster de benzoato de metila em segundos a temperaturas variando de 0 a 50 ° C. O rendimento foi melhor do que em condições capilares; os microfluídicos foram creditados com "supressão de pontos quentes, baixa retenção, condições isotérmicas e mistura intensiva."
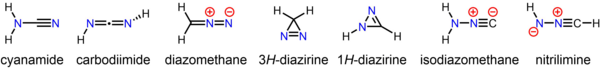
Isômeros
O composto estável cianamida , cujo tautômero menor é carbodiimida , é um isômero de diazometano. Menos estável mas ainda isómeros isoláveis de diazometano incluem o cíclico 3 H -diazirine e isocyanoamine ( isodiazomethane ). Além disso, a nitrilimina original foi observada em condições de isolamento de matriz.
Referências
links externos
- MSDS diazometano
- CDC - Guia de bolso do NIOSH para perigos químicos
- Boletim técnico Sigmaaldrich (PDF)
- Aplicações de diazometano da Sigma-Aldrich e disponibilidade comercial do precursor (Diazald)
- A reação Buchner – Curtius – Schlotterbeck no Instituto de Química, Skopje, Macedônia
- Identificação de artefatos (subprodutos) nas reações de diazometano e trimetilsilildiazometano