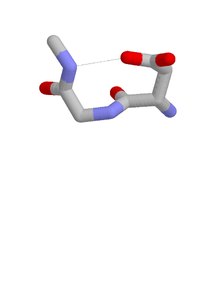
Asx turn - Asx turn
A curva Asx é uma característica estrutural em proteínas e polipeptídeos . Consiste em três resíduos de aminoácidos (marcados com i, i + 1 e i + 2) em que o resíduo i é um aspartato (Asp) ou asparagina (Asn) que forma uma ligação de hidrogênio de seu grupo de cadeia lateral CO para o grupo NH de cadeia principal de resíduo i + 2. Cerca de 14% dos resíduos Asx presentes nas proteínas pertencem às espiras Asx.
O nome "Asx" é usado aqui para representar os aminoácidos aspartato (Asp) ou asparagina (Asn).
Tipos
Quatro tipos de curvas Asx podem ser distinguidos: tipos I, I ', II e II'. Essas categorias correspondem às das voltas beta com ligações de hidrogênio mais conhecidas , que têm quatro resíduos e uma ligação de hidrogênio entre o CO do resíduo i e o NH do resíduo i + 3. As voltas Asx e as voltas beta têm laços ligados por hidrogênio estruturalmente semelhantes e exibem mimetismo da cadeia lateral-cadeia principal no sentido de que a cadeia lateral do resíduo i da volta Asx imita a cadeia principal do resíduo i da volta beta . Em relação à sua ocorrência em proteínas, eles diferem no fato de que o tipo I é o mais comum das quatro voltas beta, enquanto o tipo II 'é a mais comum das voltas Asx.
Ocorrência
As curvas Asx e ST ocorrem com frequência nos terminais N das hélices α . como parte de motivos Asx ou motivos ST, de modo que o Asx, serina ou treonina é o resíduo N. Eles são, portanto, frequentemente considerados como recursos de cobertura de hélice.
Motivos relacionados
Motivos semelhantes ocorrem com serina ou treonina como resíduo i, que são chamados de voltas ST . Apesar de serina e treonina terem um átomo de cadeia lateral a menos, de modo que o mimetismo da cadeia lateral-cadeia principal das voltas β é imperfeito, essas características ocorrem em proteínas como os quatro tipos em números que se aproximam das voltas Asx. Eles também exibem uma tendência de se substituir ao longo do tempo evolutivo.
Uma proporção de voltas Asx é acompanhada por uma ligação de hidrogênio mainchain – mainchain que os qualifica como motivos Asx .
Referências
- ^ Richardson, JS (1981). "A anatomia e taxonomia da estrutura da proteína". Advances in Protein Chemistry Volume 34 . Advances in Protein Chemistry. 34 . pp. 167-339. doi : 10.1016 / S0065-3233 (08) 60520-3 . ISBN 9780120342341 . PMID 7020376 .
- ^ Tainer, JA; Getzoff ED (1982). "Determinação e análise da estrutura 2 A do cobre, zinco superóxido dismutase". Journal of Molecular Biology . 160 (2): 181–217. doi : 10.1016 / 0022-2836 (82) 90174-7 . PMID 7175933 .
- ^ Rees, DC; Lewis M (1983). "Estrutura de cristal refinada de carboxipeptidase a com resolução de 1,54 Å". Journal of Molecular Biology . 168 (2): 367–387. doi : 10.1016 / S0022-2836 (83) 80024-2 . PMID 6887246 .
- ^ Eswar, N; Ramachandran C (1999). "Estruturas secundárias sem backbone: Uma análise do mimetismo do backbone por cadeias laterais polares em proteínas" . Protein Engineering . 12 (6): 447–455. doi : 10.1093 / proteína / 12.6.447 . PMID 10388841 .
- ^ Chakrabarti, P; Pal D (2001). "Inter-relações de conformações de cadeia lateral e cadeia principal em proteínas" . Progress in Biophysics and Molecular Biology . 76 (1–2): 1–102. doi : 10.1016 / s0079-6107 (01) 00005-0 . PMID 11389934 .
- ^ Duddy, WJ; Nissink WMJ; Allen, Frank H .; Milner-White, E. James (2004). "Mimetismo por asx- e ST-turn dos quatro principais tipos de β-turn nas proteínas" . Protein Science . 13 (11): 3051–3055. doi : 10.1110 / ps.04920904 . PMC 2286581 . PMID 15459339 .
- ^ Thakur, AK; Kishore R (2006). "Caracterização do mimetismo das voltas β e asx-voltas em um peptídeo modelo: Estabilização via interação CH ••• O". Biopolímeros . 81 (6): 440–449. doi : 10.1002 / bip.20441 . PMID 16411188 .
- ^ Duddy, WJ; Nissink WMJ; Allen, Frank H .; Milner-White, E. James (2004). "Mimetismo por asx- e ST-turn dos quatro principais tipos de beta turn nas proteínas" . Protein Science . 13 (11): 3051–3055. doi : 10.1110 / ps.04920904 . PMC 2286581 . PMID 15459339 .
- ^ Doig, AJ; Macarthur MW; MacArthur, Malcolm W .; Thornton, Janet M. (1997). "Estruturas de N-terminais de hélices em proteínas" . Protein Science . 6 (1): 147–155. doi : 10.1002 / pro.5560060117 . PMC 2143508 . PMID 9007987 .
- ^ Presta, LG; Rose GD (1988). "Helix Caps". Ciência . 240 (4859): 1632–1641. Bibcode : 1988Sci ... 240.1632P . doi : 10.1126 / science.2837824 . PMID 2837824 .
- ^ Aurora, R; Rose GD (1998). "Helix Capping" . Protein Science . 7 (1): 21–38. doi : 10.1002 / pro.5560070103 . PMC 2143812 . PMID 9514257 .
- ^ Gunasekaran, K; Nagarajam HA; Ramakrishnan, C; Balaram, P (1998). "Marcas de pontuação estereoquímica na estrutura da proteína". Journal of Molecular Biology . 275 (5): 917–932. doi : 10.1006 / jmbi.1997.1505 . PMID 9480777 . S2CID 35919397 .
- ^ Duddy, WJ; Nissink WMJ; Allen, Frank H .; Milner-White, E. James (2004). "Mimetismo por asx- e ST-turn dos quatro principais tipos de β-turn nas proteínas" . Protein Science . 13 (11): 3051–3055. doi : 10.1110 / ps.04920904 . PMC 2286581 . PMID 15459339 .
- ^ Wan, WY; Milner-White EJ (2009). "Um motivo recorrente de duas ligações de hidrogênio que incorpora um resíduo de serina ou treonina é encontrado tanto em α-helicoidal N Termini como em outras situações". Journal of Molecular Biology . 286 (5): 1651–1662. doi : 10.1006 / jmbi.1999.2551 . PMID 10064721 .
links externos
- ^ Líder, DP; Milner-White EJ (2009). "Proteínas Motivadas: Um aplicativo da web para estudar pequenos motivos de proteínas tridimensionais" . BMC Bioinformatics . 10 : 60. doi : 10.1186 / 1471-2105-10-60 . PMC 2651126 . PMID 19210785 .
- ^ Golovin, A; Henrick K (2008). "MSDmotif: explorando sites de proteínas e motivos" . BMC Bioinformatics . 9 : 312. doi : 10.1186 / 1471-2105-9-312 . PMC 2491636 . PMID 18637174 .