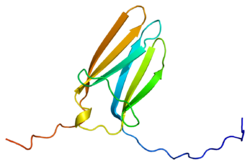
Receptor de tropomiosina quinase C - Tropomyosin receptor kinase C
Tropomiosina receptor quinase C ( TrkC ), também conhecida como receptor do factor de crescimento de NT-3 , neurotrófico tirosina quinase do receptor de tipo 3 , ou TrkC tirosina-quinase é uma proteína que, em seres humanos é codificada pelo NTRK3 gene .
TrkC é o receptor catalítico de alta afinidade para a neurotrofina NT-3 ( neurotrofina-3 ). Como tal, o TrkC medeia os múltiplos efeitos deste fator neurotrófico , que inclui a diferenciação neuronal e a sobrevivência.
O receptor TrkC faz parte da grande família de receptores tirosina quinases . Uma "tirosina quinase " é uma enzima que é capaz de adicionar um grupo fosfato a certas tirosinas nas proteínas alvo, ou "substratos". Um receptor tirosina quinase é uma "tirosina quinase" que está localizada na membrana celular e é ativada pela ligação de um ligante por meio de seu domínio extracelular. Outro exemplo de receptores de tirosina quinase incluem o receptor de insulina , o receptor IGF-1 , o receptor da proteína MuSK , o receptor do fator de crescimento endotelial vascular (VEGF), etc. As proteínas "substrato" que são fosforiladas por TrkC incluem PI3 quinase .
Função
TrkC é o receptor catalítico de alta afinidade para a neurotrofina-3 (também conhecido como NTF3 ou NT-3). Semelhante a outros receptores NTRK e tirosina quinases receptor em geral, a ligação do ligante induz a dimerização do receptor seguida por trans-autofosforilação na tirosina conservada no domínio intracelular (citoplasmático) do receptor. Estas tirosinas conservadas servem como locais de encaixe para proteínas adaptadoras que desencadeiam cascatas de sinalização a jusante. A sinalização por meio de PLCG1 , PI3K e RAAS , a jusante de NTRK3 ativado, regula a sobrevivência, proliferação e motilidade celular
Além disso, o TrkC foi identificado como uma nova molécula de adesão sinaptogênica responsável pelo desenvolvimento de sinapses excitatórias.
O locus TrkC codifica pelo menos oito isoformas, incluindo formas sem o domínio de quinase ou com inserções de quinase adjacentes ao local de autofosforilação principal. Essas formas surgem por eventos de splicing alternativos e são expressas em diferentes tecidos e tipos de células. A ativação de NT-3 da isoforma catalítica de TrkC promove a proliferação de células da crista neural e a diferenciação neuronal. Por outro lado, a ligação de NT-3 à isoforma TrkC não catalítica induz diferenciação neuronal, mas nem proliferação neuronal
Membros da família
Os receptores quinases de tropomiosina, também conhecidos como receptores neurotróficos de tirosina quinase (Trk), desempenham um papel essencial na biologia dos neurônios ao mediar a sinalização ativada por neurotrofina. Existem três receptores transmembrana TrkA , TrkB e TrkC (codificados pelos genes NTRK1, NTRK2 e NTRK3 respectivamente) que compõem a família de receptores Trk. Esta família de receptores é ativada por neurotrofinas, incluindo NGF (para fator de crescimento do nervo ), BDNF (para fator neurotrófico derivado do cérebro ), NT-4 (para neurotrofina-4 ) e NT-3 (para neurotrofina-3). Enquanto o TrkA medeia os efeitos do NGF, o TrkB é ligado e ativado pelo BDNF , NT-4 e NT-3. Além disso, o TrkC se liga e é ativado pelo NT-3. TrkB liga BDNF e NT-4 mais fortemente do que liga NT-3. O TrkC liga o NT-3 mais fortemente do que o TrkB.
Há uma outra família de receptores NT-3 além dos Trks (TrkC e TrkB), chamada de " LNGFR " (para " receptor de fator de crescimento de nervo de baixa afinidade "). Ao contrário do TrkC, o LNGFR desempenha um papel um pouco menos claro na biologia do NT-3 . Alguns pesquisadores mostraram que o LNGFR se liga e serve como um "sumidouro" para as neurotrofinas. As células que expressam os receptores LNGFR e Trk podem, portanto, ter uma maior atividade - uma vez que têm uma maior "microconcentração" da neurotrofina. Também foi demonstrado, no entanto, que o LNGFR pode sinalizar uma célula para morrer por apoptose - portanto, as células que expressam o LNGFR na ausência de receptores Trk podem morrer em vez de viver na presença de uma neurotrofina.
Foi demonstrado que o NTRK3 é um receptor de dependência, ou seja, pode ser capaz de induzir proliferação ao se ligar ao seu ligante NT-3, porém, a ausência do NT-3 resultará na indução de apoptose pelo NTRK3.
Papel na doença
Com o passar dos anos, muitos estudos têm mostrado que a falta ou desregulamentação do TrkC ou do complexo TrkC: NT-3 pode estar associada a diferentes doenças.
Um estudo demonstrou que camundongos com defeito para NT-3 ou TrkC apresentam graves defeitos sensoriais. Esses ratos têm nocicepção normal, mas são defeituosos na propriocepção, a atividade sensorial responsável por localizar os membros no espaço.
A redução da expressão de TrkC foi observada em doenças neurodegenerativas, incluindo Alzheimer (AD), Parkinson (PD) e doenças de Huntington (HD). O papel do NT-3 também foi estudado terapeuticamente em modelos de esclerose lateral amiotrófica ( ELA ) com perda de neurônios motores da medula espinhal que expressam TrkC
Além disso, foi demonstrado que o TrkC desempenha um papel no câncer. A expressão e função dos subtipos Trk dependem do tipo de tumor. Por exemplo, no neuroblastoma, a expressão de TrkC se correlaciona com um bom prognóstico, mas em cânceres de mama, próstata e pâncreas, a expressão do mesmo subtipo de TrkC está associada à progressão do câncer e metástase.
Papel no câncer
Embora originalmente identificada como uma fusão oncogênica em 1982, apenas recentemente houve um interesse renovado na família Trk no que se refere ao seu papel em cânceres humanos devido à identificação de NTRK1 (TrkA), NTRK2 (TrkB) e NTRK3 (TrkC) fusões gênicas e outras alterações oncogênicas em vários tipos de tumor. Vários inibidores de Trk estão (em 2015) em ensaios clínicos e mostraram-se promissores no encolhimento de tumores humanos. A família de receptores de neurotrofina, incluindo NTRK3, demonstrou induzir uma variedade de resposta pleiotórpica em células malignas, incluindo maior capacidade de invasão de células tumorais e quimiotoxia . A expressão aumentada de NTRK3 foi demonstrada no neuroblastoma , no meduloblastoma e em tumores cerebrais neuroectodérmicos .
Metilação NTRK3
A região promotora de NTRK3 contém uma densa ilha CpG localizada relativamente adjacente ao local de início da transcrição (TSS) . Usando matrizes HumanMethylation450 , PCR quantitativo específico de metilação (qMSP) e ensaios Methylight , foi indicado que NTRK3 é metilado em todas as linhas de células CRC e não nas amostras de epitélio normal . À luz de sua metilação preferencial em CRCs e por causa de seu papel como um receptor de neurotrofina, tem sido sugerido ter um papel funcional na formação do câncer colorretal . Também foi sugerido que o estado de metilação do promotor NTRK3 é capaz de discriminar amostras de tumor CRC de tecido livre de tumor adjacente normal. Portanto, pode ser considerado um biomarcador para detecção molecular de CRC, especialmente em combinação com outros marcadores como SEPT9 . NTRK3 também foi indicado como um dos genes no painel de nove sondas de metilação CpG localizadas no promotor ou na região do exon 1 de oito genes (incluindo DDIT3 , FES , FLT3 , SEPT5 , SEPT9, SOX1 , SOX17 e NTRK3) para previsão de prognóstico em pacientes com CCEE (carcinoma epidermóide de esôfago).
Inibidores TrkC (gene NTRK3) em desenvolvimento
Entrectinibe (anteriormente RXDX-101) é um medicamento experimental desenvolvido pela Ignyta, Inc., que possui atividade antitumoral potencial. É um inibidor oral pan-TRK, ALK e ROS1 que demonstrou sua atividade antitumoral em murinos, linhagens de células tumorais humanas e modelos de xenoenxertos derivados de pacientes. In vitro, o entrectinibe inibe os membros da família Trk TrkA, TrkB e TrkC em baixas concentrações de nano molar. É altamente ligado às proteínas plasmáticas (99,5%) e pode se difundir facilmente através da barreira hematoencefálica (BBB).
Entrectinibe foi aprovado pelo FDA em 15 de agosto de 2019 para o tratamento de pacientes adultos e pediátricos com 12 anos de idade ou mais com tumores sólidos que apresentam fusão do gene do receptor de tirosina quinase neurotrófico
Interações
Foi demonstrado que o TrkC interage com:
- SH2B2
- SQSTM1
- KIDINS220
- PTPRS
- MAPK8IP3 / JIP3
- Neurotrofina-3
- TβRII
- DOK5
- BMPRII
- PLCG1
Ligantes
Peptidomiméticos de pequenas moléculas baseados em β-turn NT-3 , com a justificativa de direcionar o domínio extracelular do receptor TrkC, mostraram ser agonistas de TrkC. Estudos posteriores mostraram que os peptidomiméticos com uma estrutura orgânica e um farmacóforo baseado na estrutura NT-3 da volta β também podem funcionar como um antagonista de TrkC.
Referências
Leitura adicional
- Lamballe F, Klein R, Barbacid M (setembro de 1991). "trkC, um novo membro da família trk de proteínas tirosina quinases, é um receptor para neurotrofina-3". Cell . 66 (5): 967–79. doi : 10.1016 / 0092-8674 (91) 90442-2 . PMID 1653651 .
- Tessarollo L, Tsoulfas P, Martin-Zanca D, Gilbert DJ, Jenkins NA, Copeland NG, Parada LF (junho de 1993). "trkC, um receptor para neurotrofina-3, é amplamente expresso no sistema nervoso em desenvolvimento e em tecidos não neuronais". Desenvolvimento . 118 (2): 463–75. PMID 8223273 .
- Klein R, Silos-Santiago I, Smeyne RJ, Lira SA, Brambilla R, Bryant S, et al. (Março de 1994). "A interrupção do gene trkC do receptor da neurotrofina-3 elimina as aferências musculares e resulta em movimentos anormais". Nature . 368 (6468): 249–51. Bibcode : 1994Natur.368..249K . doi : 10.1038 / 368249a0 . PMID 8145824 .
- Ip NY, Stitt TN, Tapley P, Klein R, Glass DJ, Fandl J, et al. (Fevereiro de 1993). "Semelhanças e diferenças na maneira como as neurotrofinas interagem com os receptores Trk em células neuronais e não neuronais". Neuron . 10 (2): 137–49. doi : 10.1016 / 0896-6273 (93) 90306-C . PMID 7679912 .
- Ebendal T (agosto de 1992). "Função e evolução na família NGF e seus receptores". Journal of Neuroscience Research . 32 (4): 461–70. doi : 10.1002 / jnr.490320402 . PMID 1326636 .
- Guiton M, Gunn-Moore FJ, Glass DJ, Geis DR, Yancopoulos GD, Tavaré JM (setembro de 1995). "As inserções de tirosina quinase de ocorrência natural bloqueiam a ligação de alta afinidade da fosfolipase C gama e Shc à sinalização de TrkC e neurotrofina-3" . The Journal of Biological Chemistry . 270 (35): 20384–90. doi : 10.1074 / jbc.270.35.20384 . PMID 7657612 .
- Shelton DL, Sutherland J, Gripp J, Camerato T, Armanini MP, Phillips HS, et al. (Janeiro de 1995). "Trks humanos: clonagem molecular, distribuição em tecidos e expressão de imunoadesinas de domínio extracelular" . The Journal of Neuroscience . 15 (1 Pt 2): 477–91. doi : 10.1523 / JNEUROSCI.15-01-00477.1995 . PMC 6578290 . PMID 7823156 .
- Pflug BR, Dionne C, Kaplan DR, Lynch J, Djakiew D (janeiro de 1995). "Expressão de um receptor de fator de crescimento de nervo de alta afinidade Trk na próstata humana". Endocrinology . 136 (1): 262–8. doi : 10.1210 / en.136.1.262 . PMID 7828539 .
- Lamballe F, Tapley P, Barbacid M (agosto de 1993). "trkC codifica múltiplos receptores de neurotrofina-3 com propriedades biológicas distintas e especificidades de substrato" . The EMBO Journal . 12 (8): 3083–94. doi : 10.1002 / j.1460-2075.1993.tb05977.x . PMC 413573 . PMID 8344249 .
- Andersson B, Wentland MA, Ricafrente JY, Liu W, Gibbs RA (abril de 1996). "Um método de" adaptador duplo "para melhorar a construção da biblioteca shotgun". Analytical Biochemistry . 236 (1): 107–13. doi : 10.1006 / abio.1996.0138 . PMID 8619474 .
- Yamamoto M, Sobue G, Yamamoto K, Terao S, Mitsuma T (agosto de 1996). "Expressão de mRNAs para fatores neurotróficos (NGF, BDNF, NT-3 e GDNF) e seus receptores (p75NGFR, trkA, trkB e trkC) no sistema nervoso periférico humano adulto e tecidos não neurais". Neurochemical Research . 21 (8): 929–38. doi : 10.1007 / BF02532343 . PMID 8895847 .
- Yu W, Andersson B, Worley KC, Muzny DM, Ding Y, Liu W, et al. (Abril de 1997). "Sequenciação de cDNA de concatenação em grande escala" . Genome Research . 7 (4): 353–8. doi : 10.1101 / gr.7.4.353 . PMC 139146 . PMID 9110174 .
- Valent A, Danglot G, Bernheim A (1997). "Mapeamento dos receptores de tirosina quinase trkA (NTRK1), trkB (NTRK2) e trkC (NTRK3) para cromossomos humanos 1q22, 9q22 e 15q25 por hibridização fluorescente in situ". European Journal of Human Genetics . 5 (2): 102–4. doi : 10.1159 / 000484742 . PMID 9195161 .
- Terenghi G, Mann D, Kopelman PG, Anand P (maio de 1997). "A expressão de trkA e trkC está aumentada na pele diabética humana". Cartas de neurociência . 228 (1): 33–6. doi : 10.1016 / S0304-3940 (97) 00350-9 . PMID 9197281 .
- Knezevich SR, McFadden DE, Tao W, Lim JF, Sorensen PH (fevereiro de 1998). "A novel ETV6-NTRK3 gene fusion in congenital fibrosarcoma". Nature Genetics . 18 (2): 184–7. doi : 10.1038 / ng0298-184 . PMID 9462753 .
- Urfer R, Tsoulfas P, O'Connell L, Hongo JA, Zhao W, Presta LG (março de 1998). "Mapeamento de alta resolução do sítio de ligação de TrkA para fator de crescimento de nervo e TrkC para neurotrofina-3 no segundo domínio semelhante a imunoglobulina dos receptores Trk" . The Journal of Biological Chemistry . 273 (10): 5829–40. doi : 10.1074 / jbc.273.10.5829 . PMID 9488719 .
- Hu YQ, Koo PH (julho de 1998). "Inibição de fosforilação de TrkB e TrkC e sua transdução de sinal por alfa2-macroglobulina" . Journal of Neurochemistry . 71 (1): 213–20. doi : 10.1046 / j.1471-4159.1998.71010213.x . PMID 9648868 .
- Ichaso N, Rodriguez RE, Martin-Zanca D, Gonzalez-Sarmiento R (outubro de 1998). "Caracterização genômica do gene trkC humano" . Oncogene . 17 (14): 1871–5. doi : 10.1038 / sj.onc.1202100 . PMID 9778053 .
- Qian X, Riccio A, Zhang Y, Ginty DD (novembro de 1998). "Identificação e caracterização de novos substratos de receptores Trk em neurônios em desenvolvimento" . Neuron . 21 (5): 1017–29. doi : 10.1016 / S0896-6273 (00) 80620-0 . PMID 9856458 .
- Bibel M, Hoppe E, Barde YA (fevereiro de 1999). "Interações bioquímicas e funcionais entre os receptores de neurotrofina trk e p75NTR" . The EMBO Journal . 18 (3): 616–22. doi : 10.1093 / emboj / 18.3.616 . PMC 1171154 . PMID 9927421 .
- Labouyrie E, Dubus P, Groppi A, Mahon FX, Ferrer J, Parrens M, et al. (Fevereiro de 1999). "Expressão de neurotrofinas e seus receptores na medula óssea humana" . The American Journal of Pathology . 154 (2): 405–15. doi : 10.1016 / s0002-9440 (10) 65287-x . PMC 1849993 . PMID 10027399 .