Haleto de arila - Aryl halide
Em química orgânica , um haleto de arila (também conhecido como haloareno ) é um composto aromático no qual um ou mais átomos de hidrogênio, diretamente ligados a um anel aromático, são substituídos por um haleto . Os haloarenos são diferentes dos haloalcanos porque apresentam muitas diferenças nos métodos de preparação e nas propriedades. Os membros mais importantes são os cloretos de arila, mas a classe de compostos é tão ampla que existem muitos derivados e aplicações.
Preparação
As duas principais rotas preparatórias para halogenetos de arila são halogenação direta e via sais de diazônio.
Halogenação direta
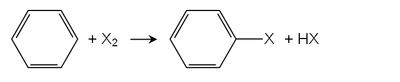
Na halogenação de Friedel-Crafts , os ácidos de Lewis atuam como catalisadores. Muitos cloretos de metal são usados, exemplos incluem cloreto de ferro (III) ou cloreto de alumínio . O haleto de arila mais importante, o clorobenzeno , é produzido por essa rota. A monocloração do benzeno é sempre acompanhada pela formação dos derivados de diclorobenzeno.
Arenes com grupos doadores de elétrons reagem com halogênios mesmo na ausência de ácidos de Lewis. Por exemplo, fenóis e anilinas reagem rapidamente com cloro e água de bromo para dar vários produtos halogenados. A descoloração da água de bromo por arenos ricos em elétrons é usada no teste de bromo .
A halogenação direta de arenos é possível na presença de luz ou em alta temperatura. Para derivados de alquilbenzeno, as posições alquil tendem a ser halogenadas primeiro na halogenação de radical livre. Para halogenar o anel, os ácidos de Lewis são necessários e a luz deve ser excluída para evitar a reação competitiva.
Reações de Sandmeyer, Balz-Schiemann e Gattermann
A segunda rota principal é a reação de Sandmeyer . As anilinas ( arilaminas ) são convertidas em seus sais de diazônio usando ácido nitroso . Por exemplo, o cloreto de cobre (I) converte os sais de diazônio em cloreto de arila. O nitrogênio gasoso é o grupo de saída, o que torna essa reação muito favorável. A reação de Schiemann semelhante usa o ânion tetrafluoroborato como doador de flúor. A reação Gatterman também pode ser usada para converter o sal de diazônio em clorobenzeno ou bromobenzeno, usando pó de cobre em vez de cloreto de cobre ou brometo de cobre. Mas isso deve ser feito na presença de HCl e HBr, respectivamente.
Halogenetos de arila na natureza
Os halogenetos de arila ocorrem amplamente na natureza, mais comumente produzidos por organismos marinhos que utilizam o cloreto e o brometo nas águas oceânicas. Os compostos aromáticos clorados e bromados também são numerosos, por exemplo, derivados de tirosina, triptofano e vários derivados de pirrol. Alguns destes halogenetos de arilo de ocorrência natural exibem propriedades medicinais úteis.

Tendências estruturais
As distâncias CX para haletos de arila seguem a tendência esperada. Estas distâncias para fluorobenzeno, clorobenzeno, bromobenzeno e 4-iodobenzoato de metila são 135,6 (4), 173,90 (23), 189,8 (1) e 209,9 pm , respectivamente.
Reações
Substituição
Ao contrário dos halogenetos de alquil típicos, os halogenetos de aril normalmente não participam das reações de substituição convencionais. Arilo halogenetos com grupos removedores de electrões nas orto e para- posições, pode submeter-se a S N Ar reacções. Por exemplo, 2,4-dinitroclorobenzeno reage em solução básica para dar um fenol:
Ao contrário da maioria das outras reações de substituição, o flúor é o melhor grupo de saída e o iodeto o pior. Um artigo de 2018 indica que esta situação pode realmente ser bastante comum, ocorrendo em sistemas que antes eram assumidos para proceder por meio de mecanismos S N Ar.
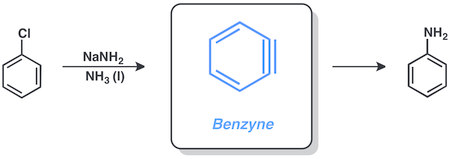
Benzyne
Os halogenetos de arila freqüentemente reagem por intermédio dos benzinos . O clorobenzeno e a amida sódica reagem na amônia líquida para dar anilina por essa via.
Formação de reagente organometálico
Os haletos de arila reagem com metais, geralmente lítio ou magnésio , para dar mais derivados organometálicos que funcionam como fontes de ânions de arila. Pela reação de troca de metal-halogênio , haletos de arila são convertidos em compostos de aril-lítio. Ilustrativo é a preparação de fenil-lítio a partir de bromobenzeno usando butil-lítio (BuLi):
- C 6 H 5 Br + BuLi → C 6 H 5 Li + BuBr
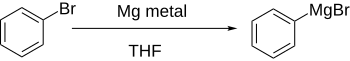
A formação direta de reagentes de Grignard , pela adição de magnésio ao haleto de arila em uma solução etérea, funciona bem se o anel aromático não for significativamente desativado por grupos de retirada de elétrons.
Outras reações
Os haletos podem ser substituídos por nucleófilos fortes por meio de reações envolvendo ânions radicais. Alternativamente, haletos de arila, especialmente os brometos e iodetos, sofrem adição oxidativa e, portanto, estão sujeitos a reações do tipo de aminação de Buchwald-Hartwig .
O clorobenzeno já foi o precursor do fenol , que agora é feito pela oxidação do cumeno . Em altas temperaturas, os grupos arila reagem com a amônia para dar anilinas.
Biodegradação
Rhodococcus phenolicus é uma bactéria que degrada o diclorobenzeno como única fonte de carbono.
Formulários
Os halogenetos de arila produzidos em maior escala são clorobenzeno e os isômeros de diclorobenzeno. Uma aplicação principal, mas descontinuada, foi o uso de clorobenzeno como solvente para dispersar o herbicida Lasso. No geral, a produção de cloretos de arila (também derivados de naftila) vem diminuindo desde a década de 1980, em parte devido a preocupações ambientais. A trifenilfosfina é produzida a partir do clorobenzeno:
- 3 C 6 H 5 Cl + PCl 3 + 6 Na → P (C 6 H 5 ) 3 + 6 NaCl
Os brometos de arila são amplamente usados como retardadores de fogo. O membro mais proeminente é o tetrabromobisfenol-A , que é preparado por bromação direta do difenol.