Glicerol-3-fosfato desidrogenase - Glycerol-3-phosphate dehydrogenase
| Glicerol-3-fosfato desidrogenase (NAD + ) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Estrutura cristalográfica da glicerol-3-fosfato desidrogenase humana 1.
| |||||||||
| Identificadores | |||||||||
| EC nº | 1.1.1.8 | ||||||||
| CAS no. | 9075-65-4 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
| Glicerol-3-fosfato desidrogenase (quinona) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| EC nº | 1.1.5.3 | ||||||||
| CAS no. | 9001-49-4 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| Terminal N de glicerol-3-fosfato desidrogenase dependente de NAD | |||||||||
|---|---|---|---|---|---|---|---|---|---|
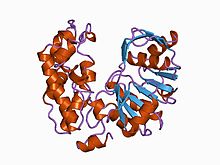 estrutura cristalina da n- (1-d-carboxiletil) -l-norvalina desidrogenase de arthrobacter sp. cepa 1c
| |||||||||
| Identificadores | |||||||||
| Símbolo | NAD_Gly3P_dh_N | ||||||||
| Pfam | PF01210 | ||||||||
| Clã Pfam | CL0063 | ||||||||
| InterPro | IPR011128 | ||||||||
| PRÓSITO | PDOC00740 | ||||||||
| SCOP2 | 1m66 / SCOPe / SUPFAM | ||||||||
| |||||||||
| Terminal C de glicerol-3-fosfato desidrogenase dependente de NAD | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 estrutura da glicerol-3-fosfato desidrogenase de archaeoglobus fulgidus
| |||||||||
| Identificadores | |||||||||
| Símbolo | NAD_Gly3P_dh_C | ||||||||
| Pfam | PF07479 | ||||||||
| Clã Pfam | CL0106 | ||||||||
| InterPro | IPR006109 | ||||||||
| PRÓSITO | PDOC00740 | ||||||||
| SCOP2 | 1m66 / SCOPe / SUPFAM | ||||||||
| |||||||||
Glicerol-3-fosfato desidrogenase ( GPDH ) é uma enzima que catalisa a conversão redox reversível de fosfato de dihidroxiacetona (também conhecido como fosfato de glicerona, desatualizado) em sn- glicerol 3-fosfato .
A glicerol-3-fosfato desidrogenase atua como um elo principal entre o metabolismo de carboidratos e o metabolismo de lipídeos . É também um grande contribuidor de elétrons para a cadeia de transporte de elétrons na mitocôndria .
Termos mais antigos para glicerol-3-fosfato desidrogenase incluem alfa glicerol-3-fosfato desidrogenase (alfaGPDH) e glicerolfosfato desidrogenase (GPDH). No entanto, a glicerol-3-fosfato desidrogenase não é o mesmo que a gliceraldeído 3-fosfato desidrogenase (GAPDH), cujo substrato é um aldeído e não um álcool .
Função metabólica
O GPDH desempenha um papel importante na biossíntese de lipídios . Através da redução do fosfato de dihidroxiacetona em glicerol 3-fosfato , o GPDH permite a imediata desfosforilação do glicerol 3-fosfato em glicerol . Além disso, o GPDH é uma das enzimas envolvidas na manutenção do potencial redox através da membrana mitocondrial interna .
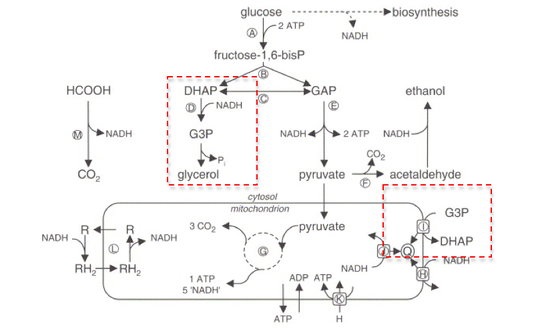
Reação
O par de coenzimas NAD + / NADH atua como um reservatório de elétrons para as reações redox metabólicas , transportando elétrons de uma reação para outra. A maioria dessas reações do metabolismo ocorre na mitocôndria . Para regenerar o NAD + para uso posterior, os pools de NADH no citosol devem ser reoxidados. Uma vez que a membrana mitocondrial interna é impermeável ao NADH e ao NAD + , eles não podem ser trocados livremente entre o citosol e a matriz mitocondrial .
Uma maneira de transportar este equivalente de redução através da membrana é através da lançadeira de Glicerol-3-fosfato , que emprega as duas formas de GPDH:
- O GPDH citosólico, ou GPD1, está localizado na membrana externa da mitocôndria voltada para o citosol e catalisa a redução do fosfato de diidroxiacetona em glicerol-3-fosfato .
- Em conjunto, o GPDH mitocondrial, ou GPD2, está embutido na superfície externa da membrana mitocondrial interna , negligenciando o citosol e catalisa a oxidação do glicerol-3-fosfato em fosfato de dihidroxiacetona .
As reações catalisadas por GPDH citosólico (solúvel) e mitocondrial são as seguintes:
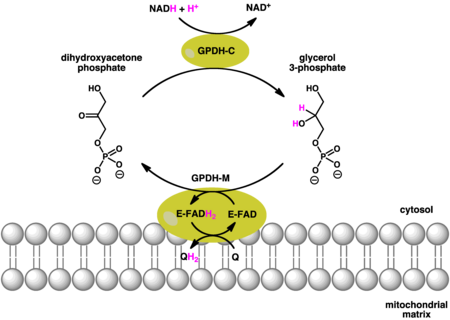
Reações acopladas catalisadas pelas formas citosólica (GPDH-C) e mitocondrial (GPDH-M) da glicerol 3-fosfato desidrogenase. GPDH-C e GPDH-M usam NADH e quinol (QH) como doadores de elétrons, respectivamente. Além disso, o GPDH-M usa FAD como cofator.
|
Variantes
Existem duas formas de GPDH:
| Enzima | Proteína | Gene | |||||
|---|---|---|---|---|---|---|---|
| Número CE | Nome | Doador / Aceitante | Nome | Localização subcelular | Abreviação | Nome | Símbolo |
| 1.1.1.8 | glicerol-3-fosfato desidrogenase | NADH / NAD + | Glicerol-3-fosfato desidrogenase [NAD + ] | citoplasmático | GPDH-C | glicerol-3-fosfato desidrogenase 1 (solúvel) | GPD1 |
| 1.1.5.3 | glicerol-3-fosfato desidrogenase | quinol / quinona | Glicerol-3-fosfato desidrogenase | mitocondrial | GPDH-M | glicerol-3-fosfato desidrogenase 2 (mitocondrial) | GPD2 |
Os seguintes genes humanos codificam proteínas com atividade enzimática GPDH:
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
GPD1
A glicerol-3-fosfato desidrogenase citosólica (GPD1) é uma enzima dependente de NAD + que reduz o fosfato de dihidroxiacetona a glicerol-3-fosfato . Simultaneamente, o NADH é oxidado a NAD + na seguinte reação:
Como resultado, o NAD + é regenerado para atividade metabólica adicional.
GPD1 consiste em duas subunidades e reage com fosfato de dihidroxiacetona e NAD + por meio da seguinte interação:
Figura 4. O site ativo putativo. O grupo fosfato de DHAP é meio circundado pela cadeia lateral de Arg269 e interage com Arg269 e Gly268 diretamente por ligações de hidrogênio (não mostrado). Os resíduos conservados Lys204, Asn205, Asp260 e Thr264 formam uma rede de ligações de hidrogênio estável. A outra rede de ligações de hidrogênio inclui resíduos Lys120 e Asp260, bem como uma molécula de água ordenada (com um fator B de 16,4 Å2), que se liga a Gly149 e Asn151 (não mostrado). Nessas duas redes eletrostáticas, apenas o grupo ε-NH 3 + de Lys204 é o mais próximo do átomo C2 de DHAP (3,4 Å).
GPD2
Glicerol-3-fosfato desidrogenase mitocondrial (GPD2), catalisa a oxidação irreversível do glicerol-3-fosfato em fosfato de diidroxiacetona e, concomitantemente, transfere dois elétrons do FAD para a cadeia de transporte de elétrons . GPD2 consiste em 4 subunidades idênticas.
Resposta a tensões ambientais
- Estudos indicam que o GPDH não é afetado principalmente pelas mudanças de pH : nem o GPD1 nem o GPD2 são favorecidos em certas condições de pH .
- Em altas concentrações de sal (por exemplo, NaCl ), a atividade do GPD1 é aumentada em relação ao GPD2, uma vez que um aumento na salinidade do meio leva a um acúmulo de glicerol em resposta.
- As mudanças na temperatura não parecem favorecer nem GPD1 nem GPD2.
Lançadeira de glicerol-3-fosfato
O citosólico junto com a mitocondrial glicerol-3-fosfato desidrogenase atuam em conjunto. A oxidação do NADH citoplasmático pela forma citosólica da enzima cria glicerol-3-fosfato a partir do fosfato de dihidroxiacetona. Uma vez que o glicerol-3-fosfato se moveu através da membrana mitocondrial externa, ele pode ser oxidado por uma isoforma separada de glicerol-3-fosfato desidrogenase que usa quinona como oxidante e FAD como cofator. Como resultado, há uma perda líquida de energia, comparável a uma molécula de ATP.
A ação combinada dessas enzimas mantém a relação NAD + / NADH que permite a operação contínua do metabolismo.
Papel na doença
O papel fundamental do PIBH na manutenção do potencial NAD + / NADH , assim como seu papel no metabolismo lipídico , torna o PIBH um fator em doenças com desequilíbrio lipídico, como a obesidade .
- A atividade intensificada de GPDH, particularmente GPD2, leva a um aumento na produção de glicerol . Como o glicerol é uma subunidade principal no metabolismo lipídico , sua abundância pode facilmente levar a um aumento no acúmulo de triglicerídeos em nível celular. Como resultado, há uma tendência à formação de tecido adiposo levando ao acúmulo de gordura que favorece a obesidade .
- GPDH também desempenha um papel na síndrome de Brugada . Foi comprovado que mutações no gene que codifica GPD1 causam defeitos na cadeia de transporte de elétrons . Acredita-se que esse conflito com os níveis de NAD + / NADH na célula contribua para defeitos na regulação do canal iônico de sódio cardíaco e possa levar a uma arritmia letal durante a infância.
Alvo farmacológico
Acredita-se que a isoforma mitocondrial da G3P desidrogenase seja inibida pela metformina , um medicamento de primeira linha para o diabetes tipo 2 .
Pesquisa Biológica
Sarcophaga barbata foi usado para estudar a oxidação do L-3-glicerofosfato na mitocôndria. Verificou-se que o L-3-glicerofosfato não entra na matriz mitocondrial, ao contrário do piruvato. Isso ajuda a localizar a L-3-glicerofosfato-flavoproteína oxidoredutase, que está na membrana interna da mitocôndria.
Estrutura
A glicerol-3-fosfato desidrogenase consiste em dois domínios proteicos . O domínio N-terminal é um domínio de ligação NAD , e o C-terminal atua como um domínio de ligação ao substrato. No entanto, resíduos de interface de dímero e tetrâmero estão envolvidos na ligação de GAPDH-RNA, uma vez que GAPDH pode exibir várias atividades clandestinas, incluindo a modulação da ligação de RNA e / ou estabilidade.
Veja também
- páginas de substrato: glicerol 3-fosfato , dihidroxiacetona fosfato
- tópicos relacionados: transporte de fosfato de glicerol , creatina quinase , glicólise , gliconeogênese
Referências
Leitura adicional
- Baranowski T (1963). "α-Glicerofosfato desidrogenase". Em Boyer PD, Lardy H, Myrbäck K (eds.). The Enzymes (2ª ed.). Nova York: Academic Press. pp. 85–96.
- Brosemer RW, Kuhn RW (maio de 1969). "Propriedades estruturais comparativas das desidrogenases alfa-glicerofosfato de abelha e coelho". Bioquímica . 8 (5): 2095–105. doi : 10.1021 / bi00833a047 . PMID 4307630 .
- O'Brien SJ, MacIntyre RJ (outubro de 1972). "O ciclo do glicerofosfato em Drosophila melanogaster. I. Aspectos bioquímicos e de desenvolvimento". Biochemical Genetics . 7 (2): 141–61. doi : 10.1007 / BF00486085 . PMID 4340553 . S2CID 22009695 .
- Warkentin DL, Fondy TP (julho de 1973). "Isolamento e caracterização da L-glicerol-3-fosfato desidrogenase citoplasmática do tecido adiposo renal de coelho e sua comparação com a enzima do músculo esquelético" . European Journal of Biochemistry / FEBS . 36 (1): 97–109. doi : 10.1111 / j.1432-1033.1973.tb02889.x . PMID 4200180 .
- Albertyn J, van Tonder A, Prior BA (agosto de 1992). "Purificação e caracterização de glicerol-3-fosfato desidrogenase de Saccharomyces cerevisiae" . FEBS Letters . 308 (2): 130–2. doi : 10.1016 / 0014-5793 (92) 81259-O . PMID 1499720 . S2CID 39643279 .
- Koekemoer TC, Litthauer D, Oelofsen W (junho de 1995). "Isolamento e caracterização da glicerol-3-fosfato desidrogenase do tecido adiposo". The International Journal of Biochemistry & Cell Biology . 27 (6): 625–32. doi : 10.1016 / 1357-2725 (95) 00012-E . PMID 7671141 .
- Påhlman IL, Larsson C, Averét N, Bunoust O, Boubekeur S, Gustafsson L, Rigoulet M (agosto de 2002). "Regulação cinética da mitocondrial glicerol-3-fosfato desidrogenase pela NADH desidrogenase externa em Saccharomyces cerevisiae" . The Journal of Biological Chemistry . 277 (31): 27991–5. doi : 10.1074 / jbc.M204079200 . PMID 12032156 .
- Overkamp KM, Bakker BM, Kötter P, van Tuijl A, de Vries S, van Dijken JP, Pronk JT (maio de 2000). "Análise in vivo dos mecanismos de oxidação do NADH citosólico pelas mitocôndrias de Saccharomyces cerevisiae" . Journal of Bacteriology . 182 (10): 2823–30. CiteSeerX 10.1.1.335.5313 . doi : 10.1128 / JB.182.10.2823-2830.2000 . PMC 101991 . PMID 10781551 .
- Dawson AG, Cooney GJ (julho de 1978). "Reconstrução da lançadeira alfa-glicerolfosfato usando mitocôndrias de rim de rato" . FEBS Letters . 91 (2): 169–72. doi : 10.1016 / 0014-5793 (78) 81164-8 . PMID 210038 .
- Opperdoes FR, Borst P, Bakker S, Leene W (junho de 1977). "Localização de glicerol-3-fosfato oxidase na mitocôndria e particulado NAD + -ligado glicerol-3-fosfato desidrogenase nos micro-corpos da corrente sanguínea forma para Trypanosoma brucei". European Journal of Biochemistry / FEBS . 76 (1): 29–39. doi : 10.1111 / j.1432-1033.1977.tb11567.x . PMID 142010 .
- Eswaramoorthy S, Bonanno JB, Burley SK, Swaminathan S (junho de 2006). "Mecanismo de ação de uma monooxigenase contendo flavina" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 103 (26): 9832–7. Bibcode : 2006PNAS..103.9832E . doi : 10.1073 / pnas.0602398103 . PMC 1502539 . PMID 16777962 .
links externos
- entradas equivalentes:
- alphaGPDH nos cabeçalhos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)
- GPDH
- Termo GO do banco de dados do genoma de levedura: GPDH


