Adsorção supercrítica - Supercritical adsorption
Adsorção supercrítica, também conhecida como adsorção de fluidos supercríticos , é a adsorção em temperaturas acima do crítico. Existem diferentes entendimentos tácitos de fluidos supercríticos. Por exemplo, “um fluido é considerado 'supercrítico' quando sua temperatura e pressão excedem a temperatura e pressão no ponto crítico”. Nos estudos de extração supercrítica, entretanto, “fluido supercrítico” é aplicado para uma região estreita de temperatura de 1-1,2 ou a +10 K, que é chamada de região supercrítica. ( é a temperatura crítica)
História
Observações de adsorção supercrítica relatadas antes de 1930 foram cobertas em estudos por McBain e Britton. Todos os artigos importantes sobre o assunto publicados entre 1930 e 1966 foram revisados por Menon. Durante os últimos 20 anos, observou-se um crescente interesse na pesquisa de adsorção supercrítica sob o impulso da busca por combustíveis alternativos limpos . Um progresso considerável foi feito em ambas as técnicas de medição de adsorção e simulação molecular de adsorção em computadores, gerando novos insights sobre a natureza da adsorção supercrítica.
Propriedades
De acordo com o comportamento de adsorção, a adsorção de gases em sólidos pode ser classificada em três faixas de temperatura relativas a :
1. Região subcrítica (T < )
2. Região quase crítica ( <T < +10)
3. A região T> +10
Isotérmicas na primeira região mostrarão a característica de adsorção subcrítica. Isotérmicas na segunda região mostrarão a característica de transição do mecanismo. Isotermas na terceira região mostrarão a característica de adsorção supercrítica. A transição será contínua se as isotermas em ambos os lados da temperatura crítica pertencerem ao mesmo tipo, como a adsorção em carvão ativado microporoso . No entanto, a transição descontínua pode ser observada nas isotermas da segunda região se houver uma transformação dos tipos de isotermas, como a adsorção em sílica gel mesoporosa . O fator decisivo em tal classificação de adsorção é apenas a temperatura, independentemente da pressão. Isso ocorre porque um fluido não pode passar por uma transição para uma fase líquida em temperatura acima da crítica, independentemente da pressão aplicada. Esta lei fundamental determina os diferentes mecanismos de adsorção para as regiões subcríticas e supercríticas. Para a região subcrítica, a pressão de equilíbrio de adsorção mais elevada é a pressão de saturação do adsorbato . Além de acontecer condensação. O adsorbato na fase adsorvida está em grande parte no estado líquido, com base no qual diferentes teorias de adsorção e termodinâmica, bem como suas aplicações, foram desenvolvidas. Para a região supercrítica, a condensação não pode acontecer, não importa quão grande seja a pressão.
Aquisição de isotérmicas de adsorção supercríticas
Uma isoterma de adsorção representa a relação entre a quantidade de adsorvato e a pressão da fase em massa (ou densidade) em equilíbrio para uma temperatura constante. É um conjunto de dados de equilíbrio de adsorção especificado. Esses dados de equilíbrio são necessários para um projeto ideal de processo baseado na adsorção e são considerados informações fundamentais para estudos teóricos.
Medição do equilíbrio de adsorção gás-sólido
Método volumétrico
O método volumétrico foi usado nos primeiros dias dos estudos de adsorção por Langmuir, Dubinin e outros. Basicamente, compreende um processo de expansão de gás de um recipiente de armazenamento (célula de referência) para uma câmara de adsorção incluindo adsorvente (célula de adsorção) através de uma válvula de controle C, conforme esquematicamente mostrado na Figura 1. A célula de referência com volume é mantida a uma temperatura constante . O valor de inclui o volume do tubo entre a célula de referência e a válvula C. A célula de adsorção é mantida na temperatura de equilíbrio especificada . O volume do tubo de conexão entre a célula de adsorção e a válvula é dividido em duas partes: uma parte com volume com a mesma temperatura da célula de referência. A outra parte está enterrada em uma atmosfera de temperatura . Seu volume é adicionado ao volume da célula de adsorção .
A quantidade adsorvida pode ser calculada a partir das leituras de pressão antes e depois de abrir a válvula C com base na relação pVT de gases reais. Uma amostra de adsorvente seca e desgaseificada de peso conhecido foi incluída na célula de adsorção. Uma quantidade de gás é deixada entrar para manter a pressão . Os moles de gás confinados são calculados como:
A pressão cai para depois da válvula de abertura C. A quantidade de gás mantida em , e são respectivamente:
A quantidade adsorvida ou o excesso de adsorção de N é então obtido:
onde e são os moles do gás remanescente dentro e antes da abertura da válvula C. Todos os valores do fator de compressibilidade são calculados por uma equação de estado apropriada, que pode gerar valores z apropriados para temperaturas não próximas à zona crítica.
As principais vantagens desse método são a simplicidade do procedimento, a disponibilidade comercial de instrumentos e as grandes faixas de pressão e temperatura nas quais esse método pode ser realizado. A desvantagem das medições volumétricas é a quantidade considerável de amostra adsorvente necessária para superar os efeitos da adsorção nas paredes dos vasos. Porém, este pode ser um aspecto positivo se a amostra for adequada. Uma quantidade maior de amostra resulta em adsorção considerável e geralmente fornece um espaço vazio maior na célula de adsorção, reduzindo ao mínimo o efeito da incerteza no “espaço morto”.
Método gravimétrico
No método gravimétrico, a mudança de peso da amostra adsorvente no campo gravimétrico devido à adsorção da fase gasosa é registrada. Vários tipos de microbalança sensível foram desenvolvidos para esse propósito. Uma técnica gravimétrica de fluxo contínuo associada à retificação wavelet permite maior precisão, especialmente na região quase crítica.
As principais vantagens do método gravimétrico incluem sensibilidade, precisão e a possibilidade de verificar o estado de ativação de uma amostra adsorvente. No entanto, deve-se considerar a correção da flutuabilidade na medição gravimétrica. Uma contraparte é usada para este propósito. A amostra sólida é colocada em um porta-amostras em um braço da microbalança enquanto a contraparte é carregada no outro braço. Deve-se ter cuidado para manter o volume da amostra e da contraparte o mais próximo possível para reduzir o efeito de flutuabilidade. O sistema é aspirado e a balança é zerada antes de iniciar os experimentos. A flutuabilidade é medida pela introdução de hélio e pressurização até a pressão mais alta do experimento. Supõe-se que o hélio não se adsorve e qualquer mudança de peso (ΔW) é devido à flutuabilidade. Conhecendo a densidade do hélio ( ), pode-se determinar a diferença de volume (ΔV) entre a amostra e a contraparte:
O peso medido pode ser corrigido para o efeito de flutuabilidade a uma temperatura e pressão especificadas:
é a leitura do peso antes da correção.
Geração de isotérmicas por simulação molecular de adsorção
As abordagens de Monte Carlo e dinâmica molecular tornaram-se ferramentas úteis para cálculos teóricos com o objetivo de predições de equilíbrios de adsorção e difusividades em pequenos poros de várias geometrias simples. As interações entre as moléculas de adsorvato são representadas pelo potencial Lenard-Jones:
onde r é a distância entre as partículas, é o ponto em que o potencial é zero e é a profundidade do poço.
Isotermas experimentais da região supercrítica
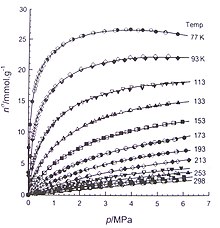
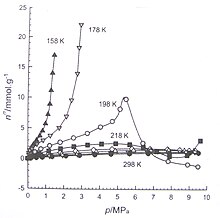
Li Zhou e colegas de trabalho usaram um aparelho volumétrico para medir o equilíbrio de adsorção de hidrogênio e metano em carvão ativado (Figura 2, 3). Eles também medem o equilíbrio de adsorção de nitrogênio em carvão ativado microporoso (Figura 4) e em um gel de sílica mesoporoso (Figura 5) para a região subcrítica e supercrítica. A Figura 6 mostra as isotermas de metano em sílica gel.
Problemas futuros
A adsorção de fluido em temperaturas acima do crítico e pressões elevadas é um campo de crescente importância na ciência e na engenharia. É a base físico-química de muitos processos de engenharia e potenciais aplicações industriais. Por exemplo, separação ou purificação de hidrocarbonetos leves, armazenamento de gases combustíveis em sólidos microporosos, adsorção de gases supercríticos em processos de extração e cromatografia. Além disso, o conhecimento do fenômeno da interface gás / sólido em altas pressões é fundamental para a catálise heterogênea. No entanto, o número limitado de dados confiáveis de adsorção de alta pressão dificultou o progresso do estudo teórico.
Pelo menos dois problemas precisam ser resolvidos antes que um sistema consistente de teorias para adsorção supercrítica se torne sofisticado: primeiro, como estabelecer um estado termodinamicamente padrão para a fase adsorvida supercrítica, de modo que o potencial de adsorção para adsorção supercrítica possa ser avaliado? Em segundo lugar, como determinar a quantidade total na fase adsorvida com base em dados de equilíbrio medidos experimentalmente. A determinação da adsorção absoluta é necessária para estabelecer a teoria termodinâmica porque, como um reflexo do comportamento estatístico das moléculas, as regras termodinâmicas devem se basear no total, e não em parte, do material confinado no sistema estudado.
A partir de estudos recentes de adsorção supercrítica, parece haver um fim na direção de alta pressão para a adsorção supercrítica. No entanto, a densidade de fase adsorvida é o fator decisivo para a existência desta extremidade. O estado de adsorbato no “final” fornece o estado padrão da fase adsorvida supercrítica assim como o líquido saturado, que é o estado final do adsorbato na adsorção subcrítica. Portanto, o “estado final” deve ser definido com precisão. Para estabelecer uma relação definitiva para a densidade de fase adsorvida no estado final, dados experimentais abundantes e confiáveis ainda são necessários.
Referências
- József Tóth (2002). Adsorção: Teoria, Modelagem e Análise. CRC Press ISBN 0-8247-0747-8 , ISBN 978-0-8247-0747-7
- Jyh-Ping Hsu (1999). Forças e campos interfaciais: teoria e aplicações. CRC Press ISBN 0-8247-1964-6 , ISBN 978-0-8247-1964-7
- Eldred H. Chimowitz (2005). Introdução aos fenômenos críticos em fluidos. Oxford University Press US ISBN 0-19-511930-4 , ISBN 978-0-19-511930-5
- Jacques P. Fraissard, Curt W. Conner (1997). Adsorção física: experimento, teoria e aplicações. Springer ISBN 0-7923-4547-9 , ISBN 978-0-7923-4547-3
- Li Zhou (2006). Progresso de adsorção em pesquisa fundamental e de aplicação. World Scientific ISBN 978-981-277-025-7
- Y Zhou, Y Sun, L Zhou. Um estudo experimental sobre o comportamento de adsorção de gases ao cruzar a temperatura crítica. A 7ª Conferência Internacional sobre Fundamentos de Adsorção, Nagasaki, 2001
- Peng B, Yu YX, A Teoria Funcional de Densidade para Fluidos de Lennard-Jones em Poros Cilíndricos e Suas Aplicações à Adsorção de Nitrogênio em Materiais MCM-41. Langmuir, 24 (2008) 12431-12439
- Estella J, Echeverria JC, Laguna M, et al. Efeito das condições supercríticas de secagem em etanol nas propriedades estruturais e texturais de aerogéis de sílica. Journal of Porous Materials, 15 (2008) 705-713
- Li M, Pham PJ, Pittman CU, et al. Extração seletiva de fase sólida de a-tocoferol por adsorvente SBA-15 mesoporoso modificado com líquido iônico funcionalizado. Analytical Sciences, 24 (2008) 1245-1250
- Ottiger S, Pini R, Storti G, et al. Equilíbrios de adsorção competitiva de CO 2 e CH 4 em carvão seco. Adsorption-Journal of the International Adsorption Society. 14 (2008) 539-556
- Vedaraman N, Srinivasakannan C, Brunner G, et al. Cinética da extração do colesterol usando dióxido de carbono supercrítico com co-solventes. Industrial & Engineering Chemistry Research, 47 (2008) 6727-6733
- Chen Y, Koberstein JT. Fabricação de monocamadas de copolímero em bloco por adsorção de fluidos supercríticos: Um conceito versátil para modificação e funcionalização de superfícies de polímero. Langmuir, 24 (2008) 10488-10493




























![{\ displaystyle V (r) = 4 \ epsilon _ {ff} \ left [\ left ({\ frac {\ sigma _ {ff}} {r}} \ right) ^ {12} - \ left ({\ frac {\ sigma _ {ff}} {r}} \ right) ^ {6} \ right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a5efab3352aa458cba10f0432a38ac48a306019c)

