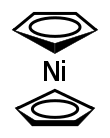
Níqueloceno - Nickelocene
|
|
|||

|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Níqueloceno |
|||
| Outros nomes
Bis (ciclopentadienil) níquel (II)
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.013.672 |
||
| Número EC | |||
| 3412 | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1325 3082 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 10 H 10 Ni | |||
| Massa molar | 188,88 g / mol | ||
| Aparência | Cristais verdes | ||
| Densidade | 1,47 g / cm 3 | ||
| Ponto de fusão | 171 a 173 ° C (340 a 343 ° F; 444 a 446 K) | ||
| insolúvel | |||
| Estrutura | |||
| D 5h , D 5d | |||
| 0 D | |||
| Perigos | |||
| Pictogramas GHS |
  
|
||
| Palavra-sinal GHS | Perigo | ||
| H228 , H302 , H317 , H350 | |||
| P201 , P202 , P210 , P240 , P241 , P261 , P264 , P270 , P272 , P280 , P281 , P301 + 312 , P302 + 352 , P308 + 313 , P321 , P330 , P333 + 313 , P363 , P370 + 378 , P405 , P501 | |||
| NFPA 704 (diamante de fogo) | |||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
490 mg kg −1 (oral, rato) 600 mg kg −1 (oral, camundongo) |
||
| Compostos relacionados | |||
|
Compostos relacionados
|
CoCp 2 , FeCp 2 | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Níqueloceno é o composto de organoníquel com a fórmula Ni ( η 5 -C 5 H 5 ) 2 . Também conhecido como bis (ciclopentadienil) níquel ou NiCp 2 , este sólido paramagnético verde brilhante é de interesse acadêmico duradouro, embora ainda não tenha nenhuma aplicação prática conhecida.
Estrutura e ligação
Ni (C 5 H 5 ) 2 pertence a um grupo de compostos organometálicos chamados metalocenos . Os metalocenos geralmente adotam estruturas nas quais um íon metálico é imprensado entre dois anéis ciclopentadienil (Cp) paralelos . No estado sólido, a molécula tem simetria D 5d , em que os dois anéis são escalonados .
O centro de Ni tem uma carga formal +2, e os anéis Cp são geralmente designados como ânions ciclopentadienil (Cp - ), relacionados ao ciclopentadieno por desprotonação. A estrutura é semelhante ao ferroceno . Em termos de sua estrutura eletrônica, três pares de elétrons d no níquel são alocados aos três orbitais d envolvidos na ligação Ni – Cp: d xy , d x 2 - y 2 , d z 2 . Os dois restantes d-electrões cada residem no d yz e d xz orbitais, dando origem a paramagnetismo da molécula, tal como se manifesta na área de desvio químico invulgarmente alta observada na sua 1 H espectro NMR . Com 20 elétrons de valência , o níqueloceno tem a maior contagem de elétrons dos metalocenos de metais de transição. Cobaltoceno , Co (C 5 H 5 ) 2 , com apenas 19 elétrons de valência é, no entanto, um agente redutor mais forte, ilustrando o fato de que a energia do elétron, e não a contagem de elétrons, determina o potencial redox.
Preparação
O níqueloceno foi preparado pela primeira vez por EO Fischer em 1953, logo após a descoberta do ferroceno , o primeiro composto de metaloceno. Foi preparado em uma reação de um único vaso, por desprotonação do ciclopentadieno com brometo de etilmagnésio e adição de acetilacetonato de níquel (II) anidro . Uma síntese moderna envolve o tratamento de fontes anidras de NiCl 2 (como cloreto de hexaammineníquel ) com ciclopentadienil de sódio :
- [Ni (NH 3 ) 6 ] Cl 2 + 2 NaC 5 H 5 → Ni (C 5 H 5 ) 2 + 2 NaCl + 6 NH 3
Propriedades
Como muitos compostos organometálicos, Ni (C 5 H 5 ) 2 não tolera exposição prolongada ao ar antes da decomposição perceptível. As amostras são normalmente tratadas com técnicas sem ar .
A maioria das reações químicas do níqueloceno é caracterizada por sua tendência a produzir produtos de 18 elétrons com perda ou modificação de um anel Cp.
- Ni (C 5 H 5 ) 2 + 4 PF 3 → Ni (PF 3 ) 4 + produtos orgânicos
A reação com fosfinas secundárias segue um padrão semelhante:
- 2 Ni (C 5 H 5 ) 2 + 2 PPh 2 H → [Ni 2 (PPh 2 ) 2 (C 5 H 5 ) 2 ] + 2 C 5 H 6
O níqueloceno pode ser oxidado ao cátion correspondente, que contém Ni (III).
O Ni (C 5 H 5 ) 2 gasoso se decompõe em um espelho de níquel ao entrar em contato com uma superfície quente, liberando os ligantes de hidrocarbonetos como coprodutos gasosos. Esse processo tem sido considerado um meio de preparação de filmes de níquel.
O níqueloceno reage com o ácido nítrico para produzir ciclopentadienil níquel nitrosil , um composto organoníquel altamente tóxico.