Tiobenzofenona - Thiobenzophenone

|
|

|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Difenilmetanotiona |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 13 H 10 S | |
| Massa molar | 198,28 g · mol −1 |
| Aparência | Sólido azul profundo |
| Ponto de fusão | 53 a 54 ° C (127 a 129 ° F; 326 a 327 K) |
| Ponto de ebulição | 174 ° C (345 ° F; 447 K) |
| Perigos | |
| Ponto de inflamação | não |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
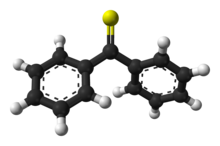
A tiobenzofenona é um composto organossulfurado com a fórmula (C 6 H 5 ) 2 CS. É a tiocetona prototípica . Ao contrário de outras tiocetonas que tendem a se dimerizar para formar anéis e polímeros, a tiobenzofenona é bastante estável, embora fotoxida no ar para formar benzofenona e enxofre. A tiobenzofenona é azul profundo e se dissolve facilmente em muitos solventes orgânicos.
Estrutura
O comprimento da ligação C = S da tiobenzofenona é 1,63 Å, que é comparável a 1,64 Å, o comprimento da ligação C = S do tioformaldeído, medido na fase gasosa. Devido às interações estéricas, os grupos fenil não são coplanares e o ângulo diédrico SC-CC é de 36 °. Uma variedade de tionas com estruturas e estabilidade relacionadas à tiobenzofenona também foram preparadas.
Síntese
Uma das primeiras sínteses relatadas de tiobenzofenona envolve a reação de hidrossulfeto de sódio e difenildiclorometano ":
- Ph 2 CCl 2 + 2 NaSH → Ph 2 C = S + 2 NaCl + H 2 S
Um método atualizado envolve sulfetação de benzofenona:
- Ph 2 C = O + H 2 S → Ph 2 C = S + H 2 O
No esquema de reação acima, uma mistura de cloreto de hidrogênio gasoso e sulfeto de hidrogênio é passada para uma solução resfriada de benzofenona em etanol. A tiobenzofenona também pode ser produzida por uma reação de Friedel-Crafts de cloreto de tiobenzoíla e benzeno.
Reatividade
Devido à fraqueza da ligação C = S, a tiobenzofenona é mais reativa do que sua contraparte C = O benzofenona. A tiobenzofenona, bem como outras tiocetonas, são consideradas superdipolarófilos e dienófilos que se combinam rapidamente com 1,3-dienos nas cicloadições de Diels-Alder. A taxa de tiocetonas em cicloadições está relacionada, mas não limitada ao tamanho da pequena lacuna de energia HOMO / LUMO dos π-MOs da ligação dupla C = S. As reações entre a tiobenzofenona e a maioria dos dienos produzem adutos de Diels-Alder, enquanto as reações com monoolefinas produzem compostos bicíclicos.
