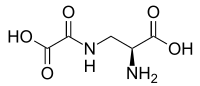
Ácido oxalildiaminopropiônico - Oxalyldiaminopropionic acid
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Ácido ( 2S ) -2-amino-3- (oxaloamino) propanóico |
|
| Outros nomes | |
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3DMet | |
| Abreviações | |
| ChEBI | |
| ChemSpider | |
| KEGG | |
| Malha | oxalildiaminopropiônico + ácido |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 5 H 8 N 2 O 5 | |
| Massa molar | 176,128 g · mol −1 |
| Compostos relacionados | |
|
Compostos relacionados
|
Beta-Metilamino-L-alanina |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O ácido oxalildiaminopropiônico ( ODAP ) é um análogo estrutural do neurotransmissor glutamato encontrado na ervilha Lathyrus sativus . É a neurotoxina responsável pelo latirismo da síndrome da degeneração do neurônio motor .
Origens
ODAP é encontrado nas sementes da leguminosa L. sativus , uma ervilha, na faixa de 0,5% p / p. L. sativus pode ser encontrado em áreas da Europa Meridional, Central e Oriental, na Bacia do Mediterrâneo, Iraque e Afeganistão, bem como em áreas da Ásia e da África.
História
Em algumas regiões, incluindo o subcontinente indiano, Bangladesh, Etiópia e Nepal, a ervilha se tornou um alimento básico. A planta tem uma alta tolerância às condições ambientais, o que resulta em ser a única fonte de alimento disponível em épocas de fome ou seca. Após essas secas de vários meses, podem ocorrer epidemias de neurolatirismo. O último caso dessa epidemia (em 2013) foi na Etiópia durante a seca de 1995-1997, durante a qual 2.000 pessoas ficaram permanentemente incapacitadas.
Efeitos biológicos
ODAP é um agonista do receptor de glutamato AMPA ionotrópico . É conhecido por causar neurolatirismo em humanos, uma doença degenerativa do neurônio motor caracterizada pela degeneração dos neurônios do trato piramidal na medula espinhal e na área do córtex que controla as pernas, resultando em paralisia da parte inferior do corpo. Não há uma explicação direta de como ODAP causa neurolathyrism; no entanto, há evidências que apóiam alguns efeitos biológicos. Uma razão pela qual o mecanismo de ação não está totalmente claro pode ser porque, até agora, não foi encontrado um bom modelo animal para o efeito do ODAP em humanos. O LD 50 também é desconhecido.
Excitotoxicidade
ODAP ativa os receptores AMPA que podem induzir excitotoxicidade ou superestimulação dos receptores de glutamato. A liberação de muito glutamato, de uma só vez ou por um período de tempo prolongado, levará ao aumento dos níveis de Ca2+
no citoplasma. Desde Ca2+
é o íon de sinalização para a liberação de glutamato na sinapse, isso pode resultar na potencialização do ciclo de liberação de glutamato e na disseminação de danos excitotóxicos aos neurônios vizinhos. Dentro do neurônio, o Ca extra2+
vai deixar o citoplasma e entrar na mitocôndria ou no retículo endoplasmático (ER), o que pode levar ao acúmulo de proteínas mal dobradas ou não dobradas no ER e, por fim, morte celular em ambos os casos. Além de atuar como agonista, há evidências de que o ODAP é transportado para a célula por um antiportador que simultaneamente transporta o glutamato para a sinapse.
Estresse oxidativo
O segundo efeito biológico do ODAP é o estresse oxidativo . As espécies reativas de oxigênio (ROS) são geradas na mitocôndria durante o metabolismo, e o corpo possui mecanismos para neutralizar essas moléculas antes que causem danos. O estresse oxidativo resulta de uma perturbação no funcionamento normal dessas vias. Um antioxidante na via de neutralização é a glutationa (GSH), cuja síntese requer os aminoácidos contendo enxofre metionina e cisteína como precursores. Acredita-se que o ODAP, possivelmente devido à excitotoxicidade induzida, reduza a ingestão de cisteína por meio de seu antiporter . Isso inibe a síntese de GSH, levando a um aumento da produção de ROS e dano mitocondrial. Os neurônios motores podem ser os mais sensíveis ao envenenamento por ODAP porque exibem uma maior dependência do precursor de GSH metionina. Além disso, L. sativus , como alimento, é deficiente em aminoácidos contendo enxofre, aumentando os efeitos do ODAP no nível do receptor na produção de GSH quando ingerido.
Síntese
Biossíntese
Em L. sativus o ODAP é sintetizado nas mudas jovens a partir do precursor (β-isoxazolin-5-on-2-il) -alanina, também conhecido como BIA. A BIA não foi detectada em partes de plantas maduras ou sementes em maturação. A via começa com a formação de BIA a partir de O-acetil-L-serina (OAS) e isoxazolin-5-on. A abertura do anel leva à formação do ácido 2,3-L-diaminopropanóico (DAPRO) intermediário de vida curta, que é então oxalilizado pela oxalil- coenzima A para formar ODAP.
Síntese química
ODAP pode ser sintetizado a partir de ácido L-α, β-diaminopropiônico e oxalato de dimetil a um pH de 4,5-5. O óxido cúprico pode ser usado para proteger temporariamente o grupo α-NH2 do ácido L-α, β-diaminopropriônico durante a reação.
Veja também
- β-Metilamino- L- alanina , uma toxina relacionada


