Tetrafluoroborato de trietiloxônio - Triethyloxonium tetrafluoroborate
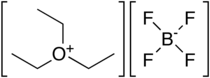
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Tetrafluoroborato de trietiloxônio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3598090 | |
| ChemSpider | |
| ECHA InfoCard |
100,006,096 |
|
PubChem CID
|
|
| UNII | |
| Número ONU | 3261 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 6 H 15 B F 4 O | |
| Massa molar | 189,99 g · mol −1 |
| Ponto de fusão | 91 a 92 ° C (196 a 198 ° F; 364 a 365 K) |
| Reage | |
| Perigos | |
|
|
|
| Frases R (desatualizado) | R14 , R34 |
| Frases S (desatualizado) | S22 , S26 , S36 / 37/39 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
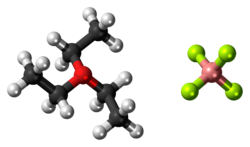
O tetrafluoroborato de trietiloxônio é o composto de oxônio orgânico com a fórmula [(CH 3 CH 2 ) 3 O] BF 4 . É freqüentemente chamado de reagente de Meerwein ou sal de Meerwein em homenagem a seu descobridor Hans Meerwein . Também bem conhecido e disponível comercialmente é o relacionado tetrafluoroborato de trimetiloxônio . Os compostos são sólidos brancos que se dissolvem em solventes orgânicos polares. Eles são fortes agentes alquilantes . Além do BF-
4 sal, muitos derivados relacionados estão disponíveis.
Síntese e reatividade
O tetrafluoroborato de trietiloxônio é preparado a partir de trifluoreto de boro , éter dietílico e epicloridrina :
- 4 Et 2 O · BF 3 + 2 Et 2 O + 3 C 2 H 3 (O) CH 2 Cl → 3 Et 3 O + BF-
4+ B [(OCH (CH 2 Cl) CH 2 OEt] 3
O sal de trimetiloxônio está disponível a partir de éter dimetílico por uma via análoga. Esses sais não têm vida útil longa em temperatura ambiente. Eles se degradam por hidrólise:
- [(CH 3 CH 2 ) 3 O] + BF-
4+ H 2 O → (CH 3 CH 2 ) 2 O + CH 3 CH 2 OH + HBF 4
A propensão dos sais de trialquiloxônio para a troca de alquil pode ser vantajosa. Por exemplo, o tetrafluoroborato de trimetiloxônio, que reage lentamente devido à sua baixa solubilidade na maioria dos solventes compatíveis, pode ser convertido in situ em alquil superior / oxônio mais solúvel, acelerando assim as reações de alquilação.
Estrutura
A estrutura do tetrafluoroborato de trietiloxônio não foi caracterizada por cristalografia de raios-X , mas a estrutura do hexafluorofosfato de trietiloxônio foi examinada. As medições confirmam que o cátion é piramidal com ângulos COC na faixa de 109,4 ° –115,5 °. A distância C – O média é 1,49 Å.
Segurança
O tetrafluoroborato de trietiloxônio é um forte agente alquilante, embora os riscos sejam reduzidos por ser não volátil. Ele libera ácido forte em contato com a água. As propriedades do derivado de metila são semelhantes.
Referências
- ^ H. Meerwein; G. Hinz; P. Hofmann; E. Kroning e E. Pfeil (1937). "Über Tertiäre Oxoniumsalze, I". Journal für Praktische Chemie . 147 (10-12): 257. doi : 10.1002 / prac.19371471001 .
- ^ H. Meerwein; E. Bettenberg; H. Gold; E. Pfeil e G. Willfang (1940). "Über Tertiäre Oxoniumsalze, II". Journal für Praktische Chemie . 154 (3–5): 83. doi : 10.1002 / prac.19391540305 .
- ^ Hartwig Prest, Dave G. Seapy "Triethyloxonium Tetrafluoroborate" em Encyclopedia of Reagents for Organic Synthesis John Wiley & Sons, New York, 2008. doi : 10.1002 / 047084289X.rt223.pub2 . Data de publicação online do artigo: 14 de março de 2008
- ^ H. Meerwein (1973). "Fluoborato de trietiloxônio" . Sínteses orgânicas .; Volume coletivo , 5 , pág. 1080
- ^ TJ Curphey (1988). "Tetrafluoroborato de trimetiloxônio" . Sínteses orgânicas .; Volume coletivo , 6 , pág. 1019
- ^ Vartak AP & Crooks PA (2009). "Uma síntese enantiosseletiva escalável do agonista alfa2-adrenérgico, lofexidina". Org. Process Res. Dev. 13 (3): 415–419. doi : 10.1021 / op8002689 .
- ^ Watkins, Michael I .; Ip, Wai Man; Olah, George A .; Bau, Robert (1982). "Structure of Oxonium Ions: An X-Ray Crystallographic Study of Triethyloxonium Hexafluorophosphate and Triphenyloxonium Tetraphenylborate". Journal of the American Chemical Society . 104 (9): 2365–2372. doi : 10.1021 / ja00373a006 .
