Síndrome de Goodpasture - Goodpasture syndrome
| Síndrome de Goodpasture | |
|---|---|
| Outros nomes | Doença de Goodpasture, doença antiglomerular de anticorpos basais, doença anti-GBM |
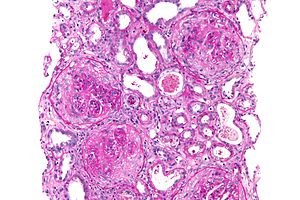 | |
| Micrografia de uma glomerulonefrite crescente que demonstrou ser doença antiglomerular da membrana basal, coloração PAS | |
| Especialidade |
Nefrologia , pneumologia , imunologia |
A síndrome de Goodpasture (GPS) , também conhecida como doença antiglomerular da membrana basal , é uma doença autoimune rara em que os anticorpos atacam a membrana basal dos pulmões e rins, causando sangramento pulmonar, glomerulonefrite e insuficiência renal . Acredita-se que ele ataque a subunidade alfa-3 do colágeno tipo IV , que, portanto, tem sido chamada de antígeno de Goodpasture. A síndrome de Goodpasture pode resultar rapidamente em danos permanentes aos pulmões e aos rins, geralmente levando à morte. É tratada com medicamentos que suprimem o sistema imunológico , como corticosteroides e ciclofosfamida , e com plasmaférese , na qual os anticorpos são removidos do sangue.
A doença foi descrita pela primeira vez por um patologista americano Ernest Goodpasture da Vanderbilt University em 1919 e mais tarde foi nomeada em sua homenagem.
sinais e sintomas
Os anti- membrana glomerular basal (GBM) anticorpos atacam primariamente os rins e pulmões, apesar de, sintomas como mal-estar, perda de peso, fadiga, febre generalizada, calafrios e também são comuns, como são as dores articulares. 60 a 80% das pessoas com a doença apresentam envolvimento pulmonar e renal; 20-40% têm envolvimento renal sozinho e menos de 10% têm envolvimento pulmonar sozinho. Os sintomas pulmonares geralmente precedem os sintomas renais e geralmente incluem: tosse com sangue , dor no peito (em menos de 50% dos casos no geral), tosse e falta de ar . Os sintomas renais geralmente incluem sangue na urina , proteína na urina , inchaço inexplicável dos membros ou da face , quantidades elevadas de ureia no sangue e pressão alta .
Causa
Embora a causa exata seja desconhecida, a predisposição genética para GPS envolve o sistema de antígeno leucocitário humano (HLA), especificamente HLA-DR15 . Além da suscetibilidade genética, um insulto ambiental inicial à vasculatura pulmonar é necessário para permitir que os anticorpos antimembrana basal glomerular (anti-GBM) atinjam os capilares alveolares . Exemplos de tal insulto incluem: exposição a solventes orgânicos (por exemplo, clorofórmio ) ou hidrocarbonetos, exposição à fumaça de tabaco , infecção (como influenza A ), inalação de cocaína , inalação de pó de metal, bacteremia , sepse , ambientes de alto oxigênio e terapias antilinfócitos (especialmente com anticorpos monoclonais ). A exposição a produtos químicos de limpeza a seco e ao herbicida da marca Paraquat também foi apontada como insultos em potencial. No GPS, anticorpos anti-GBM são produzidos e circulados por toda a corrente sanguínea, danificando as membranas que revestem os pulmões e os rins, além de direcionar seus capilares.
Fisiopatologia
O GPS é causado pela produção anormal de células plasmáticas de anticorpos anti-GBM. O principal alvo desses anticorpos anormais é o domínio não colágeno da cadeia alfa-3 do colágeno tipo 4, que é encontrado principalmente nas membranas basais dos capilares glomerulares e alveolares, explicando os sintomas obscuramente específicos dessa condição. Esses anticorpos ligam seus epítopos reativos às membranas basais e ativam a cascata do complemento, levando à morte das células marcadas. Um anticorpo específico e ligação de epítopo que mostra a maior afinidade e é patogênico ocorre entre os anticorpos GP A e a região do epítopo anti-GBM, designada E A , que é os resíduos 17-31 da subunidade alfa 3 do domínio não colágeno do tipo IV colágeno. As células T também estão implicadas, embora seja geralmente considerada uma reação de hipersensibilidade do tipo II.
Diagnóstico
O diagnóstico de GPS costuma ser difícil, pois várias outras doenças podem causar as várias manifestações da doença e a própria condição é rara. O meio mais preciso de fazer o diagnóstico é testar os tecidos afetados por meio de biópsia , principalmente do rim, por ser o órgão mais bem estudado para a obtenção de amostra para a presença de anticorpos anti-GBM. Além dos anticorpos anti-GBM implicados na doença, cerca de um em cada três dos afetados também tem anticorpos antineutrofílicos citoplasmáticos em sua corrente sanguínea, que muitas vezes antecede os anticorpos anti-GBM em cerca de alguns meses ou mesmo anos. Quanto mais tarde a doença for diagnosticada, pior será o resultado para a pessoa afetada.
Além disso, se houver suspeita substancial da doença, o teste seralógico para o ensaio ELISA geralmente é feito procurando a área do domínio alfa3 NC1 do colágeno IV para evitar falsos positivos.
Tratamento
O principal pilar do tratamento do GPS é a plasmaférese , procedimento em que o sangue da pessoa afetada é enviado por uma centrífuga e os vários componentes são separados por peso. O plasma contém os anticorpos anti-GBM que atacam os pulmões e os rins da pessoa afetada e é filtrado. As outras partes do sangue ( glóbulos vermelhos , glóbulos brancos e plaquetas ) são recicladas e reinfundidas por via intravenosa. A maioria dos indivíduos afetados pela doença também precisa ser tratada com medicamentos imunossupressores , especialmente ciclofosfamida , prednisona e rituximabe , para prevenir a formação de novos anticorpos anti-GBM de modo a prevenir maiores danos aos rins e pulmões. Outros imunossupressores menos tóxicos, como a azatioprina, podem ser usados para manter a remissão.
Prognóstico
Com o tratamento, a taxa de sobrevida em cinco anos é> 80% e menos de 30% dos indivíduos afetados requerem diálise de longo prazo. Um estudo realizado na Austrália e na Nova Zelândia demonstrou que em pacientes que requerem terapia de substituição renal (incluindo diálise), o tempo médio de sobrevida é de 5,93 anos. Sem tratamento, praticamente todas as pessoas afetadas morrerão de insuficiência renal avançada ou hemorragia pulmonar.
Epidemiologia
O GPS é raro, afetando cerca de 0,5-1,8 por milhão de pessoas por ano na Europa e na Ásia. Também é incomum entre as doenças autoimunes, pois é mais comum em homens do que em mulheres e também é menos comum em negros do que em brancos, mas mais comum no povo Māori da Nova Zelândia. As faixas etárias de pico para o início da doença são de 20-30 e 60-70 anos.
Veja também
Referências
links externos
| Classificação | |
|---|---|
| Fontes externas |