Citrato de cálcio - Calcium citrate
 Estrutura 2D do citrato de cálcio
|
|
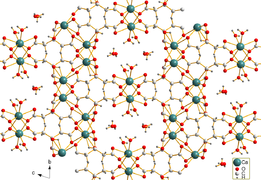 Citrato de cálcio tetrahidratado
|
|
 Citrato de cálcio tetrahidratado
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Sal de cálcio do ácido 2-hidroxi-1,2,3-propano-tricarboxílico (2: 3)
|
|
| Outros nomes
E333, dicitrato tricálcico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.011.265 |
| Número EC | |
| Número E | E333 (antioxidantes, ...) |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Ca 3 (C 6 H 5 O 7 ) 2 | |
| Massa molar | 498,4334 g / mol (anidro) 570,4945 g / mol (tetra-hidrato) |
| Aparência | pó branco |
| Odor | inodoro |
| Densidade | 1,63 g / cm 3 (anidro) 2,00 g / cm 3 (tetra-hidrato) |
| Ponto de fusão | Decompõe-se |
| Ponto de ebulição | Decompõe-se |
| 0,85 g / L (18 ° C) 0,95 g / L (25 ° C) |
|
| Solubilidade | insolúvel em álcool |
| Estrutura | |
| Triclínico (tetrahidrato) | |
| P 1 , No. 2 | |
|
a = 0,59466 (4) nm, b = 1,02247 (8) nm, c = 1,66496 (13) nm
α = 72,213 (7) °, β = 79,718 (7) °, γ = 89,791 (6) °
|
|
| Perigos | |
| Riscos principais | Irritante |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros cátions
|
Citrato de magnésio Citrato de estrôncio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O citrato de cálcio é o sal de cálcio do ácido cítrico . É comumente usado como aditivo alimentar ( E333 ), geralmente como conservante , mas às vezes para dar sabor . Nesse sentido, é semelhante ao citrato de sódio . O citrato de cálcio também é encontrado em alguns suplementos dietéticos de cálcio (por exemplo, Citracal). O cálcio representa 24,1% do citrato de cálcio (anidro) e 21,1% do citrato de cálcio (tetra-hidratado) em massa. O tetraidrato ocorre na natureza como o mineral Earlandita .
Propriedades quimicas
O citrato de cálcio é moderadamente solúvel em água. Cristais em forma de agulha de tetra-hidrato de dicitrato tricálcico [Ca 3 (C 6 H 5 O 7 ) 2 (H 2 O) 2 ] · 2H 2 O foram obtidos por síntese hidrotérmica. A estrutura cristalina compreende uma rede tridimensional na qual cátions Ca2 + óctuplo coordenados são ligados por ânions citrato e ligações de hidrogênio entre duas moléculas de água cristalina não coordenadas e duas moléculas de água coordenadas.
Produção
O citrato de cálcio é um intermediário no isolamento do ácido cítrico do processo de fermentação dos fungos , pelo qual o ácido cítrico é produzido industrialmente. O ácido cítrico na solução do caldo é neutralizado por água de cal , precipitando o citrato de cálcio insolúvel. Este é então filtrado do resto do caldo e lavado para dar citrato de cálcio limpo.
- 3 Ca (OH) 2 (s) + 2 C 6 H 8 O 7 (l) → Ca 3 (C 6 H 5 O 7 ) 2 (s) + 6 H 2 O (l)
O citrato de cálcio assim produzido pode ser vendido como está, ou pode ser convertido em ácido cítrico usando ácido sulfúrico diluído.
Papel biológico
Em muitos indivíduos, a biodisponibilidade do citrato de cálcio é igual à do carbonato de cálcio mais barato . No entanto, alterações no trato digestivo podem alterar a forma como o cálcio é digerido e absorvido. Ao contrário do carbonato de cálcio, que é básico e neutraliza o ácido do estômago, o citrato de cálcio não tem efeito sobre o ácido do estômago. O carbonato de cálcio é mais difícil de digerir do que o citrato de cálcio, e o carbonato de cálcio apresenta um risco de "rebote ácido" (o estômago supercompensa produzindo mais ácido), portanto, os indivíduos que são sensíveis a antiácidos ou que têm dificuldade em produzir ácido estomacal adequado podem escolher o citrato de cálcio sobre carbonato de cálcio para suplementação. De acordo com pesquisas recentes sobre a absorção de cálcio após a cirurgia de bypass gástrico, o citrato de cálcio pode ter melhor biodisponibilidade em relação ao carbonato de cálcio em pacientes de bypass gástrico em Y-de-Roux que estão tomando citrato de cálcio como suplemento dietético após a cirurgia. Isso se deve principalmente às mudanças relacionadas ao local onde ocorre a absorção do cálcio no trato digestivo desses indivíduos.

