Peptídeo carnudo e carnudo - Beefy meaty peptide
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
(2 S , 5 S , 8, S , 11 S , 14 S , 17 S ) -17- {2 - [(2 S ) -2,6-Diaminohexanamido] acetamido} -8- (hidroximetil) -11,14- ácido bis (3-hidroxi-3-oxopropil) -2-metil-5- (2-metilpropil) -4,7,10,13,16-pentaoxo-3,6,9,12,15-pentaazanonadecanodioico |
|
| Outros nomes
Peptídeo delicioso; BMP; BMP (peptídeo); G -Lysylglycyl- L -α-aspartyl- L -α-glutamil- L -α-glutamil- L -seryl- L -leucil- L -alanina; KGDEESLA
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
|
|
|
| Propriedades | |
| C 34 H 57 N 9 O 16 | |
| Massa molar | 847,877 g · mol −1 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O peptídeo carnudo bovino , também conhecido como peptídeo delicioso e abreviado como BMP , é um peptídeo de 8 aminoácidos que foi identificado como conferindo um sabor carnudo aos alimentos nos quais está presente. Foi isolado da sopa de carne por Yamasaki e Maekawa em 1978. Pesquisas em andamento desde sua descoberta por Yamasaki e Maekawa forneceram suporte geral para a presença de suas propriedades de conferir sabor. No entanto, devido ao seu alto custo de produção, o potencial do peptídeo para ampla aplicação na indústria de alimentos ainda precisa ser realizado, levando os esforços de pesquisa atuais a se concentrarem em encontrar um método de produção em massa para o peptídeo.
Identificação
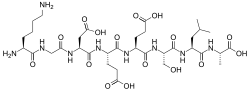
Seqüência
Lys-Gly-Asp-Glu-Glu-Ser-Leu-Ala
A estrutura primária foi determinada pela primeira vez por Yamasaki e Maekawa, que realizaram o experimento usando o método de degradação de Edman para sequenciamento N-terminal e carboxipeptidase A (Cpase A) e métodos de triazinação para sequenciamento C-terminal . No momento do experimento (1978), ambos os métodos foram usados para determinar a composição de aminoácidos e a ordem da sequência, incluindo a descoberta de uma ligação Glu-Glu e a detecção de alanina no C-terminal. No entanto, hoje em dia, qualquer uma das técnicas é suficiente para sequenciar todo o peptídeo.
Produção de sabor umami
Em um nível molecular, o sabor umami é registrado quando moléculas como o glutamato e o aspartato se ligam aos domínios de ligação do ligante de receptores de sabor especializados. Uma vez ativados, esses receptores enviam pulsos elétricos que viajam para o cérebro por meio de neurônios sensoriais. Em 1989, Tamura et al. descobriram que, por si próprios, resíduos básicos como Lys-Gly e Lys-Lys produziram sabores azedos e salgados em suas formas de dicloridrato, enquanto resíduos ácidos como Asp-Glu-Glu e Lys-Gly produziram sabores azedos e doces. No entanto, o sabor umami é produzido por combinações de resíduos de aminoácidos ácidos e básicos, como Lys-Gly-Asp. Mais especificamente, o sabor umami encontrado em BMP é gerado pela combinação de lisina no terminal N e os aminoácidos ácidos (Asp-Glu-Glu) na seção mediana do peptídeo, o que sugere que cátions e ânions desempenham um papel na a estimulação de receptores gustativos para produzir o gosto umami.
No entanto, outros fatores além da presença de certos aminoácidos podem afetar a resposta de sabor do peptídeo. A intensidade do sabor umami aumenta quando o peptídeo ácido interage com cátions para formar um sal. A um valor limite de 1,25 milimolar (mM), o dipeptídeo Asp-Glu gera o sabor umami mais forte quando exposto a NaOH e sujeito a um aumento de pH. A posição dos aminoácidos também desempenha um papel na intensidade do sabor, uma vez que um dipeptídeo Glu-Asp se registra em um valor limite de 3,14 mM, o que significa que seria necessária uma quantidade maior do composto para que uma pessoa registrasse o sabor umami. Além disso, enquanto um análogo Lys-Gly-HCl registraria um sabor salgado, umami em 1,22 mM, um análogo Gly-Lys-HCl registra um sabor azedo e doce em 5,48 mM. Assim, os resultados da pesquisa indicaram que o sabor pode ser modificado em sabor e força por meio da modificação de resíduos ácidos em peptídeos, abrindo possibilidades para a produção de peptídeos semelhantes a BMP com maior intensidade de sabor. Embora sua intensidade de sabor não mude de acordo com o pH, BMP foi descrito para produzir sabores diferentes de acordo com as mudanças de pH. Notavelmente, é relatado como ácido a um pH de 3,5, umami a um pH de 6,5 e doce, azedo e umami a um pH de 9,5.
Viabilidade para aplicação no mundo real
Foi demonstrado que o BMP permanece estável, sem quebrar, em condições de pasteurização e esterilização de alta temperatura, tornando possível o uso potencial para fins culinários. Aqueles que defendem a presença do sabor umami que intensifica o sabor do BMP relatam que seu sabor é semelhante ao do glutamato monossódico. Consequentemente, o BMP possui potencial para comercialização em larga escala na indústria de alimentos. No entanto, o principal obstáculo é o custo de produção em massa associado ao peptídeo. Atualmente, os principais modos de produção de peptídeos aromatizantes específicos, como o BMP, são a síntese química e enzimática, ambas envolvendo altos custos de produção.
