Adrenomedulina - Adrenomedullin
A adrenomedulina ( ADM ou AM ) é um hormônio peptídico vasodilatador de significado incerto na saúde e doença humana. Foi inicialmente isolado em 1993 de um feocromocitoma , um tumor da medula adrenal : daí o nome.
Em humanos, o ADM é codificado pelo gene ADM . ADM é um peptídeo expresso por todos os tecidos e encontrado na circulação. Um peptídeo semelhante denominado adreomedulina2 foi relatado em ratos em 2004, que exibe uma função semelhante.
Função
A adrenomedulina pode funcionar como um hormônio no controle da circulação porque é encontrada no sangue em uma concentração considerável. Foi inicialmente identificado como um vasodilatador , e alguns argumentaram que é o peptídeo vasodilatador endógeno mais potente encontrado no corpo. As diferenças de opinião sobre a capacidade do AM de relaxar o tônus vascular podem surgir das diferenças no sistema de modelo usado.
Outros efeitos do AM incluem estimular o crescimento de novos vasos sanguíneos ( angiogênese ) e aumentar a tolerância das células ao estresse oxidativo e lesão por hipóxia . A adrenomedulina é vista como uma influência positiva em doenças como hipertensão , infarto do miocárdio , doença pulmonar obstrutiva crônica e outras doenças cardiovasculares , enquanto pode ser vista como um fator negativo na potencialização da capacidade das células cancerosas de estender seu suprimento de sangue e, assim, permitir mais proliferação celular.
Peptide
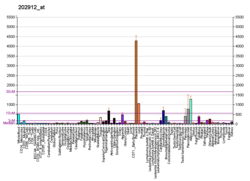
A adrenomedulina consiste em 52 aminoácidos, tem 1 ligação dissulfeto intramolecular e mostra uma ligeira homologia com o peptídeo relacionado ao gene da calcitonina (CGRP). O precursor, denominado preproadrenomedulina, consiste em 185 aminoácidos e pode ser clivado pela calicreína plasmática nos sítios Lys-Arg e Arg-Arg. Por análise de RNA-blot, o mRNA da adrenomedulina humana foi encontrado para ser expresso em todos os tecidos, e mais altamente expresso na placenta, células de gordura, pulmão, ilhotas pancreáticas, músculo liso e pele.
O gene AM humano está localizado em um único locus no cromossomo 11 com 4 exons e 3 introns. O gene AM inicialmente codifica para um peptídeo precursor de 185 aminoácidos, que pode ser excisado diferencialmente para formar uma série de peptídeos, incluindo um AM de 53 aminoácidos inativo, e PAMP, adrenotensina e AM95-146. AM humano maduro é ativado para formar um anel de 6 aminoácidos de 52 aminoácidos, que compartilha similaridade estrutural moderada com a família da calcitonina de peptídeos reguladores (calcitonina, CGRP e amilina). O AM circulante consiste na forma ativa amidada (15%) e na forma inativa glicada (85%). Tem meia-vida plasmática de 22 minutos, taxa média de depuração de 274 mL / kg / min e volume aparente de distribuição de 880 ± 150 mL / kg.
Receptores
A adrenomedulina (AM) exerce suas ações por meio de combinações do receptor semelhante ao receptor de calcitonina ( CALCRL ) ou CLR; e ( proteína modificadora da atividade do receptor ) 2 ( RAMP2 ) ou RAMP3, (conhecidos como receptores AM1 e AM2, respectivamente). Ambos transduzem a ligação do hormônio à sinalização intracelular por meio de cascatas de segundos mensageiros. O receptor AM2 tem baixa afinidade para CGRP, mas isso não tem relevância fisiológica. Ao contrário da noção clássica de um ligante-um receptor de sinalização do receptor, a interação de CALCRL e RAMP na membrana é necessária para AM mediar sua ação: nenhum deles pode se ligar ao hormônio (e, portanto, transduzir um sinal) sozinho. A estimulação de seu receptor por AM aumenta a produção de AMP cíclico (cAMP) e de óxido nítrico.
Antes da descoberta dos RAMPs e da identificação de receptores heteroméricos para a família de peptídeos da calcitonina, um único receptor de adrenomedulina acoplado à proteína G foi identificado, mas relatos mais recentes lançam dúvidas quanto à sua importância nos principais efeitos da adrenomedulina. Em pesquisas mais recentes, as funções dos receptores AM1 e AM2 foram esclarecidas por meio de estudos em camundongos geneticamente manipulados. O nocaute da adrenomedulina é um fenótipo letal embrionário e morre no meio da gestação de uma condição conhecida como hidropisia fetal. O camundongo CALCRL ou CLR KO recapitula o mesmo fenótipo, uma vez que não possui os receptores AM1 e AM2 (incidentalmente confirmando a falta de significado fisiológico para o receptor AM de proteína única anterior descoberto por Kapas). Os camundongos RAMP2 KO também recapitulam o mesmo fenótipo, mostrando que os principais efeitos fisiológicos de AM são transduzidos pelo receptor AM1. Mesmo os camundongos RAMP 2 heterozigotos têm fisiologia perturbada com ossos incomuns e defeitos da glândula mamária e endocrinologia muito aberrante, levando a problemas de fertilidade e lactação. O que é muito surpreendente é que o efeito da deleção do RAMP3 não tem efeitos deletérios e parece conferir vantagens devido à massa óssea maior do que o normal e menor ganho de peso na idade avançada.
Referências
Leitura adicional
- Morfis M, Christopoulos A, Sexton PM (novembro de 2003). "RAMPs: 5 anos depois, para onde vamos agora?". Trends Pharmacol. Sci . 24 (11): 596–601. doi : 10.1016 / j.tips.2003.09.001 . PMID 14607083 .
- Cao YN, Kitamura K, Ito K, Kato J, Hashida S, Morishita K, Eto T (maio de 2003). "A adrenomedulina estendida com glicina exerce efeito vasodilatador por meio de amidação na aorta de rato". Regul. Pept . 113 (1–3): 109–14. doi : 10.1016 / s0167-0115 (03) 00002-8 . PMID 12686469 . S2CID 21919410 .
- Cockcroft JR, Noon JP, Gardner-Medwin J, Bennett T (julho de 1997). "Efeitos hemodinâmicos da adrenomedulina na resistência humana e vasos de capacitância" . Br J Clin Pharmacol . 44 (1): 57–60. doi : 10.1046 / j.1365-2125.1997.00622.x . PMC 2042810 . PMID 9241097 .
links externos
- Adrenomedulina nos cabeçalhos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)
- Localização do genoma humano ADM e página de detalhes do gene ADM no navegador do genoma UCSC .
Este artigo incorpora texto da Biblioteca Nacional de Medicina dos Estados Unidos , que é de domínio público .