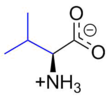
Valine - Valine
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Valine
|
|||
| Outros nomes
Ácido 2-amino-3-metilbutanoico
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.703 |
||
| Número EC | |||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 5 H 11 N O 2 | |||
| Massa molar | 117,148 g · mol −1 | ||
| Densidade | 1,316 g / cm 3 | ||
| Ponto de fusão | 298 ° C (568 ° F; 571 K) (decomposição) | ||
| solúvel | |||
| Acidez (p K a ) | 2,32 (carboxil), 9,62 (amino) | ||
| -74,3 · 10 −6 cm 3 / mol | |||
| Página de dados suplementares | |||
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|||
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
||
| UV , IR , NMR , MS | |||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Valina (símbolo Val ou V ) é um α- aminoácido usado na biossíntese de proteínas. Ele contém um grupo α- amino (que está na forma protonada −NH 3 + sob condições biológicas), um grupo de ácido α- carboxílico (que está na forma desprotonada −COO - sob condições biológicas) e um grupo isopropil de cadeia lateral , tornando-o um aminoácido alifático apolar . É essencial no ser humano, o que significa que o corpo não pode sintetizá-lo: deve ser obtido através da dieta. As fontes alimentares humanas são alimentos que contêm proteínas, como carnes, laticínios, produtos de soja, feijão e legumes. Ele é codificado por todos os códons começando com GU (GUU, GUC, GUA e GUG).
História e etimologia
A valina foi isolada pela primeira vez da caseína em 1901 por Hermann Emil Fischer . O nome valina vem do ácido valérico , que por sua vez tem o nome da planta valeriana devido à presença do ácido nas raízes da planta.
Nomenclatura
De acordo com a IUPAC , os átomos de carbono que formam a valina são numerados sequencialmente a partir de 1 denotando o carbono carboxílico , enquanto 4 e 4 'denotam os dois carbonos metil terminais .
Metabolismo
Fonte e biossíntese
A valina, como outros aminoácidos de cadeia ramificada, é sintetizada pelas plantas, mas não pelos animais. Portanto, é um aminoácido essencial em animais e deve estar presente na dieta alimentar. Os humanos adultos requerem cerca de 4 mg / kg de peso corporal por dia. É sintetizado em plantas e bactérias por meio de várias etapas a partir do ácido pirúvico . A parte inicial da via também leva à leucina . O α-cetoisovalerato intermediário sofre aminação redutiva com glutamato . As enzimas envolvidas nesta biossíntese incluem:
- Acetolactato sintase (também conhecida como acetohidroxiácido sintase)
- Isomeroredutase de ácido acetohidroxi
- Diidroxiácido desidratase
- Valina aminotransferase
Degradação
Como outros aminoácidos de cadeia ramificada, o catabolismo da valina começa com a remoção do grupo amino por transaminação , dando alfa-cetoisovalerato , um alfa- cetoácido , que é convertido em isobutiril-CoA através da descarboxilação oxidativa pela cadeia ramificada α complexo -cetoácido desidrogenase . Este é posteriormente oxidado e reorganizado em succinil-CoA , que pode entrar no ciclo do ácido cítrico .
Síntese
A valina racêmica pode ser sintetizada por bromação de ácido isovalérico seguida por aminação do derivado α-bromo
- HO 2 CCH 2 CH (CH 3 ) 2 + Br 2 → HO 2 CCHBrCH (CH 3 ) 2 + HBr
- HO 2 CCHBrCH (CH 3 ) 2 + 2 NH 3 → HO 2 CCH (NH 2 ) CH (CH 3 ) 2 + NH 4 Br
Significado médico
Resistência a insulina
A valina, como outros aminoácidos de cadeia ramificada, está associada à resistência à insulina: níveis mais elevados de valina são observados no sangue de camundongos, ratos e humanos diabéticos. Os camundongos alimentados com uma dieta de privação de valina por um dia melhoraram a sensibilidade à insulina, e a alimentação com uma dieta de privação de valina por uma semana diminui significativamente os níveis de glicose no sangue. Em camundongos obesos e resistentes à insulina induzidos por dieta, uma dieta com níveis diminuídos de valina e os outros aminoácidos de cadeia ramificada resulta em adiposidade reduzida e sensibilidade à insulina melhorada. O catabólito de valina 3-hidroxiisobutirato promove a resistência à insulina do músculo esquelético em camundongos, estimulando a absorção de ácidos graxos no músculo e o acúmulo de lipídios. Em humanos, uma dieta restrita em proteínas reduz os níveis de valina no sangue e diminui os níveis de glicose no sangue em jejum.
Células-tronco hematopoéticas
A valina dietética é essencial para a autorrenovação das células-tronco hematopoéticas (HSC), conforme demonstrado por experimentos em camundongos. A restrição dietética de valina esgota seletivamente o repovoamento de HSC a longo prazo na medula óssea de camundongos. O transplante de células-tronco com sucesso foi alcançado em camundongos sem irradiação após 3 semanas com dieta restrita em valina. A sobrevivência a longo prazo dos ratos transplantados foi alcançada quando a valina voltou à dieta gradualmente ao longo de um período de 2 semanas para evitar a síndrome de realimentação .
Veja também
Referências
links externos