Unbinilium - Unbinilium
| Unbinilium | ||||||
|---|---|---|---|---|---|---|
| Pronúncia |
/ ˌ u n b aɪ n ɪ l i ə m / ( OON -by- NIL -ee-əm ) |
|||||
| Nomes alternativos | elemento 120, eka-radium | |||||
| Unbinilium na tabela periódica | ||||||
| ||||||
| Número atômico ( Z ) | 120 | |||||
| Grupo | grupo 2 (metais alcalino-terrosos) | |||||
| Período | período 8 | |||||
| Bloquear | bloco s | |||||
| Configuração de elétron | [ Og ] 8s 2 (previsto) | |||||
| Elétrons por camada | 2, 8, 18, 32, 32, 18, 8, 2 (previsto) | |||||
| Propriedades físicas | ||||||
| Fase em STP | sólido (previsto) | |||||
| Ponto de fusão | 953 K (680 ° C, 1256 ° F) (previsto) | |||||
| Ponto de ebulição | 1973 K (1700 ° C, 3092 ° F) (previsto) | |||||
| Densidade (próximo à rt ) | 7 g / cm 3 (previsto) | |||||
| Calor de fusão | 8,03-8,58 kJ / mol (extrapolado) | |||||
| Propriedades atômicas | ||||||
| Estados de oxidação | (+1), ( +2 ), (+4) (previsto) | |||||
| Eletro-negatividade | Escala de Pauling: 0,91 (previsto) | |||||
| Energias de ionização | ||||||
| Raio atômico | empírico: 200 pm (previsto) | |||||
| Raio covalente | 206-210 pm (extrapolado) | |||||
| Outras propriedades | ||||||
| Estrutura de cristal | cúbica de corpo centrado (BCC)
(extrapolado) |
|||||
| Número CAS | 54143-58-7 | |||||
| História | ||||||
| Nomeação | Nome do elemento sistemático IUPAC | |||||
Unbinilium , também conhecido como eka-radium ou simplesmente elemento 120 , é o elemento químico hipotético na tabela periódica com o símbolo Ubn e número atômico 120. Unbinilium e Ubn são o nome e símbolo sistemático temporário IUPAC , que são usados até que o elemento seja descoberto , confirmado e um nome permanente é decidido. Na tabela periódica dos elementos, espera-se que seja um elemento s-block , um metal alcalino-terroso e o segundo elemento no oitavo período . Ele chamou a atenção por causa de algumas previsões de que pode estar na ilha de estabilidade , embora cálculos mais recentes prevejam que a ilha realmente ocorra com um número atômico ligeiramente menor, mais próximo de copernicium e flerovium .
O Unbinilium ainda não foi sintetizado, apesar das várias tentativas das equipes alemãs e russas. Evidências experimentais dessas tentativas mostram que os elementos do período 8 provavelmente seriam muito mais difíceis de sintetizar do que os elementos conhecidos anteriores, e que o unbinilium pode até ser o último elemento que pode ser sintetizado com a tecnologia atual.
A posição do Unbinilium como o sétimo metal alcalino-terroso sugere que ele teria propriedades semelhantes às de seus congêneres mais leves ; entretanto, os efeitos relativísticos podem fazer com que algumas de suas propriedades sejam diferentes daquelas esperadas de uma aplicação direta de tendências periódicas . Por exemplo, espera-se que o unbinilium seja menos reativo do que o bário e o rádio e tenha um comportamento mais próximo do estrôncio e, embora deva mostrar o estado de oxidação +2 característico dos metais alcalino-terrosos, também se prevê que mostre o estado de oxidação +4 , que é desconhecido em qualquer outro metal alcalino-terroso.
Introdução

| Vídeo externo | |
|---|---|
|
|
Os núcleos atômicos mais pesados são criados em reações nucleares que combinam dois outros núcleos de tamanhos desiguais em um; grosso modo, quanto mais desiguais os dois núcleos em termos de massa, maior a possibilidade de os dois reagirem. O material formado pelos núcleos mais pesados é transformado em alvo, que é então bombardeado pelo feixe de núcleos mais leves. Dois núcleos só podem se fundir em um se se aproximarem um do outro; normalmente, os núcleos (todos carregados positivamente) se repelem devido à repulsão eletrostática . A interação forte pode superar essa repulsão, mas apenas dentro de uma distância muito curta de um núcleo; os núcleos do feixe são, portanto, grandemente acelerados a fim de tornar essa repulsão insignificante em comparação com a velocidade do núcleo do feixe. Chegar perto sozinho não é suficiente para dois núcleos se fundirem: quando dois núcleos se aproximam, eles geralmente permanecem juntos por aproximadamente 10-20 segundos e então se separam (não necessariamente na mesma composição de antes da reação) em vez de formar um único núcleo. Se a fusão ocorrer, a fusão temporária - denominada núcleo composto - é um estado excitado . Para perder sua energia de excitação e atingir um estado mais estável, um núcleo composto fissiona ou ejeta um ou vários nêutrons , que carregam a energia. Isso ocorre em aproximadamente 10 a 16 segundos após a colisão inicial.
O feixe passa pelo alvo e atinge a próxima câmara, o separador; se um novo núcleo é produzido, ele é carregado com este feixe. No separador, o núcleo recém-produzido é separado de outros nuclídeos (o do feixe original e quaisquer outros produtos de reação) e transferido para um detector de barreira de superfície , que pára o núcleo. A localização exata do próximo impacto no detector é marcada; também marcados são sua energia e o tempo da chegada. A transferência leva cerca de 10 −6 segundos; para ser detectado, o núcleo deve sobreviver por tanto tempo. O núcleo é registrado novamente assim que sua decadência é registrada, e a localização, a energia e o tempo de decadência são medidos.
A estabilidade de um núcleo é fornecida pela interação forte. No entanto, seu alcance é muito curto; à medida que os núcleos se tornam maiores, sua influência sobre os núcleos mais externos ( prótons e nêutrons) enfraquece. Ao mesmo tempo, o núcleo é dilacerado pela repulsão eletrostática entre prótons, pois tem alcance ilimitado. Os núcleos dos elementos mais pesados são, portanto, teoricamente previstos e, até agora, observou-se que decaem principalmente por meio de modos de decaimento que são causados por tal repulsão: decadência alfa e fissão espontânea ; esses modos são predominantes para núcleos de elementos superpesados . Os decaimentos alfa são registrados pelas partículas alfa emitidas e os produtos do decaimento são fáceis de determinar antes do decaimento real; se tal decaimento ou uma série de decaimentos consecutivos produz um núcleo conhecido, o produto original de uma reação pode ser determinado aritmeticamente. A fissão espontânea, entretanto, produz vários núcleos como produtos, de modo que o nuclídeo original não pode ser determinado a partir de suas filhas.
A informação à disposição dos físicos com o objetivo de sintetizar um dos elementos mais pesados são, portanto, as informações coletadas nos detectores: localização, energia e tempo de chegada de uma partícula ao detector e de seu decaimento. Os físicos analisam esses dados e procuram concluir que ele foi de fato causado por um novo elemento e não poderia ter sido causado por um nuclídeo diferente do alegado. Freqüentemente, os dados fornecidos são insuficientes para concluir que um novo elemento foi definitivamente criado e não há outra explicação para os efeitos observados; erros na interpretação dos dados foram cometidos.
História
Elementos transactinídeos , como o unbinilium, são produzidos por fusão nuclear . Essas reações de fusão podem ser divididas em fusão "quente" e "fria", dependendo da energia de excitação do núcleo composto produzido. Em reações de fusão a quente, projéteis muito leves e de alta energia são acelerados em direção a alvos muito pesados ( actinídeos ), dando origem a núcleos compostos em alta energia de excitação (~ 40-50 MeV ) que podem fissionar ou, alternativamente, evaporar vários (3 a 5 ) nêutrons. Em reações de fusão a frio (que usam projéteis mais pesados, normalmente do quarto período , e alvos mais leves, geralmente chumbo e bismuto ), os núcleos fundidos produzidos têm uma energia de excitação relativamente baixa (~ 10-20 MeV), o que diminui a probabilidade de que estes produtos sofrerão reações de fissão. À medida que os núcleos fundidos se resfriam ao estado fundamental , eles exigem a emissão de apenas um ou dois nêutrons. No entanto, as reações de fusão a quente tendem a produzir produtos mais ricos em nêutrons porque os actinídeos têm as maiores proporções nêutron-próton de todos os elementos que atualmente podem ser feitos em quantidades macroscópicas e atualmente é o único método para produzir os elementos superpesados de flerovium (elemento 114) em diante.
Ununennium e unbinilium (elementos 119 e 120) são os elementos com os números atômicos mais baixos que ainda não foram sintetizados: todos os elementos anteriores foram sintetizados, culminando em oganesson (elemento 118), o elemento conhecido mais pesado, que completa a sétima linha da tabela periódica. As tentativas de sintetizar os elementos 119 e 120 empurram os limites da tecnologia atual, devido às seções transversais decrescentes das reações de produção e suas provavelmente curtas meias-vidas , que devem ser da ordem de microssegundos. Os elementos mais pesados provavelmente teriam vida muito curta para serem detectados com a tecnologia atual: eles decairiam em um microssegundo, antes de chegar aos detectores.
Anteriormente, uma ajuda importante (caracterizada como "balas de prata") na síntese de elementos superpesados veio das conchas nucleares deformadas ao redor do hassium -270 que aumentaram a estabilidade dos núcleos circundantes e a existência do isótopo de cálcio quase estável rico em nêutrons- 48 que poderia ser usado como um projétil para produzir isótopos de elementos superpesados mais ricos em nêutrons. (Quanto mais rico em nêutrons for um nuclídeo superpesado , mais próximo se espera que esteja da procurada ilha de estabilidade .) Mesmo assim, os isótopos sintetizados ainda têm menos nêutrons do que aqueles esperados na ilha de estabilidade. Além disso, o uso de cálcio-48 para sintetizar o unbinilium exigiria um alvo de férmio -257, que ainda não pode ser produzido em grandes quantidades (apenas picogramas podem ser produzidos atualmente; em comparação, miligramas de berquélio e califórnio estão disponíveis), e seria qualquer caso tem um rendimento menor do que usar um alvo de einstênio com projéteis de cálcio-48 para produzir ununênio. A produção mais prática de outros elementos superpesados exigiria projéteis mais pesados do que 48 Ca, mas isso tem a desvantagem de resultar em reações de fusão mais simétricas que são mais frias e menos prováveis de sucesso.
Tentativas de síntese
Após o sucesso na obtenção de oganesson pela reação entre 249 Cf e 48 Ca em 2006, a equipe do Joint Institute for Nuclear Research (JINR) em Dubna iniciou experimentos semelhantes em março-abril de 2007, na esperança de criar o unbinilium a partir de núcleos de 58 Fe e 244 Pu . A análise inicial revelou que nenhum átomo de unbinilium foi produzido, fornecendo um limite de 400 fb para a seção transversal na energia estudada.
-
244
94Pu
+ 58
26Fe
→ 302
120Ubn
* → sem átomos
A equipe russa planejou atualizar suas instalações antes de tentar a reação novamente.
Em abril de 2007, a equipe do GSI Helmholtz Center for Heavy Ion Research em Darmstadt , Alemanha , tentou criar o unbinilium usando urânio -238 e níquel -64:
-
238
92você
+ 64
28Ni
→ 302
120Ubn
* → sem átomos
Nenhum átomo foi detectado, fornecendo um limite de 1,6 pb para a seção transversal na energia fornecida. O GSI repetiu o experimento com maior sensibilidade em três execuções separadas em abril-maio de 2007, janeiro-março de 2008 e setembro-outubro de 2008, todos com resultados negativos, atingindo um limite de seção transversal de 90 fb.
Em 2011, depois de atualizar seus equipamentos para permitir o uso de mais alvos radioativos, os cientistas do GSI tentaram a reação de fusão bastante assimétrica:
-
248
96Cm
+ 54
24Cr
→ 302
120Ubn
* → sem átomos
Esperava-se que a mudança na reação quintuplicaria a probabilidade de sintetizar o unbinilium, uma vez que o rendimento de tais reações é fortemente dependente de sua assimetria. Embora essa reação seja menos assimétrica do que a reação de 249 Cf + 50 Ti, ela também cria mais isótopos de unbinilium ricos em nêutrons que devem receber maior estabilidade de sua proximidade ao fechamento da casca em N = 184. Três sinais foram observados em 18 de maio de 2011; uma possível atribuição a 299 Ubn e suas filhas foi considerada, mas não pôde ser confirmada, e uma análise diferente sugeriu que o que foi observado foi simplesmente uma sequência aleatória de eventos.
Em agosto-outubro de 2011, uma equipe diferente no GSI usando a instalação TASCA tentou uma nova reação ainda mais assimétrica:
-
249
98Cf
+ 50
22Ti
→ 299
120Ubn
* → sem átomos
Por causa de sua assimetria, a reação entre 249 Cf e 50 Ti foi prevista como a reação prática mais favorável para a síntese de unbinilium, embora também seja um pouco fria e esteja mais longe do fechamento da camada de nêutrons em N = 184 do que qualquer um dos outras três reações tentadas. Nenhum átomo de unbinilium foi identificado, implicando em uma seção transversal limite de 200 fb. Jens Volker Kratz previu que a seção transversal máxima real para a produção de unbinilium por qualquer uma das quatro reações 238 U + 64 Ni, 244 Pu + 58 Fe, 248 Cm + 54 Cr ou 249 Cf + 50 Ti em cerca de 0,1 fb; em comparação, o recorde mundial para a menor seção transversal de uma reação bem-sucedida foi de 30 fb para a reação 209 Bi ( 70 Zn, n) 278 Nh , e Kratz previu uma seção transversal máxima de 20 fb para a produção de ununênio. Se essas previsões forem precisas, a síntese do ununênio estaria no limite da tecnologia atual, e a síntese do unbinilium exigiria novos métodos.
Essa reação foi investigada novamente em abril a setembro de 2012 no GSI. Este experimento usou um alvo de 249 Bk e um feixe de 50 Ti para produzir o elemento 119 , mas uma vez que 249 Bk decai para 249 Cf com meia-vida de cerca de 327 dias, ambos os elementos 119 e 120 podem ser pesquisados simultaneamente. Nenhum átomo foi identificado, implicando em um limite de seção transversal de 200 fb para a reação de 249 Cf + 50 Ti.
A equipe russa do Joint Institute for Nuclear Research em Dubna , na Rússia, planejou conduzir um experimento antes de 2012, e nenhum resultado foi divulgado, o que implica fortemente que o experimento não foi realizado ou nenhum átomo de unbinilium foi identificado.
Nomeação
A nomenclatura de Mendeleev para elementos não nomeados e não descobertos chamaria unbinilium eka- radium . As recomendações da IUPAC de 1979 o chamam temporariamente de unbinilium (símbolo Ubn ) até que seja descoberto, a descoberta seja confirmada e um nome permanente seja escolhido. Embora os nomes sistemáticos da IUPAC sejam amplamente usados na comunidade química em todos os níveis, de salas de aula de química a livros didáticos avançados, os cientistas que trabalham teoricamente ou experimentalmente em elementos superpesados normalmente o chamam de "elemento 120", com o símbolo E120 , (120) ou 120 .
Propriedades previstas
Estabilidade nuclear e isótopos


A estabilidade dos núcleos diminui muito com o aumento do número atômico após o cúrio , o elemento 96, cuja meia-vida é quatro ordens de magnitude mais longa do que a de qualquer elemento de número superior conhecido atualmente. Todos os isótopos com um número atômico acima de 101 sofrem decaimento radioativo com meia-vida de menos de 30 horas. Nenhum elemento com número atômico acima de 82 (após o chumbo ) possui isótopos estáveis. No entanto, por razões ainda não bem compreendidas, há um ligeiro aumento da estabilidade nuclear em torno dos números atômicos 110 - 114 , o que leva ao surgimento do que é conhecido na física nuclear como a " ilha de estabilidade ". Este conceito, proposto por Universidade da Califórnia professor de Glenn Seaborg , explica por elementos superpesados durar mais tempo do que o previsto.
Prevê-se que os isótopos de unbinilium tenham meias-vidas de decaimento alfa da ordem de microssegundos . Em um modelo de tunelamento quântico com estimativas de massa de um modelo macroscópico-microscópico, as meias-vidas de decaimento alfa de vários isótopos de unbinilium ( 292–304 Ubn) foram previstas em cerca de 1–20 microssegundos. Alguns isótopos mais pesados podem ser mais estáveis; Fricke e Waber previram que 320 Ubn seria o isótopo de unbinilium mais estável em 1971. Uma vez que se espera que o unbinilium decaia por meio de uma cascata de decaimentos alfa, levando à fissão espontânea em torno do copernício , as meias-vidas totais dos isótopos de unbinilium também devem ser medidas em microssegundos. Isso tem consequências para a síntese do unbinilium, pois os isótopos com meia-vida abaixo de um microssegundo decaem antes de chegar ao detector. No entanto, novos modelos teóricos mostram que a lacuna esperada em energia entre os orbitais de prótons 2f 7/2 (preenchido no elemento 114) e 2f 5/2 (preenchido no elemento 120) é menor do que o esperado, de modo que o elemento 114 não parece mais ser uma camada nuclear fechada esférica estável, e esta lacuna de energia pode aumentar a estabilidade dos elementos 119 e 120. O próximo núcleo duplamente mágico agora deve estar em torno do 306 Ubb esférico (elemento 122), mas a meia-vida baixa esperada e A seção transversal de baixa produção deste nuclídeo torna sua síntese um desafio.
Dado que o elemento 120 preenche o orbital de prótons 2f 5/2 , muita atenção tem sido dada ao núcleo composto 302 Ubn * e suas propriedades. Vários experimentos foram realizados entre 2000 e 2008 no Laboratório Flerov de Reações Nucleares em Dubna estudando as características de fissão do núcleo composto 302 Ubn *. Duas reações nucleares foram utilizadas, a saber, 244 Pu + 58 Fe e 238 U + 64 Ni. Os resultados revelaram como núcleos como este fissão predominantemente pela expulsão de núcleos de concha fechada, como 132 Sn ( Z = 50, N = 82). Verificou-se também que o rendimento da via de fusão-fissão foi semelhante entre projéteis de 48 Ca e 58 Fe, sugerindo um possível uso futuro de projéteis de 58 Fe na formação de elementos superpesados.
Em 2008, a equipe do GANIL , França, descreveu os resultados de uma nova técnica que tenta medir a meia-vida de fissão de um núcleo composto com alta energia de excitação, uma vez que os rendimentos são significativamente maiores do que os dos canais de evaporação de nêutrons. É também um método útil para sondar os efeitos de fechamentos de camadas sobre a capacidade de sobrevivência de núcleos compostos na região superpesada, o que pode indicar a posição exata da próxima camada de prótons ( Z = 114, 120, 124 ou 126). A equipe estudou a reação de fusão nuclear entre íons de urânio e um alvo de níquel natural:
-
238
92você
+ nat
28Ni
→ 296.298.299.300.302
120Ubn
* → fissão
Os resultados indicaram que os núcleos de unbinilium foram produzidos com energia de excitação alta (~ 70 MeV) que sofreu fissão com meia-vida mensurável pouco mais de 10 −18 s. Embora muito curto (na verdade, insuficiente para que o elemento seja considerado pela IUPAC a existir, porque um núcleo composto não tem estrutura interna e seus núcleos não foram organizados em camadas até que tenha sobrevivido por 10-14 s, quando forma uma nuvem eletrônica ), a capacidade de medir tal processo indica um forte efeito de camada em Z = 120. Em energia de excitação mais baixa (ver evaporação de nêutrons), o efeito da camada será intensificado e os núcleos do estado fundamental podem ter metade relativamente longa -vidas. Este resultado poderia explicar parcialmente a meia-vida relativamente longa de 294 Og medida em experimentos em Dubna. Experimentos semelhantes indicaram um fenômeno semelhante no elemento 124, mas não para flerovium , sugerindo que a próxima camada de próton na verdade está além do elemento 120. Em setembro de 2007, a equipe da RIKEN iniciou um programa utilizando alvos de 248 cm e indicou experimentos futuros para sonda a possibilidade de 120 ser o próximo número mágico do próton (e 184 ser o próximo número mágico do nêutron) usando as reações nucleares mencionadas para formar 302 Ubn *, bem como 248 Cm + 54 Cr. Eles também planejaram mapear a região investigando os núcleos compostos próximos 296 Og *, 298 Og *, 306 Ubb * e 308 Ubb *.
Atômico e físico
Sendo o segundo elemento do período 8 , o unbinilium é previsto para ser um metal alcalino-terroso, abaixo do berílio , magnésio , cálcio , estrôncio , bário e rádio . Cada um desses elementos tem dois elétrons de valência no orbital s mais externo (configuração de elétrons de valência n s 2 ), que é facilmente perdido em reações químicas para formar o estado de oxidação +2 : assim, os metais alcalino-terrosos são elementos bastante reativos , com o exceção do berílio devido ao seu pequeno tamanho. Prevê-se que o unbinilium continue a tendência e tenha uma configuração eletrônica de valência de 8s 2 . Portanto, espera-se que ele se comporte de maneira muito semelhante a seus congêneres mais leves ; no entanto, também se prevê que difira dos metais alcalino-terrosos mais leves em algumas propriedades.
A principal razão para as diferenças previstas entre o unbinilium e os outros metais alcalino-terrosos é a interação spin-órbita (SO) - a interação mútua entre o movimento e o spin dos elétrons . A interação SO é especialmente forte para os elementos superpesados porque seus elétrons se movem mais rápido - em velocidades comparáveis à velocidade da luz - do que aqueles em átomos mais leves. Nos átomos de unbinilium, ele reduz os níveis de energia do elétron 7p e 8s, estabilizando os elétrons correspondentes, mas dois dos níveis de energia do elétron 7p são mais estabilizados do que os outros quatro. O efeito é chamado de divisão de subshell, pois divide o subshell 7p em partes mais estabilizadas e menos estabilizadas. Químicos computacionais entendem a divisão como uma mudança do segundo número quântico ( azimutal ) l de 1 para 1/2 e 3/2 para as partes mais estabilizadas e menos estabilizadas da subcamada 7p, respectivamente. Assim, os elétrons 8s externos do unbinilium são estabilizados e se tornam mais difíceis de remover do que o esperado, enquanto os elétrons 7p 3/2 são desestabilizados, talvez permitindo que participem de reações químicas. Essa estabilização do orbital s mais externo (já significativo no rádio) é o fator-chave que afeta a química do unbinilium e faz com que todas as tendências das propriedades atômicas e moleculares dos metais alcalino-terrosos invertam a direção após o bário.
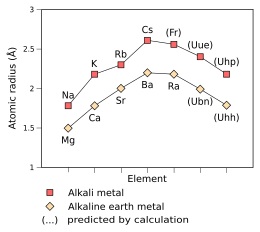
Raios atômicos empíricos (Na – Cs, Mg – Ra) e preditos (Fr – Uhp, Ubn – Uhh) dos metais alcalinos e alcalino-terrosos do terceiro ao nono período , medidos em angstroms
|
Devido à estabilização de seus elétrons 8s externos, a primeira energia de ionização do unbinilium - a energia necessária para remover um elétron de um átomo neutro - é estimada em 6,0 eV, comparável à do cálcio. O elétron do átomo de unbinilium semelhante ao hidrogênio - oxidado de modo que tenha apenas um elétron, Ubn 119+ - está previsto para se mover tão rapidamente que sua massa é 2,05 vezes a de um elétron imóvel , uma característica proveniente dos efeitos relativísticos . Para efeito de comparação, o valor para o rádio semelhante ao hidrogênio é 1,30 e o valor para o bário semelhante ao hidrogênio é 1,095. Segundo simples extrapolações das leis da relatividade, isso indiretamente indica a contração do raio atômico para cerca de 200 pm , muito próxima à do estrôncio (215 pm); o raio iônico do íon Ubn 2+ também é reduzido correspondentemente para 160 pm. A tendência na afinidade eletrônica também deve reverter a direção de forma semelhante no rádio e no unbinilium.
O unbinilium deve ser um sólido à temperatura ambiente, com ponto de fusão de 680 ° C: isso continua a tendência de queda no grupo, sendo inferior ao valor de 700 ° C para o rádio. O ponto de ebulição do unbinilium está previsto em cerca de 1700 ° C, que é inferior ao de todos os elementos anteriores do grupo (em particular, o rádio ferve a 1737 ° C), seguindo a tendência periódica decrescente. A densidade do unbinilium foi prevista em 7 g / cm 3 , continuando a tendência de aumento da densidade no grupo: o valor do rádio é de 5,5 g / cm 3 .
Químico
| Composto | Comprimento da ligação (Å) |
Energia de dissociação de ligação (eV) |
|---|---|---|
| Ca 2 | 4,277 | 0,14 |
| Sr 2 | 4,498 | 0,13 |
| Ba 2 | 4.831 | 0,23 |
| Ra 2 | 5,19 | 0,11 |
| Ubn 2 | 5,65 | 0,02 |
Prevê-se que a química do unbinilium seja semelhante à dos metais alcalino-terrosos, mas provavelmente se comportaria mais como cálcio ou estrôncio do que como bário ou rádio. Como o estrôncio, o unbinilium deve reagir vigorosamente com o ar para formar um óxido (UbnO) e com a água para formar o hidróxido (Ubn (OH) 2 ), que seria uma base forte , liberando gás hidrogênio . Ele também deve reagir com os halogênios para formar sais como UbnCl 2 . Embora essas reações fossem esperadas de tendências periódicas , sua intensidade reduzida é um tanto incomum, pois, ignorando os efeitos relativísticos, as tendências periódicas predizem que o unbinilium é ainda mais reativo do que o bário ou o rádio. Esta reatividade reduzida é devido à estabilização relativística do elétron de valência do unbinilium, aumentando a primeira energia de ionização do unbinilium e diminuindo os raios metálico e iônico ; este efeito já é visto para o rádio. a química do unbinilium no estado de oxidação +2 deve ser mais semelhante à química do estrôncio do que à do rádio. Por outro lado, o raio iônico do íon Ubn 2+ é previsto para ser maior do que o do Sr 2+ , porque os orbitais 7p são desestabilizados e são, portanto, maiores do que os orbitais p das camadas inferiores. Unbinilium também pode mostrar o estado de oxidação +4 , que não é visto em nenhum outro metal alcalino-terroso, além do estado de oxidação +2 que é característico dos outros metais alcalino-terrosos e também é o principal estado de oxidação de todos os alcalinos conhecidos metais terrestres: isso ocorre por causa da desestabilização e expansão do spinor 7p 3/2 , fazendo com que seus elétrons mais externos tenham uma energia de ionização mais baixa do que seria esperado. O estado +1 também pode ser isolável. Espera-se que muitos compostos de unbinilium tenham um grande caráter covalente , devido ao envolvimento dos elétrons 7p 3/2 na ligação: este efeito também é visto em menor extensão no rádio, que mostra uma contribuição de 6s e 6p 3/2 para a ligação em fluoreto de rádio (RaF 2 ) e astatida (RaAt 2 ), resultando nesses compostos tendo um caráter mais covalente. O potencial de redução padrão do par Ubn 2+ / Ubn é previsto em -2,9 V, que é quase exatamente o mesmo do par Sr 2+ / Sr de estrôncio (-2,899 V).
| Composto | Comprimento da ligação (Å) |
Energia de dissociação de ligação (kJ / mol) |
|---|---|---|
| CaAu | 2,67 | 2,55 |
| SrAu | 2.808 | 2,63 |
| BaAu | 2.869 | 3,01 |
| RaAu | 2,995 | 2,56 |
| UbnAu | 3.050 | 1,90 |
Na fase gasosa, os metais alcalino-terrosos geralmente não formam moléculas diatômicas covalentemente ligadas como os metais alcalinos, uma vez que tais moléculas teriam o mesmo número de elétrons nos orbitais de ligação e anti-ligação e teriam energias de dissociação muito baixas . Assim, a ligação M – M nessas moléculas é predominantemente por meio de forças de van der Waals . Os comprimentos das ligações metal-metal nessas moléculas M 2 aumentam no grupo de Ca 2 a Ubn 2 . Por outro lado, suas energias de dissociação de ligação metal-metal geralmente aumentam de Ca 2 para Ba 2 e então caem para Ubn 2 , que deve ser a ligação mais fraca de todas as moléculas homodiatômicas do grupo 2. A causa desta tendência é a participação crescente dos elétrons p 3/2 ed, bem como do orbital s contraído relativisticamente. A partir destas H 2 energias de dissociação, a entalpia de sublimação (Δ H sub ) de unbinílio está previsto para ser de 150 kJ / mol.
| Composto | Comprimento da ligação (Å) |
Frequência harmônica , cm -1 |
Anarmonicidade vibracional, cm -1 |
Energia de dissociação de ligação (eV) |
|---|---|---|---|---|
| UbnH | 2,38 | 1070 | 20,1 | 1,00 |
| BaH | 2,23 | 1168 | 14,5 | 2.06 |
| UbnAu | 3,03 | 100 | 0,13 | 1,80 |
| BaAu | 2,91 | 129 | 0,18 | 2,84 |
A ligação Ubn– Au deve ser a mais fraca de todas as ligações entre o ouro e um metal alcalino-terroso, mas ainda deve ser estável. Isso dá entalpias de adsorção extrapoladas de tamanho médio (−Δ H ads ) de 172 kJ / mol em ouro (o valor do rádio deve ser 237 kJ / mol) e 50 kJ / mol em prata , o menor de todos os metais alcalino-terrosos, que demonstrar que seria viável estudar a adsorção cromatográfica do unbinilium em superfícies feitas de metais nobres . Os valores de Δ H sub e −Δ H ads são correlacionados para os metais alcalino-terrosos.
Veja também
- Ilha de estabilidade : flerovium - unbinilium - unbihexium
Notas
Referências
Bibliografia
- Audi, G .; Kondev, FG; Wang, M .; Huang, WJ; Naimi, S. (2017). "A avaliação NUBASE2016 das propriedades nucleares" (PDF) . Chinese Física C . 41 (3): 030001. bibcode : 2017ChPhC..41c0001A . doi : 10.1088 / 1674-1137 / 41/3/030001 .
- Beiser, A. (2003). Conceitos de física moderna (6ª ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418 .
- Hoffman, DC ; Ghiorso, A .; Seaborg, GT (2000). The Transuranium People: The Inside Story . World Scientific . ISBN 978-1-78-326244-1.
- Kragh, H. (2018). De elementos transurânicos a superpesados: uma história de disputa e criação . Springer . ISBN 978-3-319-75813-8.
- Zagrebaev, V .; Karpov, A .; Greiner, W. (2013). "Futuro da pesquisa com elementos superpesados: quais núcleos poderiam ser sintetizados nos próximos anos?" (PDF) . Journal of Physics: Conference Series . 420 . 012001. arXiv : 1207.5700 . Bibcode : 2013JPhCS.420a2001Z . doi : 10.1088 / 1742-6596 / 420/1/012001 . ISSN 1742-6588 . S2CID 55434734 .


