Triptofano - Tryptophan

Fórmula esquelética de L- triptofano
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Triptofano ou ácido ( 2S ) -2-amino-3- (1 H -indol-3-il) propanóico
|
|||
| Outros nomes
Ácido 2-amino-3- (1 H -indol-3-il) propanóico
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.723 |
||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 11 H 12 N 2 O 2 | |||
| Massa molar | 204,229 g · mol −1 | ||
| Solúvel: 0,23 g / L a 0 ° C, 11,4 g / L a 25 ° C, |
|||
| Solubilidade | Solúvel em álcool quente, hidróxidos alcalinos; insolúvel em clorofórmio . | ||
| Acidez (p K a ) | 2,38 (carboxil), 9,39 (amino) | ||
| -132,0 · 10 −6 cm 3 / mol | |||
| Farmacologia | |||
| N06AX02 ( OMS ) | |||
| Página de dados suplementares | |||
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|||
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
||
| UV , IR , NMR , MS | |||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Triptofano (símbolo Trp ou W ) é um α- aminoácido usado na biossíntese de proteínas . O triptofano contém um grupo α-amino, um grupo de ácido α- carboxílico e um indol de cadeia lateral , tornando-o um aminoácido aromático apolar . É essencial no ser humano, o que significa que o corpo não consegue sintetizá-lo e deve ser obtido a partir da alimentação. O triptofano também é um precursor do neurotransmissor serotonina , do hormônio melatonina e da vitamina B3 . É codificado pelo códon UGG.
Como outros aminoácidos, o triptofano é um zwitterion em pH fisiológico onde o grupo amino é protonado (- NH+
3; pK a = 9,39) e o ácido carboxílico é desprotonado (–COO - ; pK a = 2,38).
Função
Os aminoácidos, incluindo o triptofano, são usados como blocos de construção na biossíntese de proteínas , e as proteínas são necessárias para sustentar a vida. Muitos animais (incluindo humanos) não podem sintetizar triptofano: eles precisam obtê-lo por meio de sua dieta, tornando-o um aminoácido essencial . O triptofano está entre os aminoácidos menos comuns encontrados nas proteínas, mas desempenha importantes papéis estruturais ou funcionais sempre que ocorre. Por exemplo, resíduos de triptofano e tirosina desempenham papéis especiais na "ancoragem" de proteínas de membrana dentro da membrana celular . O triptofano, junto com outros aminoácidos aromáticos , também é importante nas interações glicano-proteína . Além disso, o triptofano funciona como um precursor bioquímico para os seguintes compostos :
- Serotonina (um neurotransmissor ), sintetizada pela triptofano hidroxilase .
- A melatonina (um neuro - hormônio ) é, por sua vez, sintetizada a partir da serotonina, por meio das enzimas N-acetiltransferase e 5-hidroxiindol-O-metiltransferase .
- Quinurenina , para a qual o triptofano é principalmente (mais de 95%) metabolizado. Duas enzimas, a saber, indoleamina 2,3-dioxigenase (IDO) no sistema imunológico e no cérebro, e triptofano dioxigenase (TDO) no fígado, são responsáveis pela síntese de quinurenina a partir do triptofano. A via da quinurenina do catabolismo do triptofano é alterada em várias doenças, incluindo transtornos psiquiátricos como esquizofrenia, transtorno depressivo maior e transtorno bipolar.
- A niacina , também conhecida como vitamina B 3 , é sintetizada a partir do triptofano via quinurenina e ácidos quinolínicos .
- As auxinas (uma classe de fitohormônios ) são sintetizadas a partir do triptofano.
O distúrbio, má absorção de frutose, causa absorção inadequada de triptofano no intestino, níveis reduzidos de triptofano no sangue e depressão.
Em bactérias que sintetizam triptofano, altos níveis celulares desse aminoácido ativam uma proteína repressora , que se liga ao operon trp . A ligação desse repressor ao operon do triptofano impede a transcrição do DNA a jusante que codifica as enzimas envolvidas na biossíntese do triptofano. Portanto, altos níveis de triptofano impedem a síntese de triptofano por meio de um ciclo de feedback negativo e, quando os níveis de triptofano da célula voltam a baixar, a transcrição do operon trp é retomada. Isso permite respostas rígidas e rápidas às mudanças nos níveis de triptofano interno e externo da célula.
|
Metabolismo do triptofano pela microbiota gastrointestinal humana (
)
|
Ingestão diária recomendada
Em 2002, o Instituto de Medicina dos Estados Unidos estabeleceu uma Dieta Diária Recomendada (RDA) de 5 mg / kg de peso corporal / dia de triptofano para adultos com 19 anos ou mais.
Fontes dietéticas
O triptofano está presente na maioria dos alimentos à base de proteínas ou proteínas dietéticas. É particularmente abundante em chocolate , aveia , tâmaras secas , leite , iogurte , queijo cottage , carne vermelha , ovos , peixes , aves , gergelim , grão de bico , amêndoas , sementes de girassol , sementes de abóbora , trigo sarraceno , espirulina e amendoim . Ao contrário da crença popular de que o peru cozido contém uma abundância de triptofano, o conteúdo de triptofano no peru é típico das aves.
| Comida | Triptofano [g / 100 g de alimento] |
Proteína [g / 100 g de alimento] |
Triptofano / proteína [%] |
|---|---|---|---|
| Clara de ovo seca | 1,00 | 81,10 | 1,23 |
| Espirulina seca | 0,92 | 57,47 | 1,62 |
| Bacalhau, atlântico , seco | 0,70 | 62,82 | 1,11 |
| Soja , crua | 0,59 | 36,49 | 1,62 |
| Queijo, Parmesão | 0,56 | 37,90 | 1,47 |
| Sementes de chia , secas | 0,436 | 16,5 | 2,64 |
| Semente de gergelim | 0,37 | 17,00 | 2,17 |
| Queijo, Cheddar | 0,32 | 24,90 | 1,29 |
| Semente de girassol | 0,30 | 17,20 | 1,74 |
| Costelinha de porco | 0,25 | 19,27 | 1,27 |
| Turquia | 0,24 | 21,89 | 1,11 |
| Frango | 0,24 | 20,85 | 1,14 |
| Carne | 0,23 | 20,13 | 1,12 |
| Aveia | 0,23 | 16,89 | 1,39 |
| Salmão | 0,22 | 19,84 | 1,12 |
| Costeleta de cordeiro | 0,21 | 18,33 | 1,17 |
| Poleiro, Atlântico | 0,21 | 18,62 | 1,12 |
| Grão de bico cru | 0,19 | 19,30 | 0,96 |
| Ovo | 0,17 | 12,58 | 1,33 |
| Farinha de trigo, branca | 0,13 | 10,33 | 1,23 |
| Chocolate assado sem açúcar | 0,13 | 12,9 | 1,23 |
| Leite | 0,08 | 3,22 | 2,34 |
| Arroz, branco, grão médio, cozido | 0,028 | 2,38 | 1,18 |
| Quinoa , crua | 0,167 | 14,12 | 1,2 |
| Quinoa cozida | 0,052 | 4,40 | 1,1 |
| Batatas, castanho-avermelhado | 0,02 | 2,14 | 0,84 |
| Tamarindo | 0,018 | 2,80 | 0,64 |
| Banana | 0,01 | 1.03 | 0,87 |
Use como um antidepressivo
Como o triptofano é convertido em 5-hidroxitriptofano (5-HTP), que é então convertido no neurotransmissor serotonina, foi proposto que o consumo de triptofano ou 5-HTP pode melhorar os sintomas de depressão, aumentando o nível de serotonina no cérebro. O triptofano é vendido sem receita nos Estados Unidos (depois de ter sido banido em vários graus entre 1989 e 2005 ) e no Reino Unido como um suplemento dietético para uso como antidepressivo , ansiolítico e auxiliar para dormir . Também é comercializado como medicamento sob prescrição em alguns países europeus para o tratamento da depressão maior . Há evidências de que é improvável que os níveis de triptofano no sangue sejam alterados com a mudança da dieta, mas consumir triptofano purificado aumenta o nível de serotonina no cérebro, ao passo que comer alimentos contendo triptofano não. Isso ocorre porque o sistema de transporte que leva o triptofano através da barreira hematoencefálica também transporta outros aminoácidos contidos nas fontes de proteína alimentar . Níveis elevados de outros aminoácidos neutros grandes no plasma sanguíneo impedem que a concentração plasmática de triptofano aumente os níveis de concentração cerebral.
Em 2001, uma revisão da Cochrane sobre o efeito do 5-HTP e do triptofano na depressão foi publicada. Os autores incluíram apenas estudos de alto rigor e incluíram tanto o 5-HTP quanto o triptofano em sua revisão devido aos dados limitados de ambos. Dos 108 estudos de 5-HTP e triptofano na depressão publicados entre 1966 e 2000, apenas dois atenderam aos padrões de qualidade dos autores para inclusão, totalizando 64 participantes do estudo. As substâncias foram mais eficazes do que o placebo nos dois estudos incluídos, mas os autores afirmam que "a evidência era de qualidade insuficiente para ser conclusiva" e observam que "porque existem antidepressivos alternativos que foram comprovados como eficazes e seguros, a utilidade clínica de O 5-HTP e o triptofano são limitados atualmente ". O uso de triptofano como terapia adjuvante, além do tratamento padrão para transtornos de humor e ansiedade, não é apoiado por evidências científicas.
Efeitos colaterais
Os potenciais efeitos colaterais da suplementação de triptofano incluem náusea , diarreia , sonolência , tontura , dor de cabeça , boca seca , visão turva , sedação , euforia e nistagmo (movimentos involuntários dos olhos).
Interações
O triptofano tomado como suplemento dietético (como na forma de comprimido) tem o potencial de causar a síndrome da serotonina quando combinado com antidepressivos da classe IMAO ou ISRS ou outras drogas fortemente serotoninérgicas. Como a suplementação de triptofano não foi completamente estudada em um ambiente clínico, suas interações com outras drogas não são bem conhecidas.
Isolamento
O isolamento do triptofano foi relatado pela primeira vez por Frederick Hopkins em 1901. Hopkins recuperou o triptofano da caseína hidrolisada , recuperando 4-8 g de triptofano de 600 g de caseína bruta.
Biossíntese e produção industrial
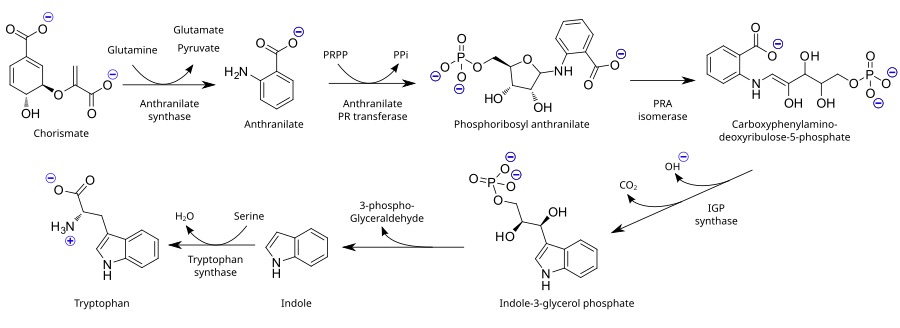
Como um aminoácido essencial, o triptofano não é sintetizado a partir de substâncias mais simples em humanos e outros animais, por isso precisa estar presente na dieta na forma de proteínas contendo triptofano. Plantas e microrganismos comumente sintetizam triptofano a partir de ácido chiquímico ou antranilato : o antranilato condensa-se com fosforibosilpirofosfato (PRPP), gerando pirofosfato como subproduto. O anel da porção ribose é aberto e sujeito a descarboxilação redutiva , produzindo fosfato de indol-3-glicerol; este, por sua vez, é transformado em indol . Na última etapa, a triptofano sintase catalisa a formação de triptofano a partir do indol e do aminoácido serina .
A produção industrial de triptofano também é biossintética e é baseada na fermentação de serina e indol usando bactérias do tipo selvagem ou geneticamente modificadas , como B. amyloliquefaciens , B. subtilis , C. glutamicum ou E. coli . Essas cepas carregam mutações que impedem a recaptação de aminoácidos aromáticos ou operons trp múltiplos / superexpressos . A conversão é catalisada pela enzima triptofano sintase .
Sociedade e cultura
Síndrome de eosinofilia-mialgia
Houve um grande surto de síndrome de eosinofilia-mialgia (EMS) nos Estados Unidos em 1989, com mais de 1.500 casos relatados ao CDC e pelo menos 37 mortes. Depois que uma investigação preliminar revelou que o surto estava relacionado à ingestão de triptofano, a Food and Drug Administration (FDA) dos EUA fez um recall dos suplementos de triptofano em 1989 e proibiu a maioria das vendas públicas em 1990, com outros países seguindo o exemplo.
Estudos subsequentes sugeriram que o EMS estava ligado a lotes específicos de L-triptofano fornecidos por um único grande fabricante japonês, a Showa Denko . Por fim, ficou claro que lotes recentes de L-triptofano da Showa Denko estavam contaminados por traços de impurezas, que foram posteriormente considerados responsáveis pelo surto de EMS em 1989. No entanto, outras evidências sugerem que o próprio triptofano pode ser um fator potencialmente importante de contribuição na EMS.
O FDA afrouxou suas restrições sobre vendas e marketing de triptofano em fevereiro de 2001, mas continuou a limitar a importação de triptofano não destinado a um uso isento até 2005.
O fato de que a instalação da Showa Denko usou bactérias geneticamente modificadas para produzir os lotes contaminados de L-triptofano que mais tarde se descobriu ter causado o surto da síndrome de eosinofilia-mialgia foi citado como evidência da necessidade de "monitoramento rigoroso da pureza química da biotecnologia produtos derivados ". Aqueles que pedem monitoramento de pureza, por sua vez, foram criticados como ativistas anti- OGM que negligenciam as possíveis causas de contaminação não-OGM e ameaçam o desenvolvimento da biotecnologia.
Carne de peru e sonolência
Uma afirmação comum nos Estados Unidos é que o consumo excessivo de carne de peru resulta em sonolência , devido aos altos níveis de triptofano contidos no peru. No entanto, a quantidade de triptofano na Turquia é comparável à contida em outras carnes. A sonolência após comer pode ser causada por outros alimentos ingeridos com o peru, principalmente carboidratos . A ingestão de uma refeição rica em carboidratos desencadeia a liberação de insulina . A insulina, por sua vez, estimula a absorção de grandes aminoácidos neutros de cadeia ramificada (BCAA), mas não o triptofano, para o músculo, aumentando a proporção de triptofano para BCAA na corrente sanguínea. O aumento da proporção de triptofano resultante reduz a competição no grande transportador de aminoácidos neutros (que transporta BCAA e aminoácidos aromáticos), resultando em maior captação de triptofano através da barreira hematoencefálica para o líquido cefalorraquidiano (LCR). Uma vez no LCR, o triptofano é convertido em serotonina nos núcleos da rafe pela via enzimática normal. A serotonina resultante é posteriormente metabolizada em melatonina pela glândula pineal . Conseqüentemente, esses dados sugerem que a "sonolência induzida pelo banquete" - ou sonolência pós-prandial - pode ser o resultado de uma refeição pesada rica em carboidratos, o que indiretamente aumenta a produção de melatonina no cérebro e, portanto, promove o sono.
Pesquisar
Em 1912, Felix Ehrlich demonstrou que a levedura metaboliza os aminoácidos naturais essencialmente separando o dióxido de carbono e substituindo o grupo amino por um grupo hidroxila . Por essa reação , o triptofano dá origem ao triptofol .
O triptofano afeta a síntese de serotonina no cérebro quando administrado por via oral em uma forma purificada e é usado para modificar os níveis de serotonina para fins de pesquisa. O baixo nível de serotonina no cérebro é induzido pela administração de proteína pobre em triptofano em uma técnica chamada depleção aguda de triptofano . Estudos usando este método avaliaram o efeito da serotonina no humor e no comportamento social, descobrindo que a serotonina reduz a agressão e aumenta a simpatia.
Fluorescência
O triptofano é uma importante sonda fluorescente intrínseca (aminoácido), que pode ser usada para estimar a natureza do microambiente em torno do resíduo de triptofano. A maioria das emissões de fluorescência intrínseca de uma proteína dobrada são devidas à excitação de resíduos de triptofano.
Veja também
- 5-hidroxitriptofano (5-HTP)
- Reação Acree-Rosenheim
- Reação de Adamkiewicz
- Atenuador (genética)
- N , N- Dimetiltriptamina
- Reação de Hopkins-Cole
- Serotonina
- Triptamina
Referências
Leitura adicional
- Wood RM, Rilling JK, Sanfey AG, Bhagwagar Z, Rogers RD (maio de 2006). "Efeitos da depleção de triptofano no desempenho de um jogo iterado do Dilema do Prisioneiro em adultos saudáveis" . Neuropsicofarmacologia . 31 (5): 1075–84. doi : 10.1038 / sj.npp.1300932 . PMID 16407905 .
links externos
- "CAMINHO DE KEGG: Metabolismo do triptofano - Homo sapiens" . KEGG: Enciclopédia de genes e genomas de Kyoto. 23 de agosto de 2006 . Página visitada em 20 de abril de 2008 .
- GP Moss. "Catabolismo do triptofano (estágios iniciais)" . Comitê de Nomenclatura da União Internacional de Bioquímica e Biologia Molecular (NC-IUBMB). Arquivado do original em 13 de setembro de 2003 . Página visitada em 20 de abril de 2008 .
- GP Moss. "Catabolismo do triptofano (fases posteriores)" . Comitê de Nomenclatura da União Internacional de Bioquímica e Biologia Molecular (NC-IUBMB). Arquivado do original em 13 de setembro de 2003 . Página visitada em 20 de abril de 2008 .
- B. Mikkelson; DP Mikkelson (22 de novembro de 2007). "O peru causa sonolência" . Páginas de referência de lendas urbanas . Snopes.com . Página visitada em 20 de abril de 2008 .