Persulfato de sódio - Sodium persulfate

|
|

|
|

|
|
| Nomes | |
|---|---|
| Outros nomes
Peroxodissulfato de sódio Peroxodissulfato de
sódio Peroxidissulfato de sódio Peroxidissulfato de sódio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.028.993 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1505 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Na 2 S 2 O 8 | |
| Massa molar | 238,10 g / mol |
| Aparência | pó branco |
| Densidade | 2,59 g / cm 3 (densidade aparente solta: 1,12 g / cm 3 ) |
| Ponto de fusão | 180 ° C (356 ° F; 453 K) se decompõe |
| 55,6 g / 100 ml (20 ° C) | |
| Perigos | |
| Ficha de dados de segurança | ICSC 1136 |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H272 , H302 , H315 , H317 , H319 , H334 , H335 , H371 | |
| P220 , P261 , P280 , P305 + 351 + 338 , P342 + 311 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Compostos relacionados | |
|
Outros ânions
|
Ditionito de sódio Sulfito de sódio Sulfato de sódio |
|
Outros cátions
|
Persulfato de potássio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Persulfato de sódio é o composto inorgânico com a fórmula Na 2 S 2 O 8 . É o sal de sódio do ácido peroxidissulfúrico , H 2 S 2 O 8 , um agente oxidante . É um sólido branco que se dissolve na água. É quase não higroscópico e tem boa vida útil.
Produção
O sal é preparado pela oxidação eletrolítica do hidrogenossulfato de sódio :
- 2 NaHSO 4 → Na 2 S 2 O 8 + H 2
A oxidação é conduzida em um ânodo de platina. Desta forma, cerca de 165.000 toneladas foram produzidas em 2005.
O potencial redox padrão do persulfato de sódio em sulfato de hidrogênio é 2,1 V, que é maior que o do peróxido de hidrogênio (1,8 V), mas menor que o ozônio (2,2 V). O radical sulfato formado in situ tem um potencial de eletrodo padrão de 2,7 V.
No entanto, existem algumas desvantagens na utilização de ânodos de platina para produzir os sais; o processo de fabricação é ineficiente devido à evolução do oxigênio e o produto pode conter contaminantes provenientes da corrosão da platina (principalmente devido à natureza extremamente oxidante do radical sulfato). Assim, eletrodos de diamante dopados com boro têm sido propostos como alternativas aos eletrodos convencionais de platina.
Formulários
É usado principalmente como um iniciador radical para reações de polimerização em emulsão para polímeros à base de estireno , como acrilonitrila butadieno estireno . Também aplicável para cura acelerada de adesivos com baixo teor de formaldeído .
Outros usos
É um alvejante , tanto autônomo (principalmente em cosméticos para cabelos) quanto um componente detergente . É um substituto para o persulfato de amônio em misturas de corrosão para zinco e placas de circuito impresso e é usado para decapagem de cobre e alguns outros metais.
Ele também é usado como um condicionador de solo e para remediação de solo e água subterrânea e na fabricação de corantes , modificação de amido , ativador de branqueamento , agente de desengomagem para desengomagem oxidativa, etc.
Química orgânica
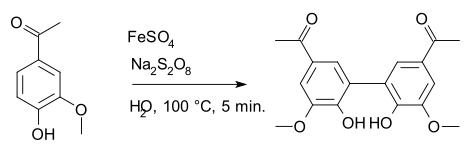
O persulfato de sódio é um agente oxidante especializado em química , classicamente na oxidação do persulfato Elbs e nas reações de oxidação de Boyland-Sims . Também é usado em reações radicais; por exemplo, em uma síntese de diapocinina a partir da apocinina, onde o sulfato de ferro (II) é o iniciador radical.
Segurança
O sal é um oxidante e forma misturas combustíveis com materiais orgânicos como o papel. Agentes redutores fortes, como magnésio, podem formar composições explosivas quando misturados.