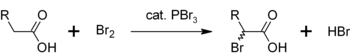Tribrometo de fósforo - Phosphorus tribromide

|
|

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Tribrometo de fósforo
|
|
| Outros nomes
brometo de fósforo (III),
brometo de fósforo, tribromofosfina |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.029.253 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| PBr 3 | |
| Massa molar | 270,69 g / mol |
| Aparência | líquido claro e incolor |
| Densidade | 2,852 g / cm 3 |
| Ponto de fusão | −41,5 ° C (−42,7 ° F; 231,7 K) |
| Ponto de ebulição | 173,2 ° C (343,8 ° F; 446,3 K) |
| hidrólise rápida | |
|
Índice de refração ( n D )
|
1.697 |
| Viscosidade | 0,001302 Pas |
| Estrutura | |
| trigonal piramidal | |
| Perigos | |
| Ficha de dados de segurança | Veja: página de dados |
|
|
|
| Frases R (desatualizado) | R14 , R34 , R37 |
| Frases S (desatualizado) | (S1 / 2) , S26 , S45 |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros ânions
|
trifluoreto de fósforo tricloreto de fósforo triiodeto de fósforo |
|
Outros cátions
|
tribrometo de nitrogênio arsênico tribrometo tribrometo de antimônio |
|
Compostos relacionados
|
pentabrometo de fósforo oxibrometo de fósforo |
| Página de dados suplementares | |
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
| UV , IR , NMR , MS | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O tribrometo de fósforo é um líquido incolor com a fórmula P Br 3 . O líquido fumega no ar úmido devido à hidrólise e tem um odor penetrante. É usado em laboratório para a conversão de álcoois em brometos de alquila .
Preparação
PBr 3 é preparado tratando fósforo vermelho com bromo . Um excesso de fósforo é usado para prevenir a formação de PBr 5 :
- 2 P + 3 Br 2 → 2 PBr 3
Como a reação é altamente exotérmica, muitas vezes é conduzida na presença de um diluente como PBr 3 .
Reações
O tribrometo de fósforo, como o PCl 3 e o PF 3 , tem propriedades tanto de base de Lewis quanto de ácido de Lewis . Por exemplo, com um ácido de Lewis, como tribrometo de boro, ele forma adutos 1: 1 estáveis, como Br 3 B · PBr 3 . Ao mesmo tempo, o PBr 3 pode reagir como eletrófilo ou ácido de Lewis em muitas de suas reações, por exemplo, com aminas .
A reação mais importante de PBr 3 é com álcoois , onde substitui um grupo OH por um átomo de bromo para produzir um brometo de alquila . Todos os três brometos podem ser transferidos.
- PBr 3 + 3 ROH → 3 RBr + HP (O) (OH) 2
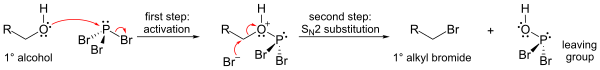
O mecanismo (mostrado para um álcool primário) envolve a formação de um éster de fósforo (para formar um bom grupo de saída), seguido por uma substituição S N 2 .
Por causa da etapa de substituição S N 2, a reação geralmente funciona bem para álcoois primários e secundários , mas falha para álcoois terciários. Se o centro do carbono reagente for quiral , a reação geralmente ocorre com inversão da configuração no carbono alfa do álcool , como é usual com uma reação S N 2.
Em uma reação semelhante, PBr 3 também converte ácidos carboxílicos em brometos de acila .
- PBr 3 + 3 RCOOH → 3 RCOBr + HP (O) (OH) 2
Formulários
O principal uso do tribrometo de fósforo é para a conversão de álcoois primários ou secundários em brometos de alquila , conforme descrito acima . PBr 3 geralmente dá rendimentos mais elevados do que o ácido bromídrico e evita problemas de rearranjo de carbocátions - por exemplo, até mesmo o brometo de neopentila pode ser feito a partir do álcool com 60% de rendimento.
Outro uso para PBr 3 é como um catalisador para a α-brominação de ácidos carboxílicos . Embora os brometos de acila raramente sejam feitos em comparação com os cloretos de acila , eles são usados como intermediários na halogenação de Hell-Volhard-Zelinsky . Inicialmente o PBr 3 reage com o ácido carboxílico para formar o brometo de acila, que é mais reativo à bromação. O processo geral pode ser representado como
Em escala comercial, o tribrometo de fósforo é usado na fabricação de produtos farmacêuticos como alprazolam , metoexital e fenoprofeno . É também um potente agente de supressão de incêndio comercializado sob o nome de PhostrEx .
Precauções
PBr 3 desenvolve HBr corrosivo, que é tóxico, e reage violentamente com água e álcoois.
- PBr 3 + 3 H 2 O → H 3 PO 3 + 3 HBr
Em reações que produzem ácido fosforoso como subproduto, ao trabalhar por destilação, esteja ciente de que este pode se decompor acima de 160 ° C para dar fosfina que pode causar explosões em contato com o ar.
Referências
Leitura adicional
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Lide, DR, ed. (1990). Handbook of Chemistry and Physics (71ª ed.). Ann Arbor, MI: CRC Press. ISBN 978-0849304712.
- March, J. (1992). Advanced Organic Chemistry (4ª ed.). Nova York: Wiley. p. 723 . ISBN 978-0471601807.
- Stecher, PG, ed. (1960). The Merck Index (7ª ed.). Rahway, NJ, EUA: Merck & Co.
- Holmes, RR (1960). "Um Exame da Natureza Básica dos Trihalides de Fósforo, Arsênico e Antimônio". Journal of Inorganic and Nuclear Chemistry . 12 (3–4): 266–275. doi : 10.1016 / 0022-1902 (60) 80372-7 .