Lactoperoxidase - Lactoperoxidase
A lactoperoxidase é uma enzima peroxidase secretada pelas glândulas mamárias, salivares e outras glândulas mucosas, incluindo os pulmões, brônquios e nariz, que funciona como uma linha natural e de primeira linha de defesa contra agentes antibacterianos e antivirais. A lactoperoxidase é um membro da família de enzimas heme peroxidase . Em humanos, a lactoperoxidase é codificada pelo gene LPO .
A lactoperoxidase catalisa a oxidação de vários substratos inorgânicos e orgânicos pelo peróxido de hidrogênio . Esses substratos incluem brometo e iodeto e, portanto, a lactoperoxidase pode ser categorizada como haloperoxidase . Um outro substrato importante é o tiocianato . Os produtos oxidados produzidos pela ação dessa enzima possuem atividades bactericidas e antivirais potentes e inespecíficas , incluindo a destruição do vírus influenza. A lactoperoxidase junto com seus substratos de íons inorgânicos, peróxido de hidrogênio e produtos oxidados é conhecido como sistema lactoperoxidase . Portanto, o LPO é considerado uma defesa muito importante contra bactérias invasivas e agentes virais, como a gripe e o vírus SARS-CoV-2, quando é fornecido iodo suficiente.
O sistema lactoperoxidase desempenha um papel importante no sistema imunológico inato matando bactérias no leite e mucosas (revestimentos de origem principalmente endodérmica, cobertos por epitélio, que estão envolvidos na absorção e secreção) secreções, portanto, o aumento do sistema lactoperoxidase pode ter aplicações terapêuticas. Além disso, a adição ou aumento do sistema lactoperoxidase tem aplicações potenciais no controle de bactérias em alimentos e produtos de saúde de consumo. O sistema da lactoperoxidase não ataca o DNA e não é mutagênico. No entanto, sob certas condições, o sistema lactoperoxidase pode contribuir para o estresse oxidativo. Além disso, a lactoperoxidase pode contribuir para o início do câncer de mama , por meio de sua capacidade de oxidar hormônios estrogênicos produtores de intermediários de radicais livres .
Estrutura
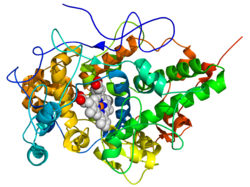
A estrutura da lactoperoxidase consiste principalmente em alfa-hélices mais duas curtas fitas beta antiparalelas . A lactoperoxidase pertence à família heme peroxidase de enzimas de mamíferos que também inclui mieloperoxidase (MPO), eosinófila peroxidase (EPO), tireoide peroxidase (TPO) e prostaglandina H sintase (PGHS). Um cofator heme está ligado próximo ao centro da proteína.
Função
A lactoperoxidase catalisa a oxidação do peróxido de hidrogênio (H 2 O 2 ) de várias moléculas aceitadoras:
- aceptor reduzido + H 2 O 2 → aceptor oxidado + H 2 O
Exemplos específicos incluem:
- tiocianato (SCN - ) → hipotiocianito (OSCN - )
- brometo (Br - ) → hipobromito (BrO - )
- iodeto (I - ) → hipoiodito (IO - )
A fonte do peróxido de hidrogênio (H 2 O 2 ) geralmente é a reação da glicose com o oxigênio na presença da enzima glicose oxidase ( EC 1.1.3.4 ) que também ocorre na saliva . A glicose, por sua vez, pode ser formada a partir do amido na presença da enzima saliva amiloglucosidase ( EC 3.2.1.3 ).
Esses intermediários oxidados de vida relativamente curta têm efeitos bactericidas potentes , portanto, a lactoperoxidase é parte do sistema de defesa antimicrobiano em tecidos que expressam lactoperoxidase. O sistema lactoperoxidase é eficaz na eliminação de uma variedade de microorganismos aeróbios e alguns anaeróbios . Pesquisa (1984): "O efeito das misturas de lactoperoxidase-tiocianato-peróxido de hidrogênio nas bactérias depende de condições experimentais. Se as bactérias forem cultivadas após a exposição à lactoperoxidase-tiocianato-peróxido de hidrogênio no ágar nutriente sob condições aeróbias, elas podem não crescer , enquanto eles crescem prontamente em ágar sangue sob condições anaeróbicas. " Em sua capacidade antimicrobiana, a lactoperoxidase parece atuar sinergicamente com a lactoferrina e a lisozima .
Formulários
A lactoperoxidase é um agente antimicrobiano e antiviral eficaz. Consequentemente, as aplicações da lactoperoxidase estão sendo encontradas na preservação de alimentos, cosméticos e soluções oftálmicas. Além disso, a lactoperoxidase encontrou aplicação no tratamento dentário e de feridas. Finalmente, a lactoperoxidase pode encontrar aplicação como agentes antitumorais e antivirais. A lactoperoxidase tem sido usada com iodo radioativo para rotular seletivamente as superfícies da membrana.
Lacticínios
A lactoperoxidase é um agente antimicrobiano eficaz e é usada como agente antibacteriano na redução da microflora bacteriana no leite e produtos lácteos. A ativação do sistema lactoperoxidase pela adição de peróxido de hidrogênio e tiocianato estende a vida útil do leite cru refrigerado. É bastante resistente ao calor e é usado como um indicador de sobrepasteurização do leite.
Higiene bucal
Um sistema lactoperoxidase é considerado apropriado para o tratamento de gengivite e paradentosis . A lactoperoxidase tem sido usada em dentifrícios ou enxaguatórios bucais para reduzir as bactérias orais e, consequentemente, o ácido produzido por essas bactérias.
Cosméticos
Uma combinação de lactoperoxidase, glicose, glicose oxidase (GOD), iodeto e tiocianato é considerada eficaz na preservação de cosméticos.
Câncer
Verificou-se que os conjugados de anticorpos de glicose oxidase e lactoperoxidase são eficazes em matar células tumorais in vitro. Além disso, os macrófagos expostos à lactoperoxidase são estimulados a matar as células cancerosas.
Significado clínico
Sistema imunológico inato
As atividades antibacteriana e antiviral da lactoperoxidase desempenham um papel importante no sistema de defesa imunológico dos mamíferos; o sistema lactoperoxidase é considerado a primeira linha de defesa contra bactérias aerotransportadas e agentes virais. É importante ressaltar que a lactoperoxidase também é expelida para o pulmão, brônquios e muco nasal.
A hipotiocianito é um dos intermediários reativos produzidos pela atividade da lactoperoxidase sobre o tiocianato e o peróxido de hidrogênio produzidos pelas proteínas oxidase 2 dupla , também conhecidas como Duox2. A secreção de tiocianato em pacientes com fibrose cística é diminuída, resultando em uma produção reduzida do hipotiocianito antimicrobiano e, consequentemente, contribui para o aumento do risco de infecção das vias aéreas.
Infecções virais
O ácido hipoiodoso gerado pela peroxidase (HOI), o hipoiodito e o hipotiocianito destroem o vírus herpes simplex e o vírus da imunodeficiência humana . Tanto o hipotiocianito quanto os produtos de íon hipoiodato são oxidantes antivirais muito potentes e, de maneira importante, não específicos, que são letais, mesmo em pequenas concentrações, para o vírus da gripe. A atividade antiviral da lactoperoxidase é aumentada com o aumento das concentrações de íon iodeto. Esta enzima se mostrou eficaz contra um vírus de RNA altamente perigoso e resistente (poliovírus) e um vírus de DNA de longa vida (vacina).
Infecções bacterianas
Foi demonstrado que o sistema duox2-lactoperoxidase oferece proteção contra muitas dezenas de bactérias e micoplasmas, incluindo variedades de Staphylococcus clinicamente importantes e muitos tipos de Streptococcus . O sistema da lactoperoxidase inibe com eficiência o helicobacter pylori comum no tampão; entretanto, em toda a saliva humana, parece ter um efeito mais fraco contra esse micróbio. Foi demonstrado que a lactoperoxidase na presença de tiocianeto pode catalisar os efeitos bactericidas e citotóxicos do peróxido de hidrogênio sob condições específicas quando o peróxido de hidrogênio está presente em excesso de tiocianeto. A combinação de lactoperoxidase, peróxido de hidrogênio e tiocianeto é muito mais eficaz do que o peróxido de hidrogênio sozinho para inibir o metabolismo e o crescimento bacteriano.
Câncer de mama
A oxidação do estradiol pela lactoperoxidase é uma possível fonte de estresse oxidativo no câncer de mama . A capacidade da lactoperoxidase de propagar uma reação em cadeia que leva ao consumo de oxigênio e ao acúmulo de peróxido de hidrogênio intracelular poderia explicar as lesões de base de DNA induzidas por radicais hidroxila recentemente relatadas em tecido feminino de câncer de mama. A lactoperoxidase pode estar envolvida na carcinogênese mamária, devido à sua capacidade de interagir com os hormônios estrogênicos e oxidá-los por meio de duas etapas de reação de um elétron. A lactoperoxidase reage com o anel A fenólico dos estrogênios para produzir radicais livres reativos . Além disso, a lactoperoxidase pode ativar aminas aromáticas e heterocíclicas carcinogênicas e aumentar os níveis de ligação dos produtos ativados ao DNA, o que sugere um papel potencial da ativação de carcinógenos catalisada pela lactoperoxidase na causa do câncer de mama.
Higiene bucal
Durante as últimas décadas, foram publicados vários estudos clínicos que descrevem a eficácia clínica do sistema lactoperoxidase em uma variedade de produtos de higiene bucal (pastas de dente, enxaguatórios bucais). Depois de mostrar indiretamente, por meio da mensuração de parâmetros experimentais de gengivite e cárie , que bochechos contendo amiloglucosidase (γ- amilase ) e glicose oxidase ativam o sistema lactoperoxidase, o mecanismo de proteção das enzimas em produtos para higiene bucal foi parcialmente elucidado. Enzimas como lisozima , lactoperoxidase e glicose oxidase são transferidas das pastas de dente para a película . Sendo componentes da película, essas enzimas são cataliticamente altamente ativas. Além disso, como parte das pastas de dente, o sistema lactoperoxidase tem uma influência benéfica para evitar a cárie na primeira infância, reduzindo o número de colônias formadas pela microflora cariogênica enquanto aumenta a concentração de tiocianato. Em pacientes com xerostomia , as pastas de dente com o sistema lactoperoxidase são aparentemente superiores às pastas de dente contendo flúor no que diz respeito à formação de placa e gengivite. Mais estudos são necessários para examinar mais detalhadamente os mecanismos de proteção.
A aplicação da lactoperoxidase não se restringe à cárie, gengivite e periodontite . Uma combinação de lisozima e lactoperoxidase pode ser aplicada para apoiar o tratamento da síndrome da boca ardente ( glossodinia ). Em combinação com lactoferrina, a lactoperoxidase combate a halitose ; em combinação com lactoferrina e lisozima, a lactoperoxidase ajuda a melhorar os sintomas de xerostomia. Além disso, os géis com lactoperoxidase ajudam a melhorar os sintomas do câncer oral quando a produção de saliva é comprometida devido à irradiação. Nesse caso, também a flora bacteriana oral é influenciada favoravelmente.
Veja também
Referências
Leitura adicional
- Galijasevic S, Saed GM, Diamond MP, Abu-Soud HM (setembro de 2004). "Alta constante de taxa de dissociação do complexo ferroso-dioxi ligado à atividade semelhante à catalase na lactoperoxidase" . The Journal of Biological Chemistry . 279 (38): 39465–70. doi : 10.1074 / jbc.M406003200 . PMID 15258136 . S2CID 30280587 .
- Ekstrand B (1994). "Lactoperoxidase and lactoferrin". Em Beuchat LR, Dillon VM, Board RG (eds.). Sistemas antimicrobianos naturais e preservação de alimentos . Oxon: CAB International. ISBN 978-0-85198-878-8.
- Kussendrager KD, van Hooijdonk AC (novembro de 2000). “Lactoperoxidase: propriedades físico-químicas, ocorrência, mecanismo de ação e aplicações” . The British Journal of Nutrition . 84 (Suplemento 1): S19-25. doi : 10.1017 / S0007114500002208 . PMID 11242442 .
- Thomas EL, Pera KA, Smith KW, Chwang AK (fevereiro de 1983). "Inibição de Streptococcus mutans pelo sistema antimicrobiano lactoperoxidase" . Infecção e imunidade . 39 (2): 767–78. doi : 10.1128 / IAI.39.2.767-778.1983 . PMC 348016 . PMID 6832819 .
- Korhonen H, Meriläinen V, Antila M, Kouvalainen K (1980). "[Fatores antimicrobianos no leite e resistência à infecção em bebês]". Duodecim; Laaketieteellinen Aikakauskirja (em finlandês). 96 (3): 184–99. PMID 7192622 .
- Oram JD, Reiter B (agosto de 1966). "A inibição dos estreptococos pela lactoperoxidase, tiocianato e peróxido de hidrogênio. O efeito do sistema inibitório em cepas suscetíveis e resistentes de estreptococos do grupo N" . The Biochemical Journal . 100 (2): 373–81. doi : 10.1042 / bj1000373 . PMC 1265145 . PMID 4290983 .
- Oram JD, Reiter B (agosto de 1966). "A inibição dos estreptococos pela lactoperoxidase, tiocianato e peróxido de hidrogênio. A oxidação do tiocianato e a natureza do composto inibitório" . The Biochemical Journal . 100 (2): 382–8. doi : 10.1042 / bj1000382 . PMC 1265146 . PMID 5338806 .
- Hannuksela S, Tenovuo J, Roger V, Lenander-Lumikari M, Ekstrand J (1994). "O flúor inibe os sistemas antimicrobianos da peroxidase na saliva total humana". Caries Research . 28 (6): 429–34. doi : 10.1159 / 000262016 . PMID 7850846 .
- Aune TM, Thomas EL (março de 1978). "Oxidação de proteínas sulfidrilas por produtos da oxidação catalisada por peroxidase do íon tiocianato". Bioquímica . 17 (6): 1005–10. doi : 10.1021 / bi00599a010 . PMID 204336 .
- Ekstrand B, Mullan WM, Waterhouse A (junho de 1985). "Inibição do Sistema Antibacteriano de Lactoperoxidase-Tiocianato-Peróxido de Hidrogênio por Leite Tratado por Calor". Journal of Food Protection . 48 (6): 494–498. doi : 10.4315 / 0362-028X-48.6.494 . PMID 30943594 .
- Reiter B, Härnulv G (setembro de 1984). "Sistema Antibacteriano da Lactoperoxidase: Ocorrência Natural, Funções Biológicas e Aplicações Práticas". Journal of Food Protection . 47 (9): 724–732. doi : 10.4315 / 0362-028X-47.9.724 . PMID 30934451 .
links externos
- Lactoperoxidase nos cabeçalhos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)