Radioatividade ambiental - Environmental radioactivity
| Parte de uma série sobre |
| Poluição |
|---|
 |
A radioatividade ambiental é produzida por materiais radioativos no ambiente humano . Enquanto alguns radioisótopos , como estrôncio-90 ( 90 Sr) e tecnécio-99 ( 99 Tc), só são encontrados na Terra como resultado da atividade humana, e alguns, como o potássio-40 ( 40 K), estão presentes apenas devido para processos naturais, alguns isótopos, por exemplo , trítio ( 3 H), resultam de processos naturais e atividades humanas. A concentração e localização de alguns isótopos naturais, particularmente urânio-238 ( 238 U), podem ser afetados pela atividade humana.
Nível de fundo em solos
A radioatividade está presente em todos os lugares , desde a formação da Terra. A radioatividade natural detectada no solo é predominantemente devida aos seguintes quatro radioisótopos naturais: 40 K, 226 Ra, 238 U e 232 Th. Em um quilograma de solo, o potássio-40 equivale a uma média de 370 Bq de radiação, com uma faixa típica de 100–700 Bq; os outros contribuem cada um com 25 Bq, com intervalos típicos de 10–50 Bq (7–50 Bq para 232 Th). Alguns solos podem variar muito em relação a essas normas.
Mar e lodo de rio
Um relatório recente sobre o rio Sava , na Sérvia, sugere que muitos dos lodos do rio contêm cerca de 100 Bq kg −1 de radioisótopos naturais ( 226 Ra, 232 Th e 238 U). De acordo com as Nações Unidas, a concentração normal de urânio no solo varia entre 300 μg kg −1 e 11,7 mg kg −1 . É bem sabido que algumas plantas, chamadas de hiperacumuladores , são capazes de absorver e concentrar metais em seus tecidos; O iodo foi isolado pela primeira vez de algas marinhas na França , o que sugere que as algas marinhas são um hiperacumulador de iodo.
Radioisótopos sintéticos também podem ser detectados em lodo. Busby cita um relatório sobre a atividade do plutônio em sedimentos intertidais galeses por Garland et al. (1989), o que sugere que quanto mais próximo um local está de Sellafield , maior é a concentração de plutônio no lodo. Alguma relação entre distância e atividade pode ser vista em seus dados, quando ajustados a uma curva exponencial, mas a dispersão dos pontos é grande (R 2 = 0,3683).
Feito pelo homem

A radioatividade adicional na biosfera causada pela atividade humana devido às liberações de radioatividade artificial e de Materiais Radioativos de Ocorrência Natural (NORM) pode ser dividida em várias classes.
- Liberações licenciadas normais que ocorrem durante a operação normal de uma planta ou processo de manuseio de materiais radioativos artificiais.
- Por exemplo, a liberação de 99 Tc de um departamento de medicina nuclear de um hospital que ocorre quando uma pessoa que recebeu um agente de imagem de Tc expele o agente.
- Liberações de materiais radioativos artificiais que ocorrem durante um acidente industrial ou de pesquisa.
- Por exemplo, o acidente de Chernobyl .
- Liberações que ocorrem como resultado de atividade militar.
- Por exemplo, um teste de armas nucleares.
- Liberações que ocorrem como resultado de um crime .
- Por exemplo, o acidente de Goiânia em que ladrões, desconhecendo seu conteúdo radioativo, roubaram alguns equipamentos médicos e, como resultado, várias pessoas foram expostas à radiação.
- Liberações de materiais radioativos de ocorrência natural (NORM) como resultado da mineração, etc.
- Por exemplo, a liberação de traços de urânio e tório no carvão, quando ele é queimado em usinas de energia.
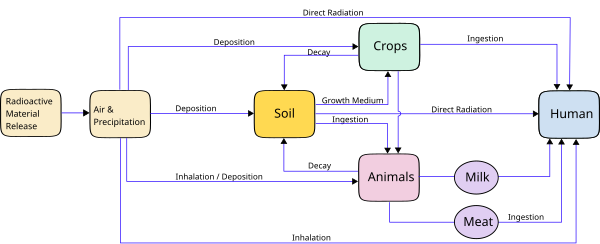
Agricultura e a transferência para humanos da radioatividade depositada
Só porque um radioisótopo pousa na superfície do solo, não significa que ele entrará na cadeia alimentar humana . Após serem liberados no meio ambiente, os materiais radioativos podem alcançar os humanos em uma variedade de rotas diferentes, e a química do elemento geralmente dita a rota mais provável.
Vacas
Jiří Hála afirma em seu livro "Radioactivity, Ionizing Radiation and Nuclear Energy" que o gado só passa uma minoria do estrôncio , césio , plutônio e amerício que ingerem aos humanos que consomem leite e carne . Usando o leite como exemplo, se a vaca ingerir diariamente 1000 Bq dos isótopos anteriores, o leite terá as seguintes atividades.
- 90 Sr, 2 Bq / L
- 137 Cs, 5 Bq / L
- 239 Pu, 0,001 Bq / L
- 241 Am, 0,001 Bq / L
Solo
O livro de Jiří Hála afirma que os solos variam muito em sua capacidade de ligar radioisótopos, as partículas de argila e os ácidos húmicos podem alterar a distribuição dos isótopos entre a água do solo e o solo. O coeficiente de distribuição K d é a razão entre a radioatividade do solo (Bq g −1 ) e a da água no solo (Bq ml −1 ). Se a radioatividade estiver fortemente ligada aos minerais do solo, então menos radioatividade pode ser absorvida pelas plantações e grama que cresce no solo.
O teste da Trindade
Uma fonte dramática de radioatividade produzida pelo homem é um teste de armas nucleares . O trinitito vítreo criado pela primeira bomba atômica contém radioisótopos formados pela ativação de nêutrons e fissão nuclear . Além disso, alguns radioisótopos naturais estão presentes. Um artigo recente relata os níveis de radioisótopos de longa vida no trinitito. O trinitito foi formado a partir de feldspato e quartzo, que foram derretidos pelo calor. Duas amostras de trinitito foram usadas, a primeira (barras do lado esquerdo no gráfico) foi retirada entre 40 e 65 metros do ponto zero, enquanto a outra amostra foi retirada mais longe do ponto zero .
Os 152 Eu (meia-vida de 13,54 anos) e os 154 Eu (meia-vida de 8,59 anos) foram formados principalmente pela ativação de nêutrons do európio no solo, é claro que o nível de radioatividade para esses isótopos é mais alto onde a dose de nêutrons para o solo era maior. Parte dos 60 Co (meia-vida de 5,27 anos) é gerada pela ativação do cobalto no solo, mas parte também foi gerada pela ativação do cobalto na torre de aço (100 pés). Esses 60 Co da torre teriam sido espalhados pelo local reduzindo a diferença nos níveis de solo.
O 133 Ba (meia-vida de 10,5 anos) e 241 Am (meia-vida de 432,6 anos) são devidos à ativação de nêutrons de bário e plutônio dentro da bomba. O bário estava presente na forma de nitrato nos explosivos químicos usados, enquanto o plutônio era o combustível físsil usado.
O nível de 137 Cs é mais alto na amostra que estava mais longe do ponto zero - acredita-se que os precursores do 137 Cs ( 137 I e 137 Xe) e, em menor grau, o próprio césio são voláteis . Os radioisótopos naturais no vidro são quase os mesmos em ambos os locais.

Produtos de ativação
A ação dos nêutrons em isótopos estáveis pode formar radioisótopos , por exemplo, o bombardeio de nêutrons (ativação de nêutrons) de nitrogênio -14 forma carbono -14. Este radioisótopo pode ser liberado do ciclo do combustível nuclear ; este é o radioisótopo responsável pela maior parte da dose experimentada pela população em decorrência das atividades da indústria de energia nuclear .
Os testes de bombas nucleares aumentaram a atividade específica do carbono, enquanto o uso de combustíveis fósseis a diminuiu. Veja o artigo sobre datação por radiocarbono para mais detalhes.
Produtos de fissão
Descargas de usinas nucleares dentro do ciclo do combustível nuclear introduzem produtos da fissão no meio ambiente. As emissões de usinas de reprocessamento nuclear tendem a ser radioisótopos de vida média a longa; isso ocorre porque o combustível nuclear pode esfriar por vários anos antes de ser dissolvido no ácido nítrico . Os lançamentos de acidentes de reatores nucleares e detonações de bombas conterão uma quantidade maior de radioisótopos de vida curta (quando os valores são expressos em atividade Bq )).
De curta duração
Um exemplo de produto de fissão de curta duração é o iodo-131 , que também pode ser formado como um produto de ativação pela ativação de nêutrons do telúrio .
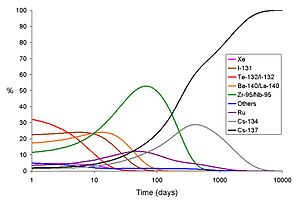
Tanto na queda da bomba quanto na liberação de um acidente com o reator de energia, os isótopos de curta duração fazem com que a taxa de dose no primeiro dia seja muito mais alta do que aquela que será experimentada no mesmo local muitos dias depois. Isso é verdadeiro mesmo que nenhuma tentativa de descontaminação seja feita. Nos gráficos abaixo, são mostradas a taxa de dose gama total e a parcela da dose devida a cada isótopo principal liberado pelo acidente de Chernobyl.
Médium viveu
Um exemplo de meio vivido é o 137 Cs, que tem meia-vida de 30 anos. O césio é liberado na precipitação de bombas e no ciclo do combustível nuclear . Um artigo foi escrito sobre a radioatividade em ostras encontradas no mar da Irlanda , estas foram encontradas por espectroscopia gama para conter 141 Ce, 144 Ce, 103 Ru, 106 Ru, 137 Cs, 95 Zr e 95 Nb. Além disso, um produto de ativação de zinco ( 65 Zn) foi encontrado, acredita-se que seja devido à corrosão do revestimento de combustível magnox em tanques de resfriamento. A concentração de todos esses isótopos no mar da Irlanda atribuível a instalações nucleares como Sellafield diminuiu significativamente nas últimas décadas.
Uma parte importante da liberação de Chernobyl foi o césio-137, este isótopo é responsável por grande parte da exposição externa de longo prazo (pelo menos um ano após o incêndio) que ocorreu no local. Os isótopos de césio na precipitação radioativa tiveram um efeito na agricultura. [2]
Grande quantidade de césio foi liberada durante o acidente em Goiânia, onde uma fonte radioativa (de uso médico) foi roubada e quebrada durante uma tentativa de convertê-la em sucata. O acidente poderia ter sido interrompido em vários estágios; primeiro, os últimos proprietários legais da fonte não tomaram providências para que a fonte fosse armazenada em um local seguro e protegido; e, em segundo lugar, os sucateiros que o pegaram não reconheceram as marcações que indicavam que se tratava de um objeto radioativo.
Soudek et al. relataram em 2006 detalhes da absorção de 90 Sr e 137 Cs em girassóis cultivados em condições hidropônicas . O césio foi encontrado nas nervuras das folhas, no caule e nas folhas apicais . Verificou-se que 12% do césio entrou na planta e 20% do estrôncio. Este artigo também relata detalhes do efeito dos íons potássio , amônio e cálcio na captação dos radioisótopos.
O césio liga-se fortemente a minerais de argila , como ilita e montmorilonita ; portanto, ele permanece nas camadas superiores do solo, onde pode ser acessado por plantas com raízes superficiais (como a grama). Conseqüentemente, a grama e os cogumelos podem carregar uma quantidade considerável de 137 Cs, que pode ser transferido para os humanos através da cadeia alimentar . Uma das melhores contra-medidas na pecuária leiteira contra o 137 Cs é misturar o solo arando profundamente o solo. Isso tem o efeito de colocar o 137 Cs fora do alcance das raízes rasas da grama, portanto, o nível de radioatividade na grama será reduzido. Além disso, após uma guerra nuclear ou acidente grave, a remoção de alguns centímetros superiores do solo e seu enterro em uma trincheira rasa reduzirá a dose gama de longo prazo para humanos devido a 137 Cs, pois os fótons gama serão atenuados por sua passagem pelo solo . Quanto mais distante a trincheira estiver dos humanos e quanto mais profunda for a trincheira, melhor será o grau de proteção que será oferecido à população humana.
Na pecuária , uma importante contramedida contra o 137 Cs é dar aos animais um pouco de azul da Prússia . Este composto de cianeto de ferro e potássio atua como um trocador de íons . O cianeto está tão fortemente ligado ao ferro que é seguro para um ser humano comer vários gramas de azul da Prússia por dia. O azul da Prússia reduz a meia-vida biológica (não deve ser confundida com a meia-vida nuclear ) do césio). A meia-vida física ou nuclear de 137 Cs é de cerca de 30 anos, que é uma constante e não pode ser alterada; no entanto, a meia-vida biológica mudará de acordo com a natureza e os hábitos do organismo para o qual é expressa. O césio em humanos normalmente tem meia-vida biológica de um a quatro meses. Uma vantagem adicional do azul da Prússia é que o césio que é retirado do animal nas fezes está em uma forma que não está disponível para as plantas. Conseqüentemente, evita que o césio seja reciclado. A forma de azul da Prússia necessária para o tratamento de humanos ou animais é um grau especial. As tentativas de usar o grau de pigmento usado em tintas não tiveram sucesso.
Longa vida
Exemplos de isótopos de vida longa incluem iodo -129 e Tc-99, que têm meia-vida nuclear de 15 milhões e 200.000 anos, respectivamente.
Plutônio e os outros actinídeos
Na cultura popular, o plutônio é considerado a maior ameaça à vida e aos membros, o que é errado; embora a ingestão de plutônio provavelmente não seja boa para a saúde, outros radioisótopos, como o rádio, são mais tóxicos para os humanos. Independentemente disso, a introdução de elementos de transurânio , como o plutônio, no meio ambiente deve ser evitada sempre que possível. Atualmente, as atividades da indústria de reprocessamento nuclear têm sido objeto de grande debate, pois um dos temores daqueles que se opõem à indústria é que grandes quantidades de plutônio sejam mal administradas ou liberadas no meio ambiente.
No passado, uma das maiores liberações de plutônio no meio ambiente foram os testes de bombas nucleares .
- Esses testes no ar espalharam algum plutônio por todo o globo; esta grande diluição do plutônio resultou na ameaça a cada pessoa exposta sendo muito pequena, pois cada pessoa é exposta apenas a uma quantidade muito pequena.
- Os testes subterrâneos tendem a formar rocha derretida, que resfria rapidamente e sela os actinídeos na rocha, tornando-os incapazes de se mover; mais uma vez, a ameaça aos humanos é pequena, a menos que o local do teste seja desenterrado.
- Os testes de segurança em que as bombas foram sujeitas a acidentes simulados representam a maior ameaça para as pessoas; algumas áreas de terra usadas para tais experimentos (conduzidas ao ar livre) não foram totalmente liberadas para uso geral, apesar de em um caso uma extensa descontaminação.
Natural
Produtos de ativação de raios cósmicos
Isótopos cosmogênicos (ou nuclídeos cosmogênicos ) são isótopos raros criados quando um raio cósmico de alta energia interage com o núcleo de um átomo in situ . Estes isótopos são produzidos dentro de materiais de terras, como rochas ou do solo , na Terra atmosfera , e em itens extraterrestres, como meteoritos . Ao medir os isótopos cosmogênicos, os cientistas são capazes de obter informações sobre uma variedade de processos geológicos e astronômicos . Existem isótopos cosmogênicos radioativos e estáveis . Alguns desses radioisótopos são trítio , carbono -14 e fósforo -32.
Modos de produção
Aqui está uma lista de radioisótopos formados pela ação dos raios cósmicos na atmosfera; a lista também contém o modo de produção do isótopo. Esses dados foram obtidos do relatório SCOPE50, consulte a tabela 1.9 do capítulo 1 .
| Isótopo | Modo de formação |
|---|---|
| ³H (trítio) | 14 N (n, 12 C) ³H |
| 7 Be | Espalação (N e O) |
| 10 Be | Espalação (N e O) |
| 11 C | Espalação (N e O) |
| 14 C | 14 N (n, p) 14 C |
| 18 F | 18 O (p, n) 18 F e Espalação (Ar) |
| 22 Na | Espalação (Ar) |
| 24 Na | Espalação (Ar) |
| 28 mg | Espalação (Ar) |
| 31 Si | Espalação (Ar) |
| 32 Si | Espalação (Ar) |
| 32 P | Espalação (Ar) |
| 34m Cl | Espalação (Ar) |
| 35 S | Espalação (Ar) |
| 36 Cl | 35 Cl (n,) 36 Cl |
| 37 Ar | 37 Cl (p, n) 37 Ar |
| 38 Cl | Espalação (Ar) |
| 39 Ar | 38 Ar (n,) 39 Ar |
| 39 Cl | 40 Ar (n, np) 39 Cl e espalhamento (Ar) |
| 41 Ar | 40 Ar (n,) 41 Ar |
| 81 Kr | 80 Kr (n,) 81 Kr |
Transferência para o solo
O nível de berílio -7 no ar está relacionado ao ciclo das manchas solares , pois a radiação do sol forma este radioisótopo na atmosfera. A taxa de transferência do ar para o solo é controlada em parte pelo clima.
Aplicações em geologia listadas por isótopo
| elemento | massa | meia-vida (anos) | aplicação típica |
|---|---|---|---|
| hélio | 3 | - estábulo - | exposição de datação de rochas portadoras de olivina |
| berílio | 10 | 1,36 milhão | datação de exposição de rochas portadoras de quartzo , sedimento, datação de testemunhos de gelo, medição de taxas de erosão |
| carbono | 14 | 5.730 | datação de matéria orgânica, água |
| néon | 21 | - estábulo - | datação de superfícies muito estáveis e expostas por muito tempo, incluindo meteoritos |
| alumínio | 26 | 720.000 | exposição, datação de rochas, sedimentos |
| cloro | 36 | 308.000 | datação de exposição de rochas, traçador de água subterrânea |
| cálcio | 41 | 103.000 | exposição de datação de rochas carbonáticas |
| iodo | 129 | 15,7 milhões | traçador de água subterrânea |
Aplicações de namoro
Como os isótopos cosmogênicos têm meia-vida longa (de milhares a milhões de anos), os cientistas os consideram úteis para datação geológica . Isótopos cosmogênicos são produzidos na superfície da Terra ou próximos a ela e, portanto, são comumente aplicados a problemas de medição de idades e taxas de eventos e processos geomórficos e sedimentares .
As aplicações específicas de isótopos cosmogênicos incluem:
- datação de exposição de superfícies de terra, incluindo rocha polida glacialmente , escarpas de falhas , detritos de deslizamento de terra
- datação de sepultamento de sedimentos, rochas, gelo
- medição das taxas de erosão em estado estacionário
- datação absoluta de matéria orgânica ( datação por radiocarbono )
- datação absoluta de massas de água, medição das taxas de transporte de água subterrânea
- datação absoluta de meteoritos, superfícies lunares
Métodos de medição para os isótopos de longa duração
Para medir isótopos cosmogênicos produzidos em materiais sólidos da terra, como rocha, as amostras geralmente são submetidas a um processo de separação mecânica. A amostra é triturada e o material desejável, como um mineral particular ( quartzo no caso de Be-10), é separado do material não desejável usando uma separação por densidade em um meio líquido pesado, como tungstato de sódio e lítio (LST). A amostra é então dissolvida, um transportador de isótopo comum adicionado (transportador Be-9 no caso de Be-10), e a solução aquosa é purificada até um óxido ou outro sólido puro.
Finalmente, a proporção do isótopo cosmogênico raro para o isótopo comum é medida usando espectrometria de massa do acelerador . A concentração original do isótopo cosmogênico na amostra é então calculada usando a razão isotópica medida, a massa da amostra e a massa do transportador adicionada à amostra.
Rádio e rádon da decadência de actinídeos de longa duração
O rádio e o radônio estão no meio ambiente porque são produtos da decomposição do urânio e do tório .
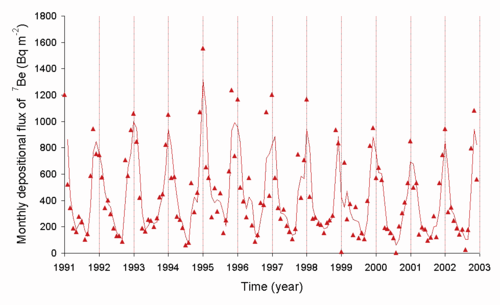
O radônio ( 222 Rn) liberado no ar decai para 210 Pb e outros radioisótopos, e os níveis de 210 Pb podem ser medidos. A taxa de deposição deste radioisótopo depende do clima. Abaixo está um gráfico da taxa de deposição observada no Japão .
Datação de urânio-chumbo
A datação de urânio - chumbo é geralmente realizada no mineral zircão (ZrSiO 4 ), embora outros materiais possam ser usados. O zircônio incorpora átomos de urânio em sua estrutura cristalina como substitutos do zircônio , mas rejeita fortemente o chumbo. Possui alta temperatura de bloqueio, é resistente às intempéries mecânicas e é quimicamente inerte. O zircão também forma múltiplas camadas de cristal durante eventos metamórficos, cada uma podendo registrar uma idade isotópica do evento. Eles podem ser datados por uma microssonda de íons SHRIMP .
Uma das vantagens deste método é que qualquer amostra fornece dois relógios, um baseado no decaimento do urânio-235 para chumbo-207 com meia-vida de cerca de 703 milhões de anos e outro baseado na decadência do urânio-238 para chumbo-206 com uma meia-vida de cerca de 4,5 bilhões de anos, fornecendo uma verificação cruzada embutida que permite a determinação precisa da idade da amostra, mesmo que parte do chumbo tenha sido perdida.
Veja também
- Journal of Environmental Radioactivity
- Material radioativo de ocorrência natural
- Radioecologia
- Rádio no meio ambiente
- Urânio no meio ambiente
Referências
Referências sobre datação isotópica cosmogênica
- Gosse, John C. e Phillips, Fred M. (2001). "Nuclídeos cosmogênicos terrestres in situ: Teoria e aplicação". Quaternary Science Reviews 20 , 1475–1560.
- Granger, Darryl E., Fabel, Derek e Palmer, Arthur N. (2001). "Incisão Plioceno-Pleistoceno do Green River, Kentucky, determinada a partir da decomposição radioativa de 26Al e 10Be cosmogênicos em sedimentos da Caverna Mammoth". Geological Society of America Bulletin 113 (7), 825–836.
Leitura adicional
- Radioatividade, Radiação Ionizante e Energia Nuclear, por J. Hala e JD Navratil
- Uma revisão do assunto foi publicada pelo Comitê Científico sobre Problemas do Meio Ambiente (SCOPE) no relatório SCOPE 50 Radioecology after chernobyl .