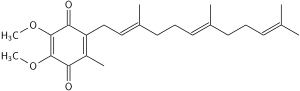
Coenzima Q 10 -Coenzyme Q10
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
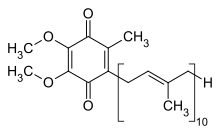
2 - [(2 E , 6 E , 10 E , 14 E , 18 E , 22 E , 26 E , 30 E , 34 E ) -3,7,11,15,19,23,27,31,35, 39-Decametiltetraconta-2,6,10,14,18,22,26,30,34,38-decaen-1-il] -5,6-dimetoxi-3-metilciclohexa-2,5-dieno-1,4 -dione |
|
| Outros nomes
A ubiquinona, ubidecarenona, coenzima Q, CoQ 10 , / ˌ k oʊ ˌ k ju t ɛ n / , CoQ, Q 10 , Q vitamina
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100,005,590 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 59 H 90 O 4 | |
| Massa molar | 863,365 g · mol −1 |
| Aparência | sólido amarelo ou laranja |
| Ponto de fusão | 48–52 ° C (118–126 ° F; 321–325 K) |
| insolúvel | |
| Farmacologia | |
| C01EB09 ( OMS ) | |
| Compostos relacionados | |
|
Quinonas relacionadas
|
1,4-Benzoquinona Plastoquinona Ubiquinol |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
A coenzima Q , também conhecida como ubiquinona , é uma família de coenzimas onipresentes em animais e na maioria das bactérias (daí o nome ubiquinona). Em humanos, a forma mais comum é a coenzima Q 10 ou ubiquinona-10 . A CoQ 10 não é aprovada pela Food and Drug Administration (FDA) dos EUA para o tratamento de qualquer condição médica; no entanto, é vendido como um suplemento dietético e é um ingrediente de alguns cosméticos.
É uma 1,4-benzoquinona , onde Q se refere ao grupo químico quinona e 10 se refere ao número de subunidades químicas de isoprenil em sua cauda. Nas ubiquinonas naturais, o número pode variar de 6 a 10. Essa família de substâncias solúveis em gordura, que se assemelham a vitaminas , está presente em todas as células eucarióticas respiratórias , principalmente nas mitocôndrias . É um componente da cadeia de transporte de elétrons e participa da respiração celular aeróbia , que gera energia na forma de ATP . Noventa e cinco por cento da energia do corpo humano é gerada dessa maneira. Órgãos com os mais altos requisitos de energia - como coração , fígado e rim - têm as maiores concentrações de CoQ 10 .
Existem três redox estados de CoQ: totalmente oxidado ( UBI quinona), semi quinona ( ubisemi quinona), e totalmente reduzida ( ubiquinol ). A capacidade desta molécula de atuar como um transportador de dois elétrons (movendo-se entre a forma quinona e quinol) e um transportador de um elétron (movendo-se entre a semiquinona e uma dessas outras formas) é central para seu papel na cadeia de transporte de elétrons devido aos aglomerados de ferro-enxofre que só podem aceitar um elétron de cada vez e como um antioxidante eliminador de radicais livres .
Deficiência e toxicidade
Existem dois fatores principais que levam à deficiência de CoQ 10 em humanos: redução da biossíntese e aumento do uso pelo corpo. A biossíntese é a principal fonte de CoQ 10 . A biossíntese requer pelo menos 12 genes , e mutações em muitos deles causam deficiência de CoQ. Os níveis de CoQ 10 também podem ser afetados por outros defeitos genéticos (como mutações do DNA mitocondrial , ETFDH , APTX , FXN e BRAF , genes que não estão diretamente relacionados ao processo biossintético da CoQ 10 ). Alguns deles, como mutações em COQ6 , podem levar a doenças graves, como a síndrome nefrótica resistente a esteroides com surdez neurossensorial .
Alguns efeitos adversos, principalmente gastrointestinais, são relatados com ingestões muito altas. O método de avaliação de risco de nível seguro observado (OSL) indicou que a evidência de segurança é forte em ingestões de até 1200 mg / dia, e esse nível é identificado como OSL.
Avaliação
Embora a CoQ 10 possa ser medida no plasma sanguíneo , essas medidas refletem a ingestão alimentar em vez do estado do tecido. Atualmente, a maioria dos centros clínicos mede os níveis de CoQ 10 em fibroblastos de pele em cultura , biópsias musculares e células mononucleares do sangue. Fibroblastos de cultura pode ser utilizado também para avaliar a taxa de endógena CoQ 10 biossíntese, por medição da captação de 14 C - rotulados p -hidroxibenzoato .
Estatinas
Foi sugerido que a miotoxicidade das estatinas se deve ao comprometimento da biossíntese de CoQ, mas as evidências que sustentam isso foram consideradas controversas em 2011.
Embora as estatinas possam reduzir a coenzima Q 10 no sangue, não está claro se elas reduzem a coenzima Q 10 no músculo. A evidência não apóia que a suplementação melhore os efeitos colaterais das estatinas. No entanto, uma metanálise mais recente concluiu que "a suplementação com CoQ10 melhorou os SAMSs, sugerindo que a suplementação com CoQ10 pode ser uma abordagem complementar para melhorar a miopatia induzida por estatina."
Suplemento dietético
Regulamento e composição
CoQ 10 é vendido em muitas jurisdições como um suplemento dietético em nome de UbiQ 300 e UbiQ 100, não sujeito aos mesmos regulamentos dos medicamentos , mas não aprovado para o tratamento de qualquer condição médica . A fabricação de CoQ 10 não é regulamentada e diferentes lotes e marcas podem variar significativamente: uma análise de laboratório de 2004 feita pelo ConsumerLab.com dos suplementos de CoQ 10 à venda nos Estados Unidos constatou que alguns não continham a quantidade identificada no rótulo do produto. As quantidades variaram de "CoQ 10 não detectável ", por meio de 75% da dose declarada, até um excesso de 75%.
Geralmente, CoQ 10 é bem tolerado. Os efeitos colaterais mais comuns são sintomas gastrointestinais ( náuseas , vômitos , supressão do apetite e dor abdominal ), erupções cutâneas e dores de cabeça .
Embora não haja uma dosagem ideal estabelecida de CoQ 10 , uma dose diária típica é de 100–200 miligramas. Diferentes formulações têm diferentes quantidades declaradas de CoQ 10 e outros ingredientes.
Doença cardíaca
Uma revisão da Cochrane de 2014 não encontrou "nenhuma evidência convincente para apoiar ou refutar" o uso da CoQ 10 para o tratamento da insuficiência cardíaca . Outra revisão da Cochrane de 2014 encontrou evidências insuficientes para fazer uma conclusão sobre seu uso para a prevenção de doenças cardíacas. Uma revisão da Cochrane de 2016 concluiu que a CoQ 10 não teve efeito sobre a pressão arterial . Em uma meta-análise de 2017 de pessoas com insuficiência cardíaca, 30–100 mg / d de CoQ 10 resultou em mortalidade 31% menor. A capacidade de exercício também foi aumentada. Nenhuma diferença significativa foi encontrada nos desfechos da fração de ejeção do coração esquerdo e na classificação da New York Heart Association (NYHA).
Enxaqueca
A diretriz da Canadian Headache Society para profilaxia da enxaqueca recomenda, com base em evidências de baixa qualidade, que 300 mg de CoQ 10 sejam oferecidos como opção para profilaxia.
Miopatia por estatina
A CoQ 10 tem sido usada rotineiramente para tratar a degradação muscular associada como um efeito colateral do uso de medicamentos com estatina . Uma meta-análise de 2015 de ensaios clínicos randomizados descobriu que a CoQ 10 não teve efeito sobre a miopatia por estatina . Uma meta-análise de 2018 concluiu que havia evidências preliminares para a CoQ 10 oral reduzir os sintomas musculares associados às estatinas, incluindo dor muscular, fraqueza muscular, cãibras musculares e cansaço muscular.
Câncer
Em 2014, nenhum grande ensaio clínico de CoQ 10 no tratamento do câncer havia sido realizado. O Instituto Nacional do Câncer dos EUA identificou problemas com os poucos e pequenos estudos que foram realizados, afirmando que "a maneira como os estudos foram feitos e a quantidade de informações relatadas não deixou claro se os benefícios foram causados pela CoQ 10 ou por outra coisa " A American Cancer Society concluiu: "CoQ 10 pode reduzir a eficácia da quimioterapia e da radioterapia, por isso a maioria dos oncologistas recomendaria evitá-la durante o tratamento do câncer."
Doença dentária
Um estudo de revisão de 1995 descobriu que não há benefício clínico para o uso de CoQ 10 no tratamento da doença periodontal . A maioria dos estudos sugerindo o contrário estavam desatualizados, focados em testes in vitro , tinham muito poucos assuntos de teste e / ou metodologia estatística e configuração de teste errôneas, ou foram patrocinados por um fabricante do produto.
Doença renal crônica
Uma revisão dos efeitos da suplementação de CoQ 10 em pessoas com DRC foi proposta em 2019.
Usos adicionais
A coenzima Q10 também tem sido usada para tratar a doença de Alzheimer, colesterol alto ou esclerose lateral amiotrófica (doença de Lou Gehrig). No entanto, a pesquisa mostrou que isso pode não ser eficaz no tratamento dessas condições
A coenzima Q10 também tem sido utilizada como ingrediente ativo em cosmecêuticos e como ingrediente inativo em formulações de filtro solar . Quando aplicado topicamente em produtos para a pele, demonstra alguma capacidade de reduzir o estresse oxidativo na pele, retardar os sinais de envelhecimento intrínseco da pele, reverter os sinais de envelhecimento extrínseco da pele, auxiliar no desbotamento da despigmentação , aumentar a estabilidade de certos ativos de filtro solar, aumentar o FPS dos filtros solares, e oferecem alguma proteção infravermelha para protetores solares. Muitas das pesquisas sobre os benefícios da ubiquinona para a pele mostram que ela funciona sinergicamente com outros antioxidantes tópicos para melhorar a pele e as formulações cosméticas.
Interações
A coenzima Q 10 tem potencial para inibir os efeitos da teofilina , bem como do anticoagulante varfarina ; a coenzima Q 10 pode interferir nas ações da varfarina ao interagir com as enzimas do citocromo p450 , reduzindo assim o INR , uma medida da coagulação do sangue. A estrutura da coenzima Q 10 é muito semelhante à da vitamina K , que compete com os efeitos anticoagulantes da varfarina e os neutraliza. A coenzima Q 10 deve ser evitada em pacientes atualmente em uso de varfarina devido ao risco aumentado de coagulação.
Propriedades quimicas
A estrutura oxidada de CoQ 10 é mostrada acima. Os vários tipos de Coenzima Q podem ser distinguidos pelo número de subunidades isoprenóides em suas cadeias laterais . A coenzima Q mais comum na mitocôndria humana é a CoQ 10 . Q refere-se à cabeça da quinona e 10 refere-se ao número de repetições de isopreno na cauda. A molécula abaixo possui três unidades isoprenóides e seria chamada de Q 3 .
Em seu estado puro, é um pó lipófilo de cor laranja, sem sabor nem odor.
Biossíntese
A biossíntese ocorre na maioria dos tecidos humanos. Existem três etapas principais:
- Criação da estrutura da benzoquinona (usando fenilalanina ou tirosina , via 4-hidroxibenzoato )
- Criação da cadeia lateral de isopreno (usando acetil-CoA )
- A junção ou condensação das duas estruturas acima
As duas reações iniciais ocorrem na mitocôndria , no retículo endoplasmático e nos peroxissomos , indicando múltiplos locais de síntese em células animais.
Uma enzima importante nessa via é a HMG-CoA redutase , geralmente um alvo para intervenção em complicações cardiovasculares. A família "estatina" de medicamentos para redução do colesterol inibe a HMG-CoA redutase. Um possível efeito colateral das estatinas é a diminuição da produção de CoQ 10 , que pode estar ligada ao desenvolvimento de miopatia e rabdomiólise . No entanto, o papel da estatina na deficiência de CoQ é controverso. Embora essas drogas reduzam os níveis sanguíneos de CoQ, os estudos sobre os efeitos dos níveis musculares de CoQ ainda estão por vir. A suplementação de CoQ também não reduz os efeitos colaterais dos medicamentos com estatina.
Os genes envolvidos incluem PDSS1 , PDSS2 , COQ2 e ADCK3 ( COQ8 , CABC1 ).
Outros organismos além dos humanos usam substâncias químicas de origem um pouco diferentes para produzir a estrutura da benzoquinona e a estrutura do isopreno. Por exemplo, a bactéria E. coli produz o primeiro a partir de corismato e o último a partir de uma fonte não mevalonato. A levedura comum S. cerevisiae , entretanto, deriva a primeira do corismato ou tirosina e a última do mevalonato . A maioria dos organismos compartilha o intermediário 4-hidroxibenzoato comum, mais uma vez usa diferentes etapas para chegar à estrutura "Q".
Absorção e metabolismo
Absorção
CoQ 10 é um pó cristalino insolúvel em água. A absorção segue o mesmo processo dos lipídios; o mecanismo de captação parece ser semelhante ao da vitamina E , outro nutriente lipossolúvel. Este processo no corpo humano envolve a secreção no intestino delgado de enzimas pancreáticas e da bile , o que facilita a emulsificação e a formação de micelas necessárias para a absorção de substâncias lipofílicas . A ingestão de alimentos (e a presença de lipídios) estimula a excreção biliar corporal de ácidos biliares e aumenta muito a absorção de CoQ 10 . A CoQ 10 exógena é absorvida pelo intestino delgado e é melhor absorvida se for tomada com uma refeição. A concentração sérica de CoQ 10 em condições de alimentação é maior do que em condições de jejum.
Metabolismo
Os dados sobre o metabolismo da CoQ 10 em animais e humanos são limitados. Um estudo com CoQ 10 marcada com 14 C em ratos mostrou a maior parte da radioatividade no fígado duas horas após a administração oral, quando o pico de radioatividade plasmática foi observado, mas CoQ 9 (com apenas 9 unidades de isoprenil) é a forma predominante de coenzima Q em ratos. Parece que a CoQ 10 é metabolizada em todos os tecidos, enquanto a principal via de eliminação é a excreção biliar e fecal . Após a suspensão da suplementação com CoQ 10 , os níveis voltam ao normal em alguns dias, independentemente do tipo de formulação utilizada.
Farmacocinética
Alguns relatórios foram publicados sobre a farmacocinética da CoQ 10 . O pico plasmático pode ser observado 2–6 horas após a administração oral, dependendo principalmente do desenho do estudo. Em alguns estudos, um segundo pico plasmático também foi observado aproximadamente 24 horas após a administração, provavelmente devido à reciclagem entero-hepática e redistribuição do fígado para a circulação. Tomono et al . usaram CoQ10 cristalina marcada com deutério para investigar a farmacocinética em humanos e determinaram uma meia-vida de eliminação de 33 horas.
Melhorando a biodisponibilidade de CoQ 10
A importância de como os medicamentos são formulados para a biodisponibilidade é bem conhecida. A fim de encontrar um princípio para aumentar a biodisponibilidade de CoQ 10 após a administração oral, várias abordagens novas foram adotadas; diferentes formulações e formas foram desenvolvidas e testadas em animais e humanos.
Redução do tamanho da partícula
As nanopartículas têm sido exploradas como um sistema de entrega para vários medicamentos, como melhorar a biodisponibilidade oral de medicamentos com características de baixa absorção. No entanto, isso não teve sucesso com CoQ 10 , embora os relatórios tenham divergido amplamente. O uso de suspensão aquosa de CoQ 10 em pó fino em água pura também revela apenas um efeito menor.
Cápsulas de gel macio com CoQ 10 em suspensão de óleo
Uma abordagem bem-sucedida é usar o sistema de emulsão para facilitar a absorção do trato gastrointestinal e melhorar a biodisponibilidade. Emulsões de óleo de soja (microesferas lipídicas) podiam ser estabilizadas de maneira muito eficaz pela lecitina e eram usadas na preparação de cápsulas de gel mole. Em uma das primeiras tentativas, Ozawa et al. realizaram um estudo farmacocinético em beagles no qual a emulsão de CoQ 10 em óleo de soja foi investigada; cerca de duas vezes o nível de CoQ 10 no plasma do que o da preparação de comprimido de controle foi determinado durante a administração de uma microesfera lipídica. Embora uma melhoria quase insignificante da biodisponibilidade tenha sido observada por Kommuru et al. com ucápsulas de cápsulas de gel à base de óleo em um estudo posterior em cães, a biodisponibilidade significativamente aumentada de CoQ 10 foi confirmada para várias formulações à base de óleo na maioria dos outros estudos.
Novas formas de CoQ 10 com maior solubilidade em água
Facilitar a absorção de drogas aumentando sua solubilidade em água é uma estratégia farmacêutica comum e também tem se mostrado eficaz para CoQ 10 . Várias abordagens foram desenvolvidas para atingir esse objetivo, com muitas delas produzindo resultados significativamente melhores em relação às cápsulas de gel macio à base de óleo, apesar das muitas tentativas de otimizar sua composição. Exemplos de tais abordagens são o uso da dispersão aquosa de CoQ 10 sólido com o polímero tiloxapol , formulações baseadas em vários agentes solubilizantes, tais como lecitina hidrogenada , e complexação com ciclodextrinas ; Entre estes últimos, o complexo com β-ciclodextrina foi encontrada para ter altamente biodisponibilidade aumentada e também é usado nas indústrias farmacêutica e de alimentos para CoQ 10 -fortification.
História
Em 1950, GN Festenstein foi o primeiro a isolar uma pequena quantidade de CoQ 10 do revestimento do intestino de um cavalo em Liverpool , Inglaterra. Em estudos subsequentes, o composto foi chamado brevemente de substância SA , foi considerado quinona e foi observado que podia ser encontrado em muitos tecidos de vários animais.
Em 1957, Frederick L. Crane e colegas da Universidade de Wisconsin-Madison Enzyme Institute isolaram o mesmo composto de membranas mitocondriais de coração de boi e observaram que ele transportava elétrons dentro das mitocôndrias. Eles o chamaram de Q-275 , pois era uma quinona . Logo eles notaram que o Q-275 e a substância SA estudada na Inglaterra podem ser o mesmo composto. Isso foi confirmado mais tarde naquele ano e o Q-275 / substância SA foi renomeado como ubiquinona , pois era uma quinona onipresente que podia ser encontrada em todos os tecidos animais.
Em 1958, sua estrutura química completa foi relatada por DE Wolf e colegas que trabalhavam com Karl Folkers na Merck em Rahway . Mais tarde naquele ano, DE Green e colegas pertencentes ao grupo de pesquisa de Wisconsin sugeriram que a ubiquinona deveria ser chamada de mitoquinona ou coenzima Q devido à sua participação na cadeia de transporte de elétrons mitocondrial .
Em 1966, A. Mellors e AL Tappel , da Universidade da Califórnia, foram os primeiros a mostrar que a CoQ 6 reduzida era um antioxidante eficaz nas células.
Na década de 1960, Peter D. Mitchell ampliou a compreensão da função mitocondrial por meio de sua teoria do gradiente eletroquímico , que envolve CoQ 10 , e no final dos anos 1970 os estudos de Lars Ernster ampliaram a importância da CoQ 10 como antioxidante. A década de 1980 testemunhou um aumento acentuado no número de ensaios clínicos envolvendo CoQ 10 .
Concentrações dietéticas
Revisões detalhadas sobre a ocorrência de CoQ 10 e ingestão alimentar foram publicadas em 2010. Além da síntese endógena dentro dos organismos, a CoQ 10 também é fornecida ao organismo por vários alimentos. Apesar do grande interesse da comunidade científica neste composto, no entanto, um número muito limitado de estudos foi realizado para determinar o conteúdo de CoQ 10 em componentes dietéticos. Os primeiros relatos sobre esse aspecto foram publicados em 1959, mas a sensibilidade e seletividade dos métodos analíticos à época não permitiam análises confiáveis, principalmente para produtos com baixas concentrações. Desde então, os desenvolvimentos em química analítica permitiram uma determinação mais confiável das concentrações de CoQ 10 em vários alimentos:
| Comida | Concentração de CoQ 10 (mg / kg) | |
|---|---|---|
| Carne | coração | 113 |
| fígado | 39-50 | |
| músculo | 26-40 | |
| Carne de porco | coração | 12-128 |
| fígado | 23–54 | |
| músculo | 14-45 | |
| Frango | seio | 8–17 |
| coxa | 24-25 | |
| ASA | 11 | |
| Peixe | sardinha | 5-64 |
| cavala : | ||
| - carne vermelha | 43-67 | |
| - carne branca | 11-16 | |
| salmão | 4-8 | |
| atum | 5 | |
| Óleos | soja | 54–280 |
| Oliva | 4-160 | |
| semente de uva | 64-73 | |
| girassol | 4-15 | |
| canola | 64-73 | |
| Nozes | amendoim | 27 |
| noz | 19 | |
| semente de gergelim | 18-23 | |
| pistache | 20 | |
| avelã | 17 | |
| amêndoa | 5-14 | |
| Legumes | salsa | 8-26 |
| brócolis | 6-9 | |
| couve-flor | 2-7 | |
| espinafre | até 10 | |
| repolho chinês | 2-5 | |
| Fruta | abacate | 10 |
| groselha preta | 3 | |
| uva | 6-7 | |
| morango | 1 | |
| laranja | 1-2 | |
| Toranja | 1 | |
| maçã | 1 | |
| banana | 1 | |
Carne e peixe são as fontes mais ricas de CoQ 10 na dieta ; níveis acima de 50 mg / kg podem ser encontrados na carne bovina , suína e coração e fígado de frango . Os produtos lácteos são fontes muito mais pobres de CoQ 10 do que os tecidos animais. Os óleos vegetais também são muito ricos em CoQ 10 . Dentre os vegetais, a salsa e a perilla são as fontes mais ricas de CoQ 10 , mas diferenças significativas em seus níveis de CoQ 10 podem ser encontradas na literatura. Brócolis , uvas e couve - flor são fontes modestas de CoQ 10 . A maioria das frutas e bagas representam uma fonte pobre a muito pobre de CoQ 10 , com exceção dos abacates , que têm um teor relativamente alto de CoQ 10 .
Ingestão
No mundo desenvolvido, a ingestão diária estimada de CoQ 10 foi determinada em 3-6 mg por dia, derivada principalmente de carne.
Efeito do calor e processamento
Cozinhar por fritura reduz o conteúdo de CoQ 10 em 14–32%.
Veja também
- Idebenona - análogo sintético com propriedades geradoras de oxidantes reduzidas
- Mesilato de mitoquinona - análogo sintético com permeabilidade mitocondrial melhorada
Referências
links externos
- "Lista de ingredientes CoQ 10 verificados pela USP " . Convenção Farmacopéica dos EUA. Arquivado do original em 9 de fevereiro de 2009.
- "Coenzima Q 10 " . Instituto Nacional do Câncer . 23 de setembro de 2005.
- Bonakdar, Robert Alan; Guarneri, Erminia (15 de setembro de 2005). "Coenzima Q 10 " . Médico de Família Americano . 72 (6): 1065–1070. PMID 16190504 .