Ácido arsenoso - Arsenous acid
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Ácido arsoroso
|
|
| Outros nomes
Ácido
arsênico óxido de arsênio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| H 3 AsO 3 | |
| Massa molar | 125,94 g / mol |
| Aparência | Só existe em soluções aquosas |
| Base conjugada | Arsenita |
| -51,2 · 10 −6 cm 3 / mol | |
| Perigos | |
| Riscos principais | Tóxico, corrosivo |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
[1910,1018] TWA 0,010 mg / m 3 |
|
REL (recomendado)
|
Ca C 0,002 mg / m 3 [15 minutos] |
|
IDLH (perigo imediato)
|
Ca [5 mg / m 3 (como As)] |
| Compostos relacionados | |
|
Compostos relacionados
|
Ácido arsênico |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
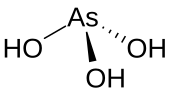
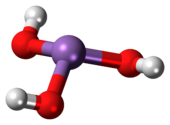
Ácido arsenoso (ou ácido arsenioso ) é o composto inorgânico com a fórmula H 3 AsO 3 . É conhecido que ocorre em soluções aquosas , mas não foi isolado como um material puro, embora este fato não diminua o significado do As (OH) 3 .
Propriedades
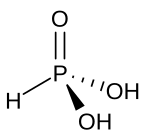
As (OH) 3 é uma molécula piramidal que consiste em três grupos hidroxila ligados ao arsênio. O espectro de 1 H NMR de soluções de ácido arsenoso consiste em um único sinal consistente com a alta simetria da molécula. Em contraste, o ácido fosforoso nominalmente relacionado H 3 PO 3 adota a estrutura HPO (OH) 2 . O análogo estrutural do ácido arsenoso (P (OH) 3 ) é um componente de equilíbrio muito menor de tais soluções. Os comportamentos diferentes dos compostos As e P refletem uma tendência em que os estados de alta oxidação são mais estáveis para membros mais leves dos elementos do grupo principal do que seus congêneres mais pesados.
Um tautômero do ácido arsenoso é HAsO (OH) 2 , que é chamado de ácido arsônico . Não foi isolado ou bem caracterizado.
Síntese
A preparação de As (OH) 3 envolve uma hidrólise lenta de trióxido de arsênio na água. A adição de base converte o ácido arsenoso em íons arsenito [AsO (OH) 2 ] - , [AsO 2 (OH)] 2− e [AsO 3 ] 3− .
Reações
Com seu primeiro p K a sendo 9,2, As (OH) 3 é um ácido fraco. As reações atribuídas ao trióxido de arsênio aquoso são devidas ao ácido arsenoso e suas bases conjugadas.
Como o trióxido de arsênio, o ácido arsênico às vezes é anfotérico . Por exemplo, ele reage com os ácidos clorídrico, bromídrico e iodídrico para produzir tricloreto de arsênio, tribrometo e triiodeto.
- As (OH) 3 + 3 HCl ⇌ AsCl 3 + 3 H 2 O
- As (OH) 3 + 3 HBr ⇌ AsBr 3 + 3 H 2 O
- As (OH) 3 + 3 HI ⇌ AsI 3 + 3 H 2 O
A reação de ácido arsenoso com iodeto de metila dá ácido metilarsônico . Esta conversão historicamente significativa é a reação de Meyer :
- As (OH) 3 + CH 3 I + NaOH ⇌ CH 3 AsO (OH) 2 + NaI + H 2 O
A alquilação ocorre no arsênio e o estado de oxidação do arsênio aumenta de +3 para +5.
Toxicologia
Os compostos que contêm arsênio são altamente tóxicos e cancerígenos . O anidrido forma de ácido arsenioso, trióxido de arsénico , é utilizado como um herbicida , pesticida , e raticida .
