Alameticina - Alamethicin

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
N -acetil-2-methylalanyl- L -prolil-2-methylalanyl- L -alanil-2-methylalanyl- L -alanyl- L -glutaminyl-2-methylalanyl- L -valil-2-methylalanylglycyl- L -leucil-2- metilalanil- L -prolil- L -valil-2-metilalanil-2-metilalanil- L -α-glutamil- N 1 - [(1 S ) -1-benzil-2-hidroxietil] - L- glutamamida
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.121.626 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 92 H 150 N 22 O 25 | |
| Massa molar | 1964,31 g / mol |
| Aparência | Sólido esbranquiçado |
| Ponto de fusão | 255 a 270 ° C (491 a 518 ° F; 528 a 543 K) |
| Insolúvel | |
| Solubilidade em DMSO , metanol , etanol | Solúvel |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
A alameticina é um antibiótico peptídeo formador de canais , produzido pelo fungo Trichoderma viride . Pertence aos peptídeos peptaibol que contêm o resíduo de aminoácido não proteinogênico Aib ( ácido 2-aminoisobutírico ). Este resíduo induz fortemente a formação da estrutura alfa-helicoidal . A sequência do peptídeo é:
Ac-Aib-Pro-Aib-Ala-Aib-Ala-Gln-Aib-Val-Aib-Gly-Leu-Aib-Pro-Val-Aib-Aib-Glu-Gln-Phl
(Ac = acetil, Phl = fenilalaninol , Aib = ácido 2-aminoisobutírico )
Nas membranas celulares , forma canais iônicos dependentes de voltagem por agregação de quatro a seis moléculas .
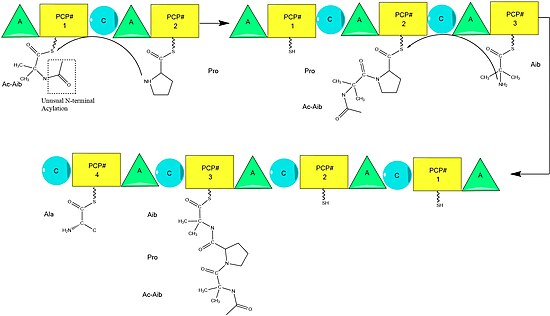
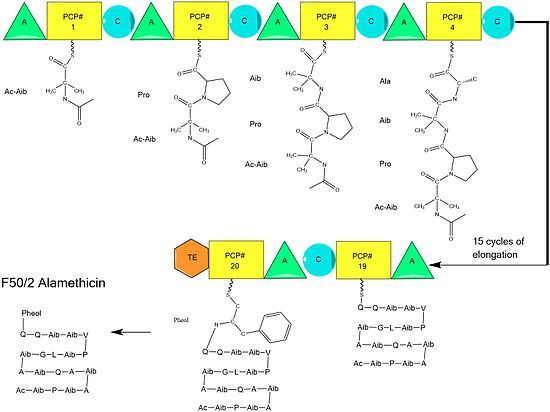
Biossíntese
A biossíntese de alameticina é hipotetizada como catalisada pela alameticina sintase, uma sintase de peptídeo não ribossômico (NRPS) isolada pela primeira vez em 1975. Embora existam várias sequências do peptídeo de alameticina aceitas, as evidências sugerem que todos seguem o mecanismo geral de NRPS com pequenas variações em aminoácidos selecionados . Começando com a acilação do terminal N do primeiro ácido aminoisobutírico na enzima ALM sintase por Acetil-CoA , isso é seguido pela condensação sequencial de aminoácidos por cada unidade modular da sintetase. Os aminoácidos são inicialmente adenilados por um domínio de " adenililação " (A) antes de serem ligados por uma ligação tioéster a uma proteína transportadora de proteína transportadora de acila semelhante a peptidila. A cadeia em crescimento é ligada ao aminoácido contendo PCP pelo domínio de "condensação" (C), seguido por outra rodada das mesmas reações pelo próximo módulo.
A montagem é completada pela adição de fenilalaninol, um substrato incomum semelhante a um aminoácido. Após a adição de fenilalaninol, a cadeia peptídica completa é clivada pelo domínio tioesterase, clivando a ligação tioéster e deixando um álcool.
Referências
Leitura adicional
- Jones, LR; Maddock, SW; Besch, HR Jr (1980). "Efeito de desmascaramento da alameticina na (Na +, K +) - ATPase, adenilato ciclase acoplada ao receptor beta-adrenérgico e atividades de proteína quinase dependente de cAMP de vesículas sarcolemais cardíacas" . J. Biol. Chem . 255 (20): 9971–9980. doi : 10.1016 / S0021-9258 (18) 43488-6 . PMID 6253461 .
- Explorar estruturas de Alameticina no banco de dados de proteínas
-
Alameticina em Norine
- De "Um modelo de canal iônico controlado por voltagem inferido da estrutura cristalina da alameticina com resolução de 1,5-A." Fox Jr, RO; Richards, FM (1982). "Um modelo de canal iônico controlado por voltagem inferido da estrutura cristalina da alameticina com resolução de 1,5-A". Nature . 300 (5890): 325–30. Bibcode : 1982Natur.300..325F . doi : 10.1038 / 300325a0 . PMID 6292726 . S2CID 4278453 .
- Leitgeb, Balázs; Szekeres, András; Manczinger, László; Vágvölgyi, Csaba; Kredics, László (01-06-2007). "A História da Alameticina: Uma Revisão do Peptaibol Mais Extensivamente Estudado". Química e Biodiversidade . 4 (6): 1027–1051. doi : 10.1002 / cbdv.200790095 . ISSN 1612-1880 . PMID 17589875 . S2CID 40886688 .