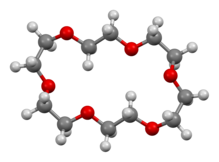
18-Coroa-6 - 18-Crown-6

|
|
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
1,4,7,10,13,16-Hexaoxaciclooctadecano |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 1619616 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.037.687 |
| Número EC | |
| 4535 | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 12 H 24 O 6 | |
| Massa molar | 264,315 g / mol |
| Densidade | 1,237 g / cm 3 |
| Ponto de fusão | 37 a 40 ° C (99 a 104 ° F; 310 a 313 K) |
| Ponto de ebulição | 116 ° C (241 ° F; 389 K) (0,2 Torr) |
| 75 g / L | |
| Perigos | |
| Pictogramas GHS |

|
| Palavra-sinal GHS | Aviso |
| H302 , H315 , H319 , H335 | |
| P261 , P264 , P270 , P271 , P280 , P301 + 312 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
| Compostos relacionados | |
|
Compostos relacionados
|
Dibenzo-18-crown-6 Triglyme Hexaaza-18-crown-6 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
18-coroa-6 é um composto orgânico com a fórmula [C 2 H 4 O] 6 e a IUPAC nome de 1,4,7,10,13,16-hexaoxacyclooctadecane. É um sólido cristalino higroscópico branco com baixo ponto de fusão. Como outros éteres coroa , 18-coroa-6 funciona como um ligante para alguns cátions metálicos com uma afinidade particular para cátions de potássio ( constante de ligação no metanol : 10 6 M −1 ). O grupo de pontos de 18-coroa-6 é S 6 . O momento dipolar de 18-coroa-6 varia em diferentes solventes e sob diferentes temperaturas. Abaixo de 25 ° C, o momento de dipolo de 18-coroa-6 é 2,76 ± 0,06 D em ciclohexano e 2,73 ± 0,02 em benzeno. A síntese dos éteres da coroa levou à atribuição do Prêmio Nobel de Química a Charles J. Pedersen .
Síntese
Este composto é preparado por uma síntese de éter Williamson modificada na presença de um cátion de modelagem: Ele também pode ser preparado pela oligomerização de óxido de etileno :
- (CH 2 OCH 2 CH 2 Cl) 2 + (CH 2 OCH 2 CH 2 OH) 2 + 2 KOH → (CH 2 CH 2 O) 6 + 2 KCl + 2 H 2 O
Pode ser purificado por destilação , onde sua tendência ao super-resfriamento se torna evidente. 18-Crown-6 também pode ser purificado por recristalização de acetonitrila quente . Inicialmente forma um solvato insolúvel. O material rigorosamente seco pode ser feito dissolvendo o composto em THF seguido pela adição de NaK para dar [K (18-coroa-6)] Na, um sal alcaleto .
A análise cristalográfica revela uma molécula relativamente plana, mas onde os centros de oxigênio não estão orientados na geometria simétrica idealizada de 6 vezes normalmente mostrada. A molécula sofre uma mudança conformacional significativa após a complexação.
Reações
O 18-Crown-6 possui alta afinidade com o íon hidrônio H 3 O + , pois pode caber dentro do éter da coroa. Assim, a reação de 18-coroa-6 com ácidos fortes dá o cátion . Por exemplo, a interação de 18-coroa-6 com gás HCl em tolueno com um pouco de umidade dá uma camada de líquido iônico com a composição , a partir da qual o sólido pode ser isolado em repouso. A reação da camada de líquido iônico com dois equivalentes molares de água dá o produto cristalino .
Formulários
18-Crown-6 liga-se a uma variedade de pequenos cátions, usando todos os seis oxigênios como átomos doadores. Os éteres de coroa podem ser usados em laboratório como catalisadores de transferência de fase . Os sais que são normalmente insolúveis em solventes orgânicos são tornados solúveis pelo éter de coroa. Por exemplo, o permanganato de potássio se dissolve em benzeno na presença de 18-coroa-6, originando o chamado "benzeno roxo", que pode ser usado para oxidar diversos compostos orgânicos.
Várias reações de substituição também são aceleradas na presença de 18-coroa-6, que suprime o emparelhamento de íons. Os ânions tornam-se assim nucleófilos nus . Por exemplo, usando 18-coroa-6, o acetato de potássio é um nucleófilo mais poderoso em solventes orgânicos:
- [K (18-coroa-6) + ] OAc - + C 6 H 5 CH 2 Cl → C 6 H 5 CH 2 OAc + [K (18-coroa-6) + ] Cl -
O primeiro sal de eletrídeo a ser examinado com cristalografia de raios-X , [Cs (18-coroa-6) 2 ] + · e - , foi sintetizado em 1983. Este sólido altamente sensível ao ar e à umidade tem uma estrutura molecular em sanduíche, onde o elétron está preso dentro de cavidades de rede quase esféricas. No entanto, a distância elétron-elétron mais curta é muito longa (8,68 Å) para tornar este material um condutor de eletricidade.
Referências
- ^ a b c d e f Steed, Jonathan W .; Atwood, Jerry L. (2009). Supramolecular Chemistry (2ª ed.). Wiley. ISBN 978-0-470-51233-3.
- ^ Caswell, Lyman R .; Savannunt, Diana S. (janeiro de 1988). "Efeitos da temperatura e do solvente nos momentos dipolares experimentais de três éteres coroa". J. Heterocyclic Chem . 25 (1): 73–79. doi : 10.1002 / jhet.5570250111 .
- ^ a b Gokel, George W .; Cram, Donald J .; Liotta, Charles L .; Harris, Henry P .; Cook, Fred L. (1977). "18-Coroa-6". Org. Synth . 57 : 30. doi : 10.15227 / orgsyn.057.0030 .
- ^ Jilek, Robert E .; Fischer, Paul J .; Ellis, John E. (2014). Bis (1,2-Bis (Dimetilfosfano) Etano) Tricarboniltitânio (0) e Hexacarboniltitanato (2−) . Sínteses inorgânicas. 36 . pp. 127–134. doi : 10.1002 / 9781118744994.ch24 . ISBN 9781118744994.
- ^ Dunitz, JD; Seiler, P. (1974). "1,4,7,10,13,16-Hexaoxaciclooctadecano". Acta Crystallogr . B30 (11): 2739. doi : 10.1107 / S0567740874007928 .
- ^ Atwood, Jerry L .; Bott, Simon G .; Coleman, Anthony W .; Robinson, Kerry D .; Whetstone, Stephen B .; Means, C. Mitchell (dezembro de 1987). "O cátion oxônio em solventes aromáticos. Síntese, estrutura e comportamento da solução de ". Journal of the American Chemical Society . 109 (26): 8100–8101. doi : 10.1021 / ja00260a033 .
- ^ Atwood, Jerry L .; Bott, Simon G .; Means, C. Mitchell; Coleman, Anthony W .; Zhang, Hongming; Maio, Michael T. (fevereiro de 1990). "Síntese de sais do ânion dicloreto de hidrogênio em solventes aromáticos. 2. Síntese e estruturas cristalinas de e afins ". Química Inorgânica . 29 (3): 467–470. doi : 10.1021 / ic00328a025 .
- ^ Liotta, CL; Berknerin, J. (2004). "18-Coroa-6". Em Paquette, L. (ed.). Encyclopedia of Reagents for Organic Synthesis, 8 Volume Set . Encyclopedia of Reagents for Organic Synthesis . Nova York: J. Wiley & Sons. doi : 10.1002 / 047084289X.rc261 . ISBN 0471936235.
- ^ Wynn, David; et al. (1984). "A solubilidade de fluoretos de metal alcalino em solventes não aquosos com e sem éteres de coroa ...". Talanta . 31 (11): 1036–1040. doi : 10.1016 / 0039-9140 (84) 80244-1 .
- ^ Cook, Fred L .; Bowers, Chauncey W .; Liotta, CL (novembro de 1974). "Química de ânions nus. III. Reações do complexo 18-coroa-6 de cianeto de potássio com substratos orgânicos em solventes orgânicos apróticos". The Journal of Organic Chemistry . 39 (23): 3416–3418. doi : 10.1021 / jo00937a026 .

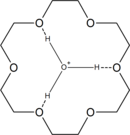
![{\ displaystyle {\ ce {[H3O.18-crown-6] +}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/05959c612544dc9b3cb3553c23497b6cb0b79eae)
![{\ displaystyle {\ ce {[H3O.18-crown-6] + [HCl2] ^ {-}.}} 3.8 {\ ce {C6H5Me}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f6c99a07eb7055bb324034bb06c5b326acac2040)
![{\ displaystyle {\ ce {[H3O.18-crown-6] + [HCl2] -}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4a39f9fa425e04e4fb9893a6534ec9ebe14ec13d)
![{\ displaystyle {\ ce {(H5O2) [H3O.18-coroa-6] Cl2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ea4d202cf03dca6460e22c323e76cdeaa4e4da33)

![{\ displaystyle {\ ce {[H3O + .18-crown-6] [Cl-H-Cl]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/570b60b09f20cda7d97987382a006e776dd9ed9e)
![{\ displaystyle {\ ce {[K.18-crown-6] [Cl-H-Cl]}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/033a571d20719af08d7a5198f57da59afc23a226)
![{\ displaystyle {\ ce {[Mg.18-crown-6] [Cl-H-Cl] 2}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/abf6c19ea8d8195eea1d4679f2a696d69feb2f72)
![{\ displaystyle {\ ce {[H3O.18-crown-6] [Cl-H-Cl]}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/53c829dc937cd5208e3ccb616bdddf618c8b6332)
![{\ displaystyle {\ ce {[H3O.18-crown-6] [Br-H-Br]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d1dbd94a5bd7bbec553563db4f4df5d9496b9cf1)